Clear Sky Science · de
Gehirnweite Kartierung zeigt zeitliche und geschlechtsspezifische Opioidwirkungen
Warum das für die Opioidkrise wichtig ist
Opioid‑Medikamente wie Morphin sind starke Schmerzmittel, treiben aber zugleich eine verheerende Suchtepidemie voran. Um bessere Behandlungen zu entwickeln, müssen Forscher genau verstehen, wie diese Medikamente die Aktivität im gesamten Gehirn verändern und wie diese Effekte zwischen Männern und Frauen sowie über die Zeit variieren. Diese Studie nutzte hochmoderne 3D‑Gehirnbildgebung bei Mäusen, um eine gehirnweite Karte von Morphins Auswirkungen auf Nervenzellen zu erstellen und zu zeigen, wann, wo und bei wem das Medikament die Gehirnaktivität am stärksten umgestaltet.
Das ganze Gehirn auf einmal sehen
Statt sich auf einige bekannte Hotspots zu konzentrieren, wollten die Forschenden das gesamte Mäusehirn in Einzelzellauflösung untersuchen. Nachdem männlichen und weiblichen Mäusen entweder Morphin oder Kochsalzlösung injiziert worden war, entnahmen sie die Gehirne eine bzw. vier Stunden später. Die Gehirne wurden optisch transparent gemacht und für c‑Fos gefärbt, ein Protein, das in kürzlich aktiven Neuronen aufleuchtet. Mit schnellen Konfokalmikroskopen erfassten sie für jedes ganze Gehirn riesige 3D‑Bilddateien. Eine maßgeschneiderte Rechenpipeline erkannte dann automatisch einzelne leuchtende Zellen und ordnete ihre Positionen einem standardisierten Maus‑Gehirnatlas zu, sodass das Team aktive Zellen in Hunderten benannter Regionen gleichzeitig zählen konnte. 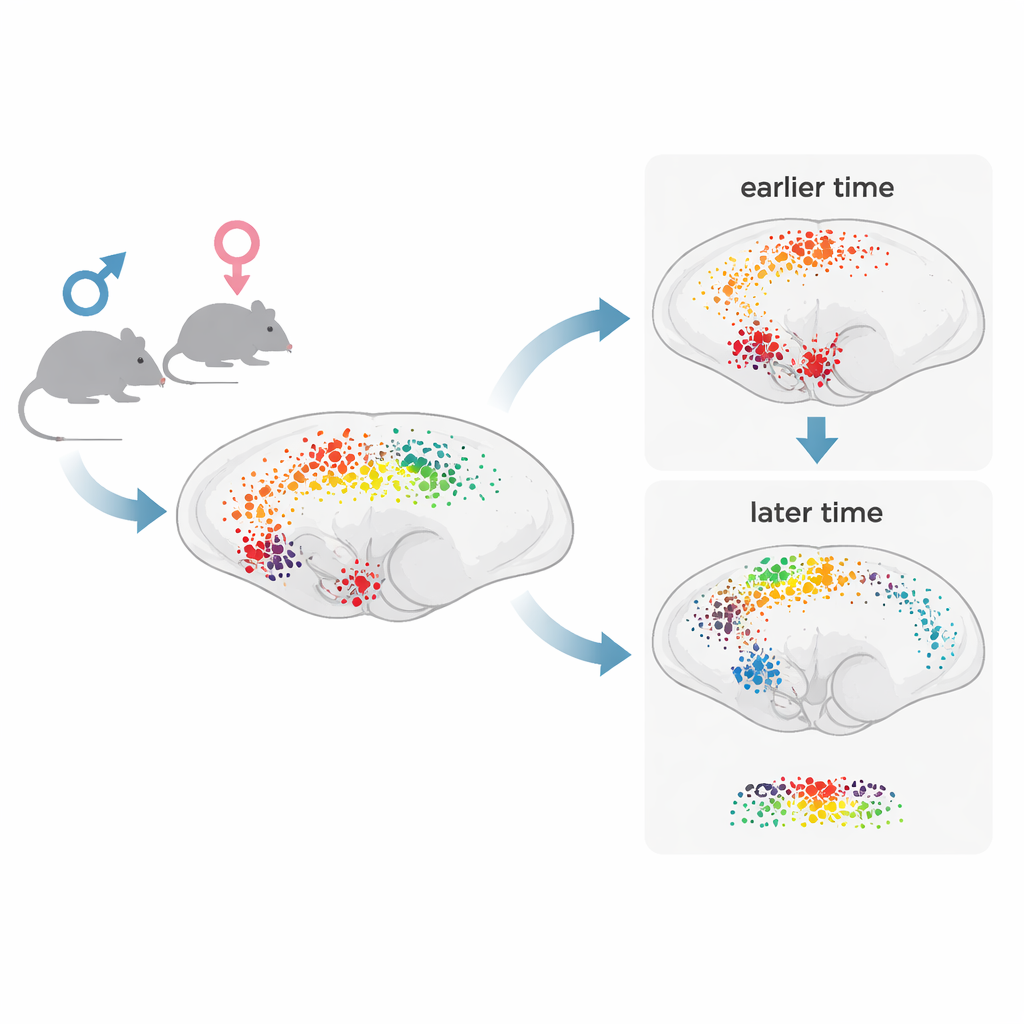
Wie sich Morphins Effekte über die Zeit ausbreiten
Die Karten zeigten, dass eine Einzeldosis Morphin im Vergleich zu Kontrollen breit die neuronale Aktivität erhöht, wobei nicht alle Regionen gleich stark oder zum selben Zeitpunkt reagieren. Etwa zwei Drittel der großen Hirnstrukturen zeigten nach Morphin mehr aktive Zellen, mit besonders starken Reaktionen in tiefen Regionen wie Hirnstamm, Pons und Hypothalamus sowie dichter Aktivierung in bestimmten Schichten der Großhirnrinde. Nach einer Stunde gehörten viele der am stärksten reagierenden Bereiche zu klassischen Komponenten von Schmerzstillung und Belohnungsschaltungen, etwa die Periaquäduktalgrauzone, der Nucleus accumbens, das ventrale Tegmentum, thalamische Relaiskerne und Hirnstammareale, die an Schmerzmodulation und Körperfunktionen beteiligt sind. Nach vier Stunden zeigten insgesamt weniger Regionen starke Veränderungen, aber das Aktivitätsmuster hatte sich verschoben: Signale breiteten sich stärker in kortikale und hippocampale Bereiche aus, die mit Lernen, Gedächtnis und langanhaltender Anpassung verknüpft sind. Das unterstützt ein „Zwei‑Wellen“‑Modell, bei dem eine frühe Welle subkortikaler Schaltkreise von einer langsameren Welle kortikaler Plastizität gefolgt wird.
Unterschiedliche Gehirnantworten bei Männern und Frauen
Die Studie enthüllte zudem auffällige Geschlechtsunterschiede. Allgemein zeigten männliche Mäuse in vielen wichtigen Belohnungs‑ und Stressregionen stärkere morphin‑induzierte Aktivierung als weibliche. Dazu gehörten der Nucleus accumbens, das laterale Septum, das ventrale Pallidum, mehrere Amygdala‑Kerne, der Nucleus des Stria terminalis und Teile des Hippocampus sowie des cingulären Kortex. Bei den Männchen erhöhte Morphin die Aktivität überwiegend zu beiden Zeitpunkten. Bei den Weibchen war das Bild komplexer: Die Aktivität war oft nach einer Stunde gedämpft und nach vier Stunden erhöht, was vermutlich stärkere Stressreaktionen auf die Injektion in der weiblichen Kontrollgruppe und Unterschiede in der Kopplung der Opioidrezeptoren an Gehirnzellen widerspiegelt. Die Daten machen deutlich, dass dieselbe Dosis unterschiedliche Netzwerke in männlichen und weiblichen Gehirnen aktiviert, insbesondere in Regionen, die mit Verlangen, Entzug, Stimmung und Schlaf verbunden sind. 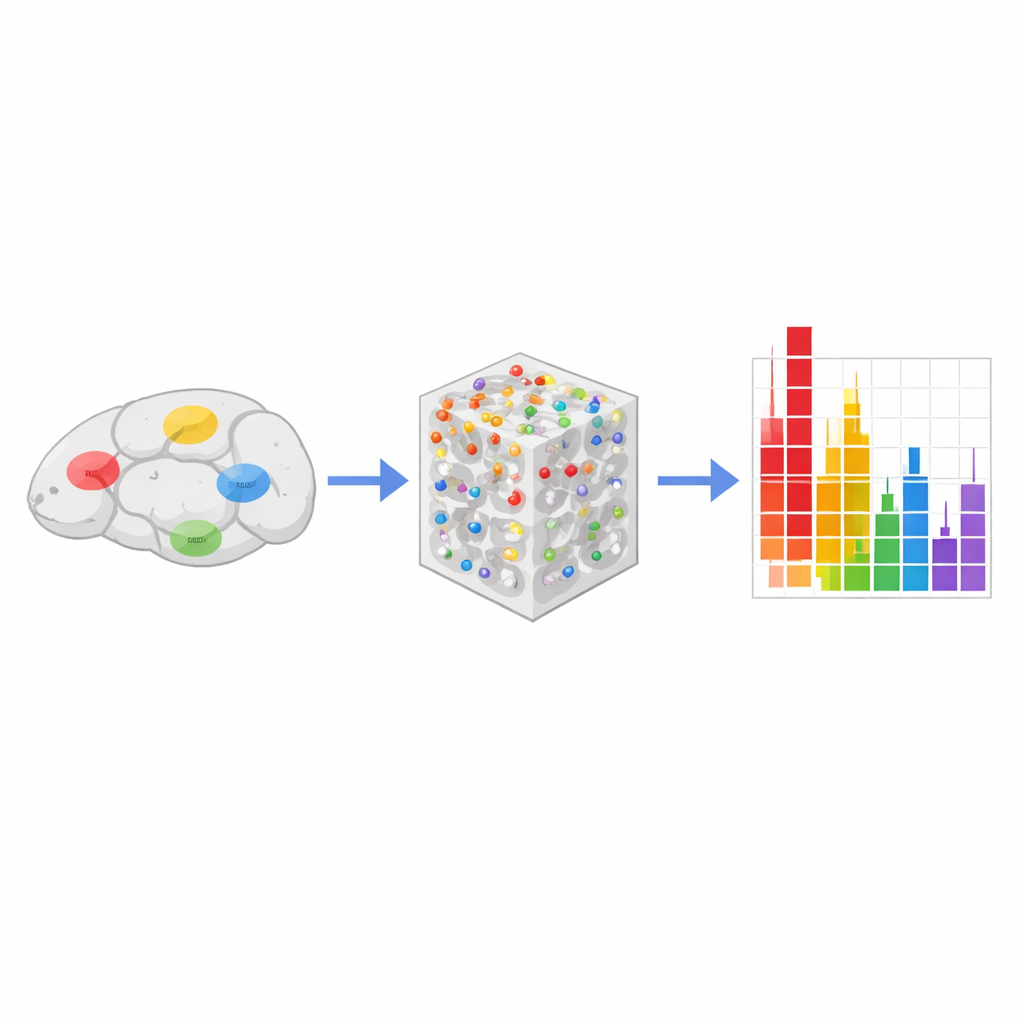
Ein neuer Fahrplan für die Untersuchung süchtig machender Medikamente
Über die bekannten Suchtzentren hinaus deckte die gehirnweite Untersuchung viele Regionen auf, die normalerweise nicht mit Opioiden assoziiert werden, wie bestimmte sensorische und Assoziationskortizes, spezifische thalamische und hypothalamische Kerne, Hirnstammstrukturen und sogar Teile des Kleinhirns. Viele dieser Areale exprimieren Opioidrezeptoren, waren in diesem Kontext aber selten untersucht worden. Durch die Kombination großflächiger Bildgebung mit maschinellen Lernmodellen zeigten die Autorinnen und Autoren, dass die genaue Vorhersage, ob eine Maus Morphin erhalten hatte, Informationen aus vielen Regionen gleichzeitig erfordert — ein Hinweis darauf, wie verteilt die Wirkung des Medikaments tatsächlich ist. Für Laien lautet die Kernaussage: Morphin trifft nicht nur ein einzelnes Lustzentrum, sondern sendet Wellen über weitläufige Gehirnnetzwerke, wobei Zeitpunkt und Geschlecht bestimmen, welche Schaltkreise am stärksten betroffen sind. Dieser neue Kartierungsansatz bietet ein kraftvolles Werkzeug, um Gehirnziele für sicherere Schmerzbehandlungen und effektivere Therapien bei Opioidgebrauchsstörungen zu identifizieren.
Zitation: Vasylieva, I., Smith, R., Aravind, E. et al. Brain-wide mapping reveals temporal and sexually dimorphic opioid actions. Commun Biol 9, 466 (2026). https://doi.org/10.1038/s42003-026-09730-8
Schlüsselwörter: Opioidabhängigkeit, Gehirnkartierung, Geschlechtsunterschiede, Morphin, neurale Aktivität