Clear Sky Science · fr
La protéine liée à l’ARN Squid régule le développement embryonnaire de l’intestin moyen via l’épissage alternatif d’Axin chez Bombyx mori
Pourquoi les petits intestins de ver à soie comptent
Tous les embryons animaux, des insectes aux humains, doivent construire un système digestif fonctionnel avant de pouvoir croître et survivre. Les insectes sont particulièrement intéressants parce que leurs intestins sont à la fois très efficaces et des cibles majeures pour la lutte antiparasitaire. Cette étude utilise le ver à soie domestique, Bombyx mori, pour révéler comment une unique protéine liant l’ARN appelée Squid contribue à façonner l’intestin moyen embryonnaire — la région clé pour la dégradation des aliments et l’absorption des nutriments. En dévoilant comment Squid ajuste finement les messages génétiques, ce travail éclaire des principes fondamentaux de la formation des organes et suggère de nouvelles approches pour contrôler les ravageurs agricoles sans recours massif aux produits chimiques.
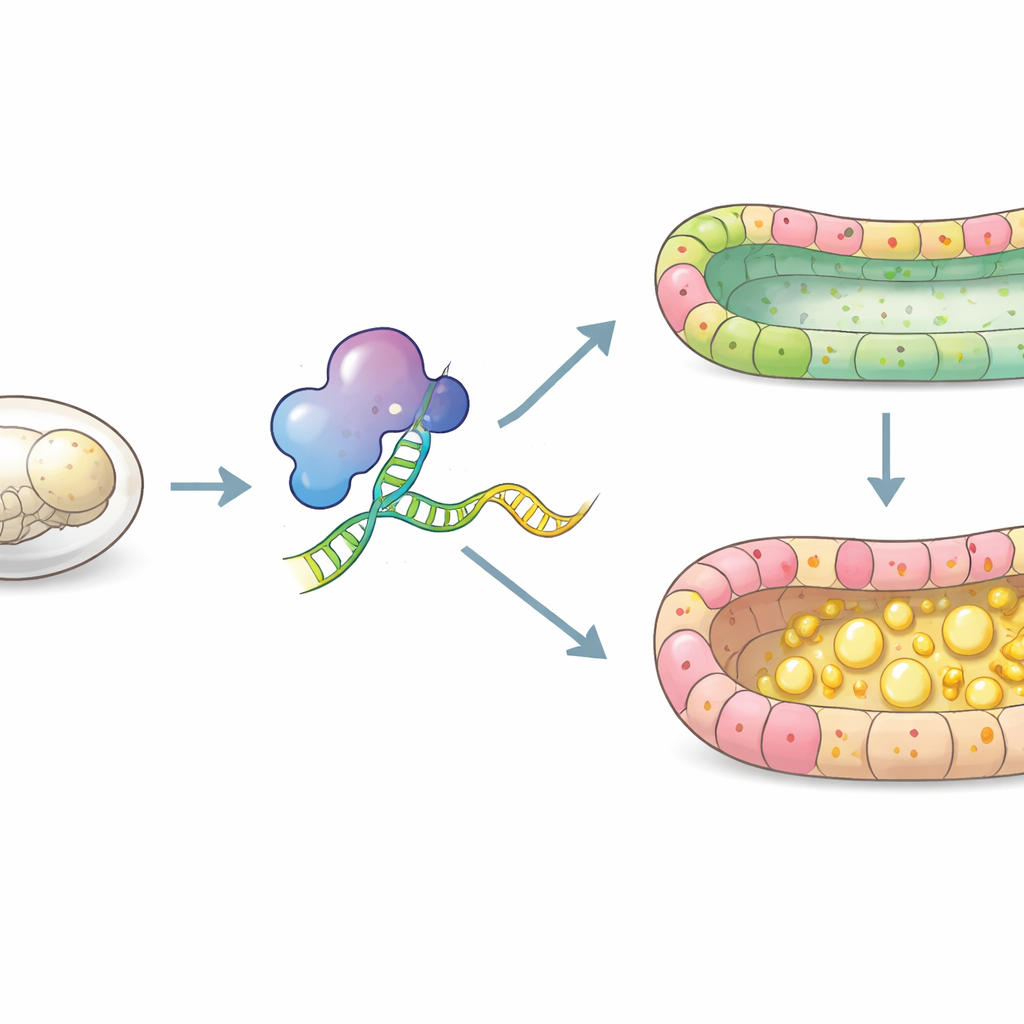
Construire un intestin d’insecte fonctionnel
L’intestin moyen des insectes est un tube simple tapissé d’une seule couche de cellules épithéliales, et pourtant il assure la digestion, l’absorption des nutriments, la défense immunitaire et la réparation tissulaire. Chez les embryons de ver à soie, cette couche est normalement organisée en trois types cellulaires principaux : des cellules souches intestinales situées à la base, des cellules prismatiques qui sécrètent des enzymes digestives et absorbent les nutriments, et des cellules caliciformes qui contribuent à gérer l’environnement interne de l’intestin. Les auteurs se sont concentrés sur Squid, membre d’une grande famille de protéines qui lient l’ARN et influencent la manière dont les messages génétiques sont modifiés et utilisés dans les cellules. Des travaux antérieurs laissaient entendre que Squid était active pendant l’embryogenèse du ver à soie, mais son rôle précis dans le développement de l’intestin était inconnu.
Quand Squid manque, l’intestin se désorganise
En utilisant l’édition génomique CRISPR/Cas9, les chercheurs ont inactivé le gène Squid dans des embryons de ver à soie. De nombreux embryons dépourvus de Squid sont morts avant l’éclosion et présentaient un développement retardé par rapport à leurs frères normaux. L’examen au microscope a révélé que, au lieu d’une paroi intestinale régulière, les embryons déficients en Squid avaient un épithélium désorganisé où les types cellulaires habituels étaient difficiles à distinguer. La lumière intestinale — la cavité centrale où la nourriture passerait — était encombrée de larges gouttelettes lipidiques, indiquant que les graisses n’étaient pas correctement traitées ou absorbées. À des stades plus précoces, la division cellulaire semblait s’arrêter normalement, mais les cellules n’ont pas achevé leur maturation en types spécialisés appropriés, ce qui suggère que Squid est crucial pour la différenciation plutôt que pour la croissance simple.
L’approvisionnement énergétique et la digestion s’arrêtent sans un intestin fonctionnel
Comme les embryons d’insectes dépendent fortement des lipides œuf stockés comme carburant, l’équipe a cherché à savoir si l’intestin défaillant des mutants Squid perturbait cette voie énergétique. La coloration des lipides a montré de grandes quantités de graisses stagnantes dans la lumière intestinale des embryons mutants, mais pas chez les embryons normaux. Une enquête large de l’activité génique a révélé que des centaines de gènes impliqués dans le métabolisme de base — tels que la dégradation des sucres, le cycle de l’acide citrique et la production d’acides aminés — étaient réprimés chez les mutants. Des tests plus ciblés ont confirmé que les transcrits codant pour des enzymes liées à la digestion et à l’absorption, y compris des étapes clés de la dégradation des lipides, étaient significativement réduits. Ensemble, ces résultats indiquent que sans Squid, l’intestin moyen embryonnaire ne peut pas convertir efficacement les nutriments stockés en énergie utilisable, ce qui contribue à la mort embryonnaire.
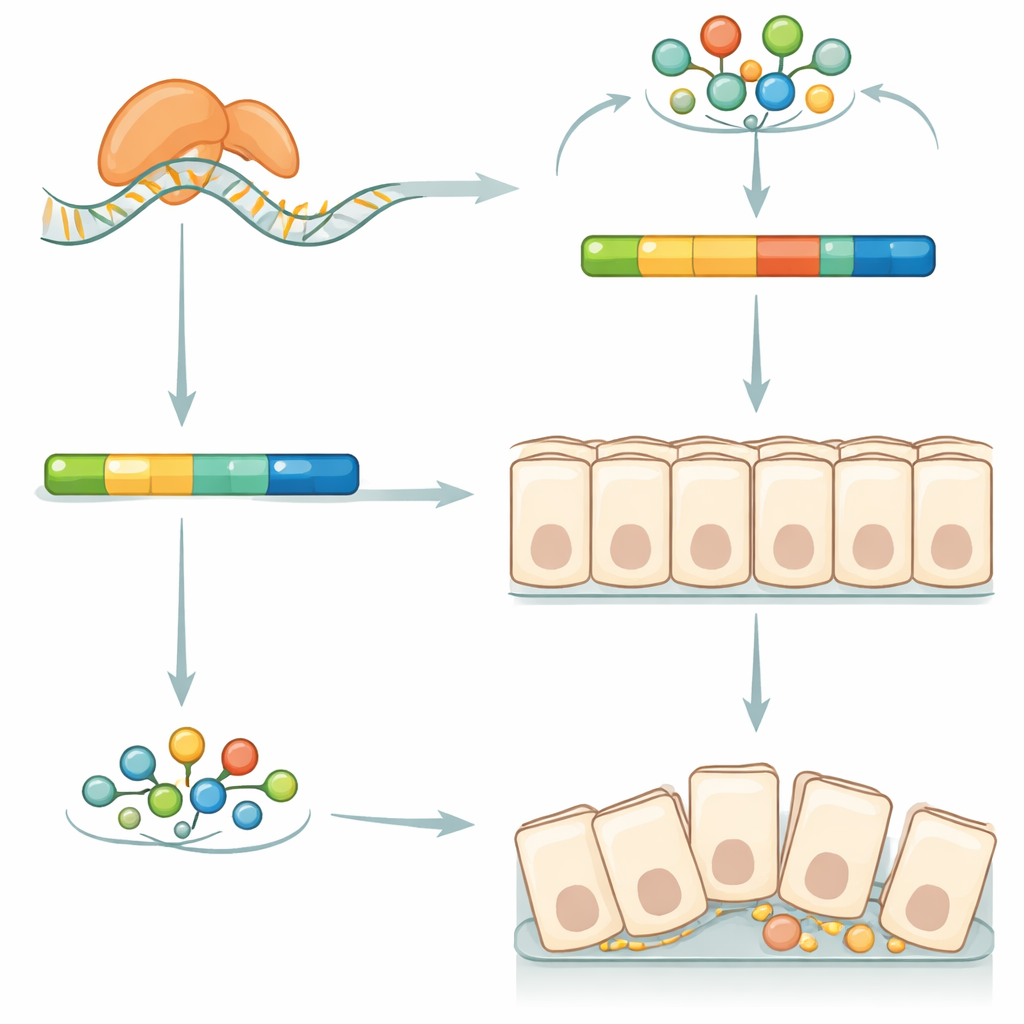
Un réglage fin sur une voie de signalisation classique
Pour comprendre comment Squid produit des effets aussi étendus, les auteurs ont recherché les ARN auxquels il se lie physiquement. Ils ont isolé Squid à partir d’extraits d’embryons et séquencé les ARN associés, identifiant plus de deux mille cibles potentielles. La comparaison entre embryons normaux et déficients en Squid a montré que des dizaines de ces cibles modifiaient l’épissage de leurs messages ARN — le processus de découpage et de rattachement de segments pour produire différentes versions protéiques. Beaucoup des gènes affectés appartenaient à la voie de signalisation bien connue Wnt/β‑caténine, centrale dans le développement intestinal chez de nombreux animaux. Une cible remarquable était Axin, une protéine échafaudage qui contribue à réguler la stabilité de la β‑caténine, un signal clé et composant structurel des tissus épithéliaux.
Comment un choix d’épissage change la forme de l’intestin
Axin existe sous deux formes chez le ver à soie : une version longue et une version plus courte dépourvue d’un petit segment de faible complexité. Chez les embryons déficients en Squid, les niveaux totaux d’Axin restaient similaires, mais l’équilibre basculait de la variante longue vers la variante courte. Ce basculement coïncidait avec une chute marquée de la β‑caténine protéique dans l’épithélium intestinal. Lorsque l’équipe surexprimait la forme longue d’Axin dans des cellules de ver à soie en culture, les niveaux de β‑caténine augmentaient ; la forme courte avait peu d’effet. Ces expériences suggèrent que Squid favorise normalement la production de la variante longue d’Axin, qui aide à maintenir des niveaux appropriés de β‑caténine pour soutenir les jonctions intercellulaires et l’organisation correcte de la couche intestinale. La perturbation de ce contrôle d’épissage délicat semble compromettre la niche des cellules souches, bloquer la différenciation normale et, en fin de compte, affaiblir l’ensemble de l’organe.
Ce que cela signifie au‑delà des vers à soie
Pour les non‑spécialistes, le message central est que la façon dont les cellules éditent leurs messages ARN peut déterminer si un organe se forme correctement. Chez les embryons de ver à soie, la protéine liant l’ARN Squid assure que un composant de signalisation clé, Axin, est épissé en la version qui maintient des niveaux sains de β‑caténine dans l’intestin moyen. Lorsque Squid est supprimé, cet équilibre est perdu, l’épithélium intestinal devient désordonné, les nutriments ne sont pas absorbés et l’embryon meurt. Comme des protéines liant l’ARN similaires et la signalisation Wnt/β‑caténine fonctionnent chez de nombreux animaux, y compris les humains, ce travail met en lumière la manière dont des modifications subtiles du traitement de l’ARN peuvent avoir des effets profonds sur le développement des tissus, la santé, et potentiellement sur des stratégies de gestion des insectes nuisibles.
Citation: Tong, C., Mo, W., Cai, M. et al. The RNA-binding protein Squid regulates embryonic midgut development via Axin alternative splicing in Bombyx mori. Commun Biol 9, 449 (2026). https://doi.org/10.1038/s42003-026-09692-x
Mots-clés: développement embryonnaire de l’intestin moyen, protéines liant l’ARN, épissage alternatif, signalisation Wnt β-caténine, ver à soie Bombyx mori