Clear Sky Science · de
Das RNA‑bindende Protein Squid reguliert die embryonale Mitteldarmentwicklung durch alternatives Spleißen von Axin in Bombyx mori
Warum winzige Seidenraupen‑Därme wichtig sind
Jeder tierische Embryo, von Insekten bis zu Menschen, muss ein funktionierendes Verdauungssystem aufbauen, bevor er wachsen und überleben kann. Insekten sind besonders interessant, weil ihre Därme sowohl hocheffizient sind als auch sich gut als Ziele für Schädlingsbekämpfung eignen. Diese Studie verwendet die heimische Seidenraupe Bombyx mori, um zu zeigen, wie ein einzelnes RNA‑bindendes Protein namens Squid den embryonalen Mitteldarm formt — die zentrale Region für den Abbau von Nahrung und die Aufnahme von Nährstoffen. Indem sie offenlegt, wie Squid Genbotschaften feinabstimmt, liefert die Arbeit Einsichten in grundlegende Prinzipien der Organbildung und deutet neue Ansätze an, um landwirtschaftliche Schädlinge ohne umfangreichen Chemikalieneinsatz zu kontrollieren.
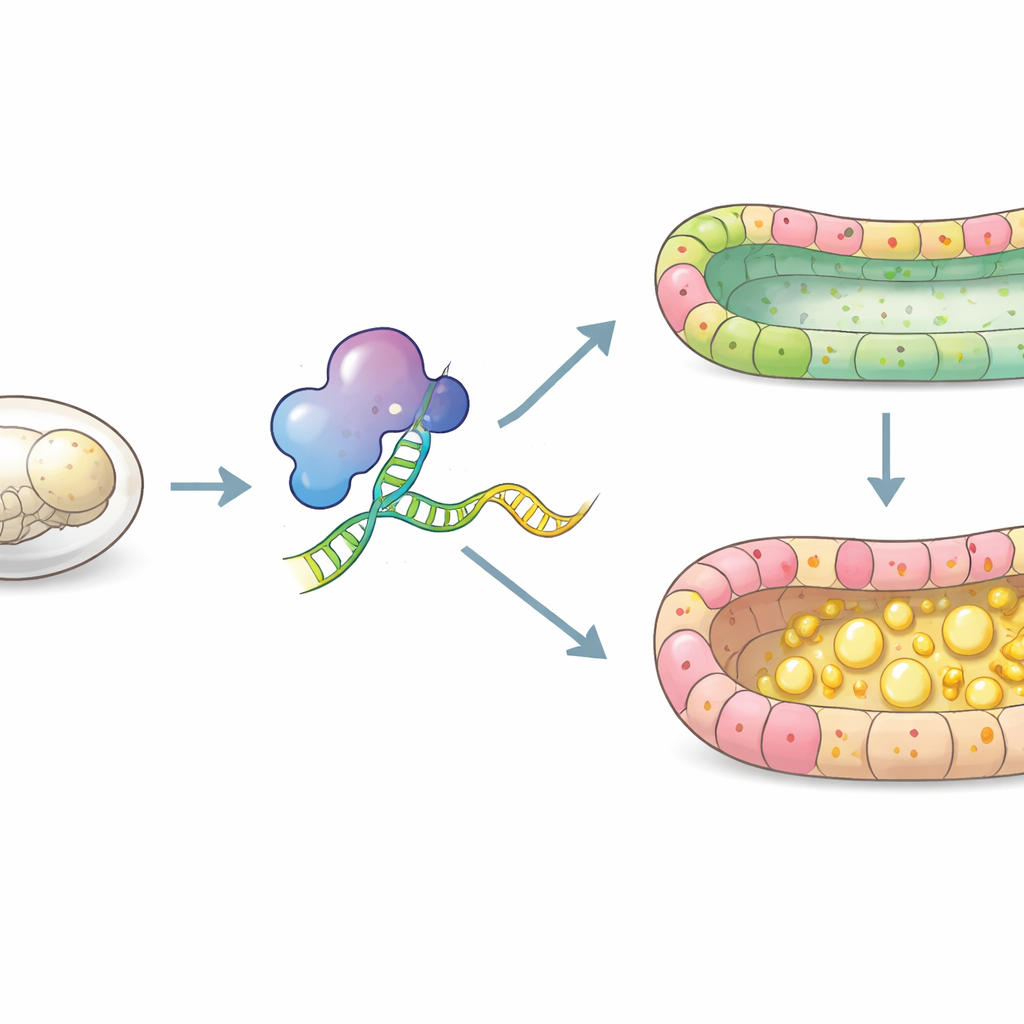
Ein funktionsfähigen Insektendarm aufbauen
Der Insektenmitteldarm ist ein einfacher Schlauch, ausgekleidet von einer einzigen Lage epithelialer Zellen, und erfüllt dennoch Verdauung, Nährstoffaufnahme, Immunabwehr und Gewebereparatur. Bei Seidenraupenembryonen ist diese Lage normalerweise in drei Hauptzelltypen organisiert: intestinale Stammzellen an der Basis, säulenförmige Zellen, die Verdauungsenzyme sezernieren und Nährstoffe aufnehmen, und Becherzellen, die das innere Milieu des Darms regulieren. Die Autoren konzentrierten sich auf Squid, ein Mitglied einer großen Proteinfamilie, die RNA bindet und beeinflusst, wie genetische Botschaften in der Zelle bearbeitet und genutzt werden. Frühere Arbeiten deuteten an, dass Squid während der Embryogenese der Seidenraupe aktiv ist, doch seine genaue Rolle bei der Darmentwicklung war unbekannt.
Fehlt Squid, bricht der Darm auseinander
Mit CRISPR/Cas9‑Geneditierung schalteten die Forschenden das Squid‑Gen in Seidenraupenembryonen aus. Viele Embryonen ohne Squid starben vor dem Schlupf und zeigten im Vergleich zu normalen Geschwistern eine verzögerte Entwicklung. Mikroskopische Untersuchungen zeigten, dass anstelle einer ordentlichen Mitteldarmwand die Squid‑defizienten Embryonen ein desorganisiertes Epithel aufwiesen, in dem die üblichen Zelltypen kaum zu unterscheiden waren. Das Darmlumen — die zentrale Höhlung, durch die Nahrung passieren würde — war mit großen Lipidtropfen gefüllt, was darauf hindeutet, dass Fette nicht richtig verarbeitet oder aufgenommen wurden. In früheren Stadien schien die Zellteilung planmäßig zu stoppen, doch die Zellen versäumten es, zu den richtigen spezialisierten Typen zu reifen, was darauf hindeutet, dass Squid eher für die Differenzierung als für einfaches Wachstum entscheidend ist.
Ohne funktionierenden Mitteldarm stocken Energieversorgung und Verdauung
Da Insektenembryonen stark auf gespeicherte Eifette als Brennstoff angewiesen sind, untersuchte das Team, ob der fehlerhafte Mitteldarm in Squid‑Mutanten diese Energieversorgung stört. Färbungen für Lipide zeigten große Fettmengen, die im Darmlumen der Mutanten zurückblieben, nicht aber in normalen Embryonen. Eine breit angelegte Analyse der Genaktivität ergab, dass Hunderte von Genen, die an der Grundversorgung des Stoffwechsels beteiligt sind — etwa Zuckerabbau, Zitronensäurezyklus und Aminosäureproduktion — in den Mutanten herunterreguliert waren. Zielgerichtete Tests bestätigten, dass Transkripte, die Verdauungs- und Aufnahmeenzyme kodieren, einschließlich zentraler Schritte beim Fettabbau, deutlich reduziert waren. Zusammengenommen deuten diese Befunde darauf hin, dass ohne Squid der embryonale Mitteldarm gespeicherte Nährstoffe nicht effizient in nutzbare Energie umwandeln kann, was zum Tod der Embryonen beiträgt.
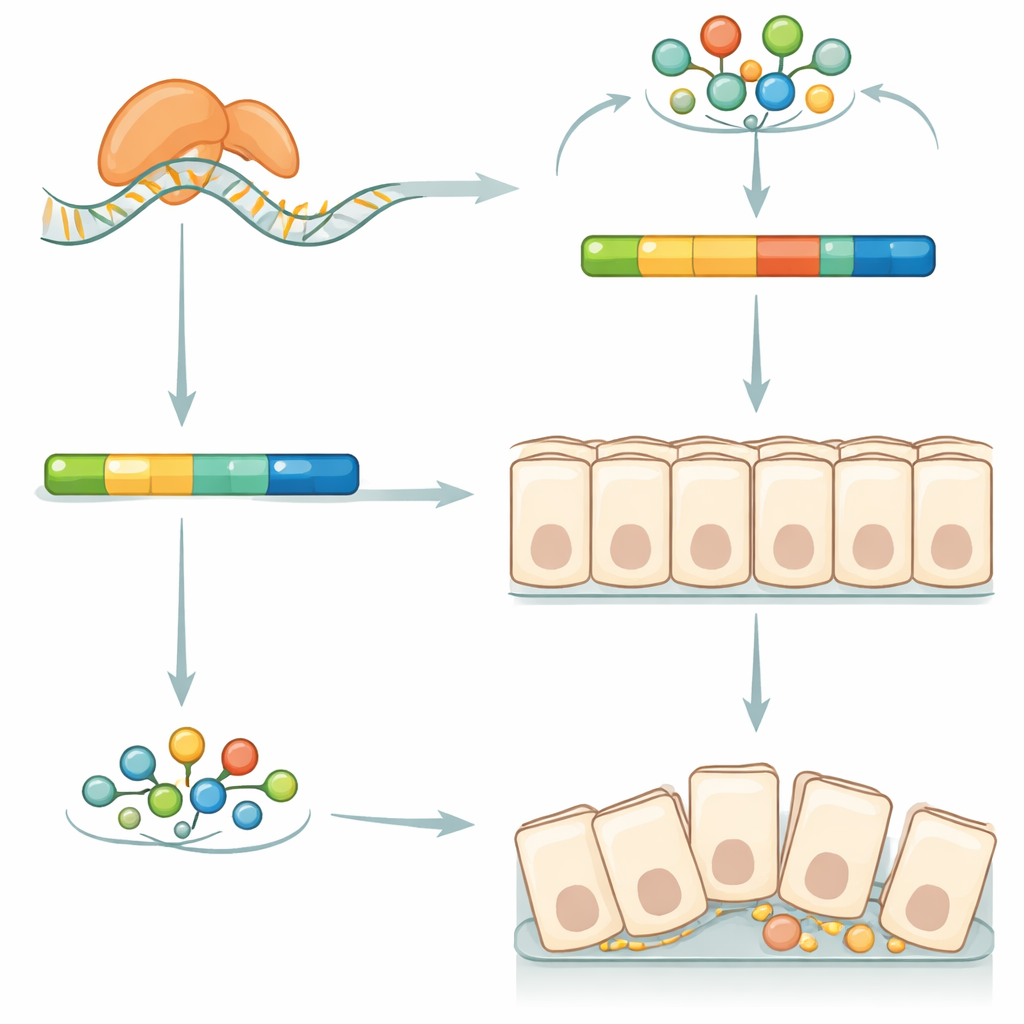
Ein feiner Stellknopf an einem klassischen Signalweg
Um zu verstehen, wie Squid so weitreichende Effekte ausübt, suchten die Autoren nach RNA‑Molekülen, an die es physisch bindet. Sie isolierten Squid aus Embryonenextrakten und sequenzierten die gebundenen RNAs und identifizierten so über zweitausend potenzielle Zielmoleküle. Der Vergleich zwischen normalen und Squid‑defizienten Embryonen zeigte, dass bei Dutzenden dieser Ziele die Art und Weise, wie ihre RNA‑Botschaften gespleißt werden — also das Ausschneiden und Neuverknüpfen von Segmenten, um verschiedene Proteinvarianten zu erzeugen — verändert war. Viele der betroffenen Gene gehörten zum bekannten Wnt/β‑Catenin‑Signalweg, der in vielen Tieren zentral für die Darmentwicklung ist. Ein herausragendes Ziel war Axin, ein Gerüstprotein, das die Stabilität von β‑Catenin reguliert, einem Schlüsselbestandteil der Signalübertragung und Struktur epithelialer Gewebe.
Wie eine einzige Spleißentscheidung den Darm umgestaltet
Axin liegt bei Seidenraupen in zwei Formen vor: einer langen Variante und einer kürzeren, der ein kleines Segment geringer Komplexität fehlt. In Squid‑defizienten Embryonen blieben die Gesamt‑Axin‑Mengen gleich, doch das Verhältnis verschob sich zugunsten der kurzen Variante. Diese Verschiebung ging mit einem starken Abfall des β‑Catenin‑Proteins im Mitteldarmepithel einher. Als das Team die lange Axin‑Form in kultivierten Seidenraupenzellen überexprimierte, stiegen die β‑Catenin‑Spiegel; die kurze Form zeigte kaum Wirkung. Diese Experimente legen nahe, dass Squid normalerweise die Produktion der langen Axin‑Variante fördert, die wiederum hilft, geeignete β‑Catenin‑Spiegel aufrechtzuerhalten, um Zell‑Zell‑Verbindungen und die richtige Organisation der Mitteldarmlage zu stützen. Die Störung dieser feinen Spleißkontrolle scheint die Stammzellnische zu untergraben, die normale Differenzierung zu blockieren und letztlich das gesamte Organ zu schwächen.
Was das über Seidenraupen hinaus bedeutet
Für Nichtfachleute lautet die zentrale Botschaft: Wie Zellen ihre RNA‑Botschaften bearbeiten, kann bestimmen, ob ein Organ korrekt entsteht. In Seidenraupenembryonen sorgt das RNA‑bindende Protein Squid dafür, dass ein wichtiges Signalprotein, Axin, so gespleißt wird, dass β‑Catenin im Mitteldarm auf gesunden Niveaus bleibt. Wenn Squid entfernt wird, gerät dieses Gleichgewicht aus den Fugen, das Darmepithel wird unordentlich, Nährstoffe werden nicht aufgenommen und der Embryo stirbt. Da ähnliche RNA‑bindende Proteine und der Wnt/β‑Catenin‑Signalweg in vielen Tieren, einschließlich des Menschen, wirken, zeigt diese Arbeit, wie subtile Veränderungen in der RNA‑Verarbeitung tiefgreifende Effekte auf Gewebeentwicklung, Gesundheit und möglicherweise auf Strategien zur Schädlingsbekämpfung haben können.
Zitation: Tong, C., Mo, W., Cai, M. et al. The RNA-binding protein Squid regulates embryonic midgut development via Axin alternative splicing in Bombyx mori. Commun Biol 9, 449 (2026). https://doi.org/10.1038/s42003-026-09692-x
Schlüsselwörter: embryonale Mitteldarmentwicklung, RNA‑bindende Proteine, alternatives Spleißen, Wnt‑β‑Catenin‑Signalweg, Seidenraupe Bombyx mori