Clear Sky Science · fr
Segmentation multi-structures efficace en IRM cardiaque pour l’évaluation cardiovasculaire avec annotations limitées en intégrant la cohérence au niveau des données et du réseau
Pourquoi cette recherche compte pour la santé cardiaque
Les examens IRM du cœur peuvent révéler des détails cruciaux sur la capacité de pompage du cœur, mais transformer ces images riches en informations en chiffres exploitables par les cliniciens nécessite généralement des tracés manuels chronophages réalisés par des experts. Cette étude présente une méthode d’intelligence artificielle (IA) capable d’apprendre à délimiter précisément les parties essentielles du cœur même lorsqu’une faible proportion des examens a été annotée par des spécialistes. En exploitant efficacement les nombreuses images non annotées déjà stockées dans les hôpitaux, l’approche pourrait rendre l’analyse cardiaque avancée plus rapide, moins coûteuse et plus largement accessible.
Transformer des images brutes du cœur en mesures utiles
Pour évaluer le fonctionnement du cœur, les cardiologues examinent plusieurs structures sur les images IRM, notamment les principales cavités de pompage et la paroi musculaire. À partir de ces éléments, ils calculent des volumes, la masse musculaire et la force de contraction—des valeurs qui guident le diagnostic, les choix thérapeutiques et le suivi à long terme pour des affections comme l’insuffisance cardiaque ou les cardiomyopathies. Aujourd’hui, ces structures sont souvent tracées à la main ou à l’aide de logiciels nécessitant encore une supervision rapprochée. La nouvelle méthode vise à automatiser largement cette étape, afin que les contours du ventricule gauche, du ventricule droit et du muscle cardiaque puissent être générés rapidement et de façon cohérente pour chaque patient.
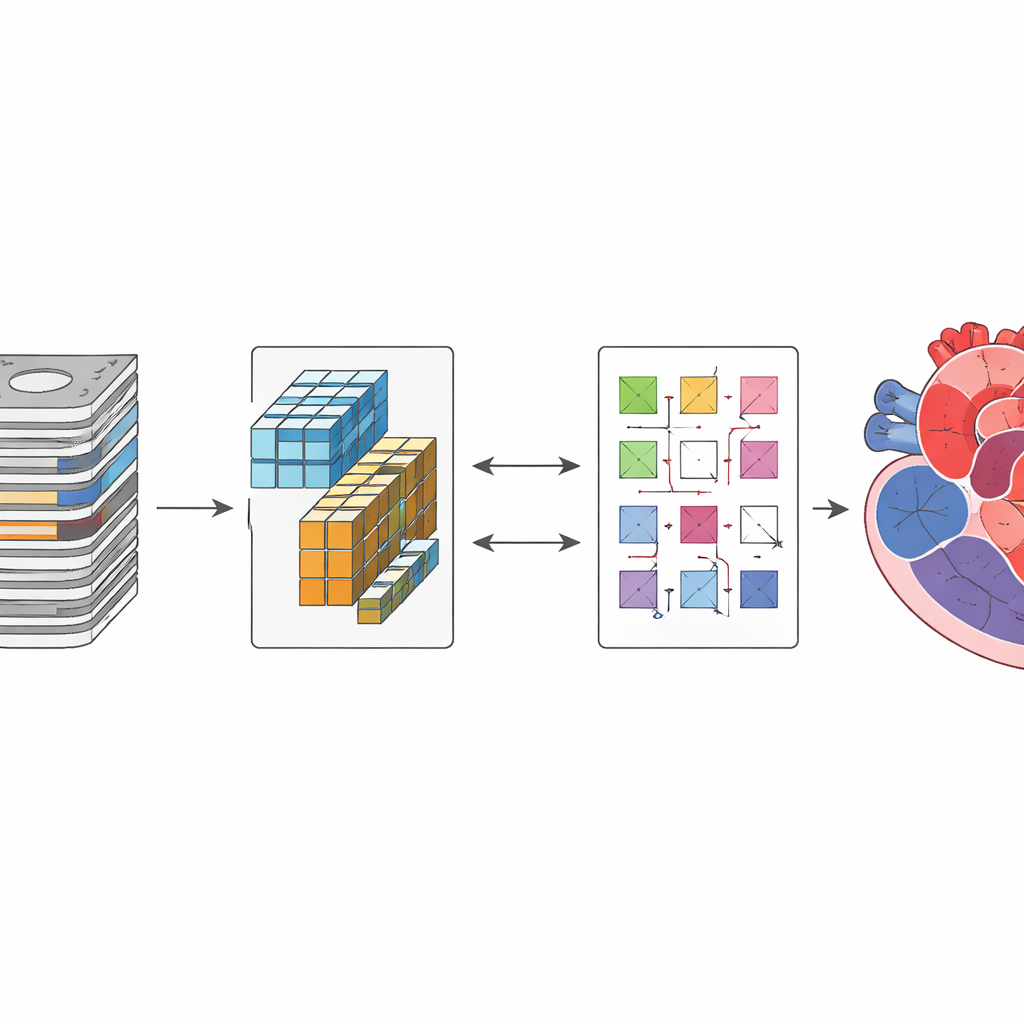
Apprendre aux ordinateurs avec peu d’exemples
Un obstacle majeur dans la construction d’une IA médicale fiable est que l’algorithme a généralement besoin de milliers d’exemples annotés par des experts, et chaque examen cardiaque peut demander des heures d’annotation. Pourtant, les hôpitaux disposent déjà de vastes répertoires d’images non annotées. Les chercheurs ont contourné ce problème en utilisant une stratégie d’apprentissage semi-supervisé, où un petit jeu d’images annotées est combiné à un grand nombre d’images non annotées. L’IA apprend d’abord à partir des images annotées de la manière habituelle. Parallèlement, elle est incitée à produire des prédictions stables et auto-cohérentes sur les images non annotées, de sorte que même les images sans tracés experts contribuent à affiner le modèle. Cette approche réduit la dépendance au travail manuel coûteux tout en orientant le système vers des résultats anatomiquement plausibles.
Deux « points de vue » d’IA différents qui coopèrent
Le cadre, nommé SemiCoTr, associe deux types complémentaires de réseaux d’analyse d’images. L’un, fondé sur des réseaux convolutionnels traditionnels, excelle à repérer des détails locaux fins. L’autre, construit sur la technologie plus récente des transformers, est performant pour appréhender les relations à longue portée sur l’ensemble de l’image. Dans SemiCoTr, les deux réseaux analysent les mêmes images et échangent des informations. Chaque réseau conserve une version « enseignant » mise à jour lentement dont les prédictions servent de référence stable pour la version « étudiant » en évolution rapide, imposant ainsi une cohérence temporelle. De plus, les deux réseaux se supervisent mutuellement : lorsqu’un réseau est confiant sur la présence d’une structure sur une image non annotée, sa prédiction aide à entraîner l’autre. Cette guidance mutuelle, tant au niveau des données qu’au niveau des réseaux, conduit à des contours cardiaques plus robustes et anatomiquement cohérents.
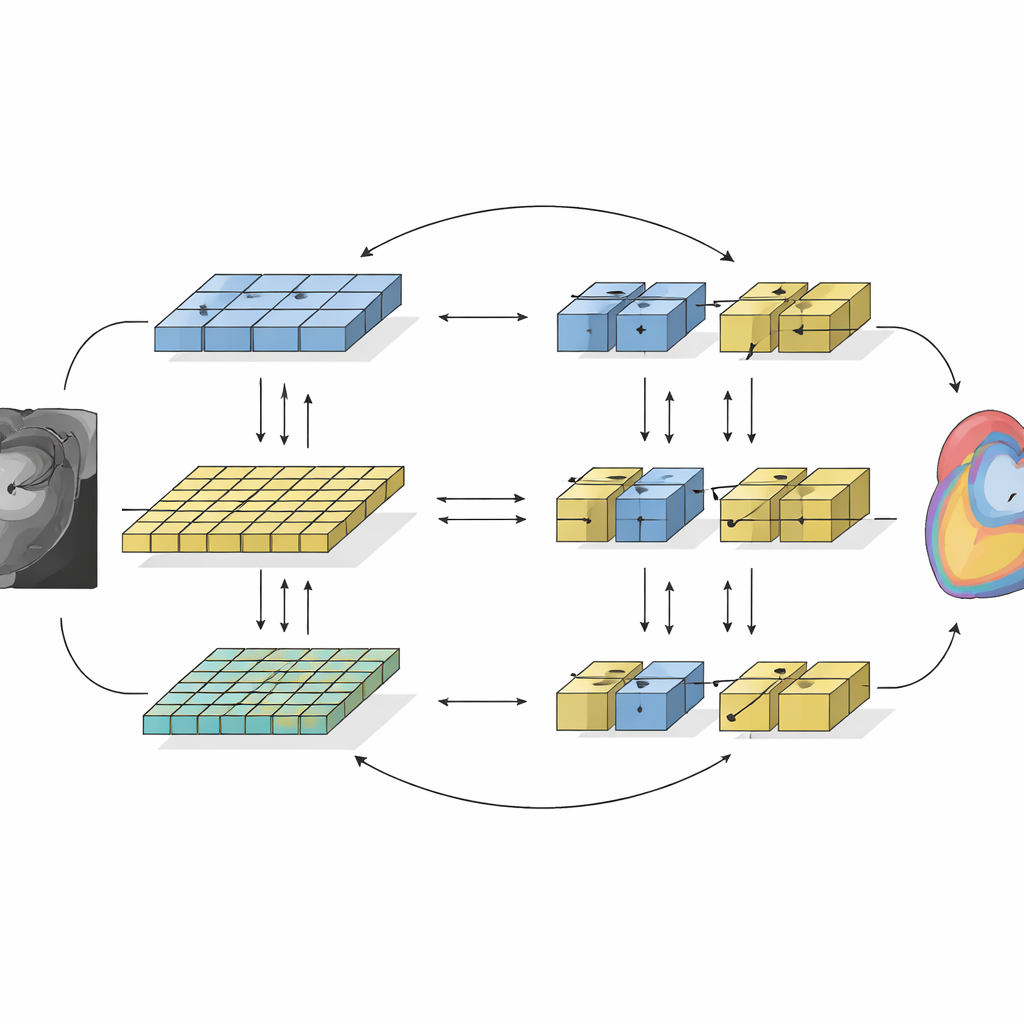
Quel est le niveau de performance réel ?
L’équipe a testé sa méthode sur un jeu de données public d’IRM cardiaques comprenant 100 patients, largement utilisé dans la communauté de recherche. Ils ont simulé un scénario réaliste où seulement 5–10 % des examens étaient annotés par des experts et ont traité le reste comme non annoté. À mesure que davantage de données non annotées étaient ajoutées, la précision des segmentations automatiques augmentait régulièrement, se rapprochant des performances de modèles entraînés sur des jeux entièrement annotés. Comparée à plusieurs techniques semi-supervisées de pointe, leur approche atteignait systématiquement une plus grande précision et des limites plus nettes pour les trois structures cardiaques clés, tout en restant raisonnable en termes de coût de calcul pour l’entraînement. Des expérimentations soignées ont montré que les gains provenaient à la fois de la conception de la perte multi-composante et de la combinaison des deux types de réseaux.
Qu’est-ce que cela signifie pour les patients et les cliniques
L’étude montre qu’il est possible d’obtenir des mesures cardiaques de haute qualité à partir d’IRM avec beaucoup moins d’annotations manuelles qu’on ne le pensait auparavant. En tirant meilleur parti des images non annotées que les hôpitaux génèrent quotidiennement, SemiCoTr ouvre la voie à des outils d’IA évolutifs capables de fournir des évaluations cardiaques précises et reproductibles dans des environnements cliniques chargés. À long terme, de tels systèmes pourraient aider les médecins à détecter plus tôt des troubles cardiaques subtils, à adapter les traitements plus finement aux patients et à suivre l’évolution des maladies avec plus de fiabilité—le tout sans alourdir la charge de travail des spécialistes en imagerie déjà sollicités.
Citation: Guo, S., Zhao, X., Ren, J. et al. Efficient cardiac MRI multi-structure segmentation for cardiovascular assessment with limited annotation by integrating data-level and network-level consistency. npj Digit. Med. 9, 328 (2026). https://doi.org/10.1038/s41746-026-02475-y
Mots-clés: IRM cardiaque, segmentation d'images médicales, apprentissage semi-supervisé, apprentissage profond, imagerie cardiovasculaire