Clear Sky Science · fr
Exploration de l'activité insecticide et étude SAR de nouveaux hétérocycles à base de Benzo[h]quinoline synthétisés contre Aphis craccivora Koch. et les larves de Culex pipiens L.
Pourquoi de nouveaux insecticides sont importants
Les agriculteurs et les agents de santé publique comptent sur les insecticides pour protéger les cultures et empêcher les moustiques de transmettre des maladies. Mais de nombreux ravageurs ont développé une résistance aux produits chimiques couramment utilisés, nous obligeant à traiter plus souvent et à des doses plus élevées. Cela augmente les coûts, nuit aux organismes utiles et risque de contaminer l’environnement. Cette étude explore une nouvelle famille de molécules synthétiques conçues pour tuer à la fois un ravageur agricole nuisible, le puceron du niébé, et le moustique commun à l’état larvaire, dans le but d’identifier des candidats puissants contre les ravageurs tout en convenant à des programmes de lutte plus sélectifs et modernes.
Construire de nouvelles molécules sur une base robuste
L’équipe de recherche est partie d’un squelette chimique rigide et cyclique appelé benzo[h]quinoline. Cette structure est connue pour bien interagir avec des cibles biologiques et apparaît déjà dans certains médicaments et agents de protection des cultures. Les scientifiques l’ont utilisée comme « ancrage » et ont fixé différents petits systèmes cycliques à une extrémité, produisant une série de composés apparentés. Ces pièces additionnelles comprenaient plusieurs blocs de construction bien connus en chimie médicinale, tels que les pyrazolones, les imidazolonés, les thiazolidinones, les pyrimidinones et les indolinones. En ne changeant que cette portion attachée tout en conservant le cœur constant, ils ont pu poser une question simple : quelles formes ajoutées améliorent la capacité de la molécule de base à tuer les insectes ?
Soumettre les nouveaux composés à l’épreuve
L’équipe a évalué le pouvoir insecticide de chaque composé en laboratoire contre deux espèces aux rôles très différents. Les pucerons du niébé attaquent les fèves, sucent la sève et propagent des virus qui freinent ou détruisent les cultures. Les moustiques Culex pipiens sont des vecteurs notoires de virus et de parasites affectant les humains, les oiseaux et d’autres animaux. Dans les tests, les pucerons adultes ont été exposés via des disques de feuilles traités, tandis que les larves de moustiques ont été mises à nager dans de l’eau contenant des concentrations connues de chaque composé. En mesurant le nombre d’insectes morts à chaque dose, les chercheurs ont estimé des valeurs LC50 — la concentration nécessaire pour tuer la moitié des individus testés — et les ont comparées à des insecticides commerciaux de référence.
Ce qui a le mieux fonctionné et ce qui a été décevant
Deux membres de la nouvelle famille se sont distingués. Les composés portant des systèmes cycliques riches en soufre appelés 2‑thioxoimidazolidine et 2‑thioxothiazolidine ont montré une très forte activité contre les deux ravageurs, avec des doses requises similaires, voire inférieures, à celles des produits de référence leaders. Les molécules portant un cycle pyrazolone substitué par un phényle ont également bien performé, bien que de façon un peu moins marquée. En revanche, des conceptions plus volumineuses, telles que celles comportant un cycle pyrimidine fortement substitué ou un fragment indolinone, se sont révélées beaucoup plus faibles, malgré la présence de groupes chimiques souvent efficaces dans d’autres insecticides. De manière générale, les nouveaux composés étaient plus puissants sur les larves de moustiques que sur les pucerons adultes, ce qui suggère que la cuticule et les tissus internes des larves sont particulièrement vulnérables à cette famille chimique.
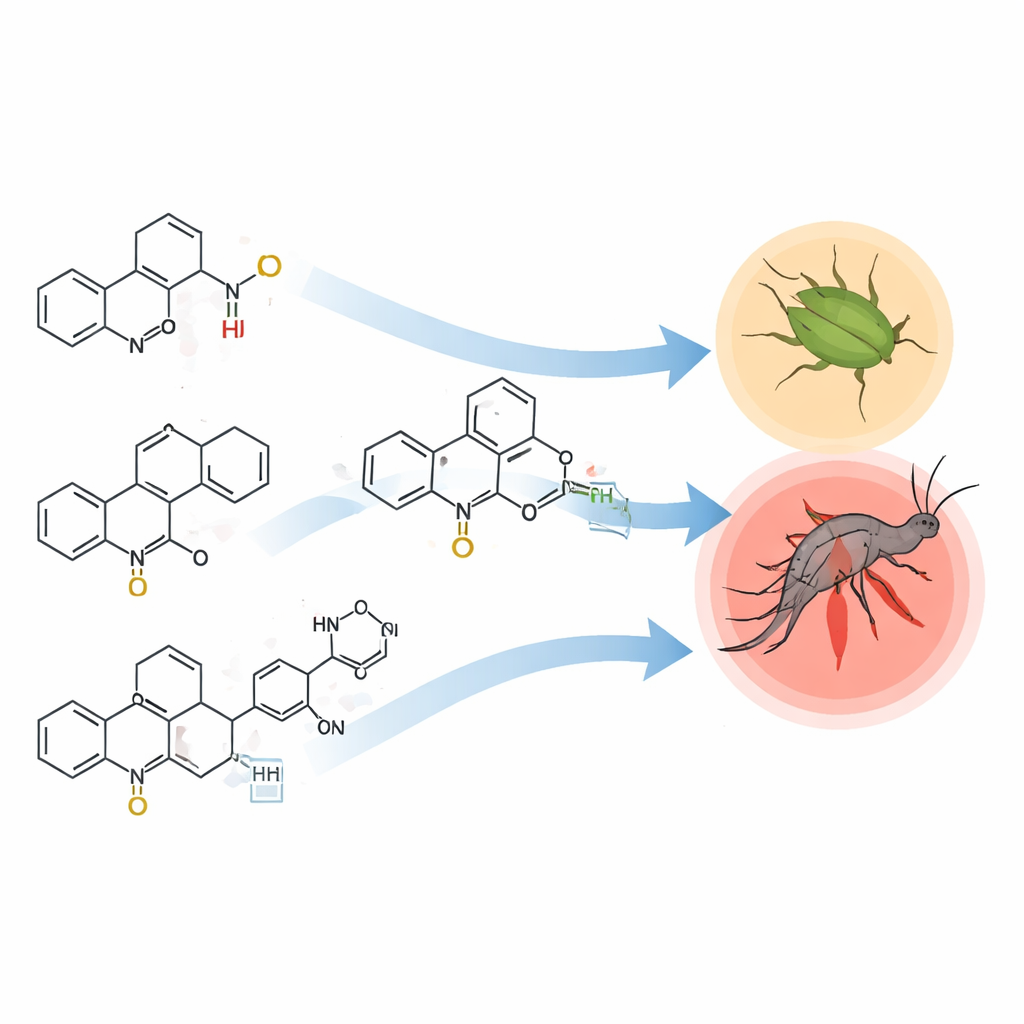
Comment la forme et la composition contrôlent l’efficacité
Parce que toutes les molécules partageaient le même noyau benzo[h]quinoline, l’équipe a pu voir clairement comment de petits changements structuraux affectaient les performances. Les atomes de soufre dans les cycles additionnels semblaient accroître l’activité, probablement en rendant les molécules plus lipophiles et plus aptes à traverser les barrières des insectes, ou en renforçant leur interaction avec des protéines clés. L’ajout d’un anneau phényle plat à des positions spécifiques a également aidé, vraisemblablement en améliorant la manière dont la molécule s’insère dans sa cible biologique. En revanche, des groupes additionnels très volumineux ou rigides semblaient empêcher un contact rapproché avec ces cibles ou ralentir la diffusion dans les tissus des insectes. Ces tendances forment une relation structure‑activité, une sorte de manuel de conception qui relie la forme moléculaire à la puissance insecticide.
Ce que cela signifie pour la lutte antiparasitaire future
Pour un non‑spécialiste, le message principal est que l’équipe a identifié un nouveau échafaudage chimique prometteur pour les insecticides de nouvelle génération, accompagné d’indices clairs sur la façon de l’ajuster. Des substituants compacts contenant du soufre sur le noyau benzo[h]quinoline ont donné les effets les plus marqués, en particulier contre les larves de moustiques, tandis que des groupes latéraux surdimensionnés ont affaibli l’activité. Ces informations peuvent orienter les chimistes vers des candidats encore plus sélectifs et puissants, et aider à éviter des conceptions peu susceptibles de fonctionner. Avant que l’une de ces molécules puisse être utilisée sur le terrain ou dans des programmes de lutte anti‑moustiques, des tests approfondis de sécurité pour les humains, la faune et l’environnement au sens large seraient nécessaires. Néanmoins, cette étude représente une étape importante pour élargir la boîte à outils destinée à contrôler des ravageurs résistants de façon plus ciblée et mieux informée.
Citation: El-Helw, E.A.E., Abdel-Haleem, D.R., Khalil, A.K. et al. Exploring insecticidal activity and SAR study of newly synthesized Benzo[h]quinoline-based heterocycles against Aphis craccivora Koch. and Culex pipiens L. Larvae. Sci Rep 16, 13401 (2026). https://doi.org/10.1038/s41598-026-48683-0
Mots-clés: insecticides, lutte antivectorielle, ravageurs pucerons, chimie hétérocyclique, résistance aux pesticides