Clear Sky Science · de
Untersuchung der insektiziden Aktivität und SAR‑Studie neu synthetisierter Benzo[h]chinolin‑basierter Heterocyclen gegen Aphis craccivora Koch. und Culex pipiens L.‑Larven
Warum neue Schädlingsbekämpfer wichtig sind
Landwirtinnen, Landwirte und Fachleute im Gesundheitswesen verlassen sich auf Insektizide, um Nutzpflanzen zu schützen und zu verhindern, dass Mücken Krankheiten verbreiten. Viele Schädlinge haben jedoch Resistenzen gegen weit verbreitete Wirkstoffe entwickelt, was zu häufigeren und höher dosierten Einsätzen zwingt. Das treibt die Kosten in die Höhe, schadet nützlichen Organismen und erhöht das Risiko von Umweltkontamination. Diese Studie untersucht eine neue Familie synthetischer Moleküle, die sowohl einen bedeutenden Kulturpflanzenschädling, die Vicia‑Blattlaus (cowpea aphid), als auch die gewöhnliche Hausmücke in ihrem Larvenstadium töten sollen, mit dem Ziel, Kandidaten zu finden, die wirksam gegen Schädlinge, aber besser geeignet für moderne, selektivere Bekämpfungsprogramme sind.
Neue Moleküle auf einem stabilen Grundgerüst
Das Forscherteam begann mit einem starren, ringförmigen chemischen Rückgrat, dem Benzo[h]chinolin. Diese Struktur ist dafür bekannt, gut mit biologischen Zielstrukturen zu interagieren und kommt bereits in einigen Arzneimitteln und Pflanzenschutzmitteln vor. Die Wissenschaftler nutzten sie als „Haken“ und setzten an einem Ende verschiedene kleine Ringsysteme an, wodurch eine Reihe verwandter Verbindungen entstand. Zu diesen Anbauteilen gehörten mehrere bekannte Bausteine aus der Arzneimittelchemie, wie Pyrazolone, Imidazolone, Thiazolidinone, Pyrimidinone und Indolinone. Indem sie nur diesen angehängten Teil veränderten und den Kern konstant hielten, konnten sie eine einfache Frage stellen: Welche angehängten Formen machen das Basismolekül besser im Töten von Insekten?
Erprobung der neuen Verbindungen
Das Team bewertete im Labor die insektizide Wirksamkeit jeder Verbindung gegen zwei Arten mit sehr unterschiedlichen ökologischen Rollen. Vicia‑Blattläuse befallen Ackerbohnen, entziehen der Pflanze Saft und übertragen Viren, die das Wachstum hemmen oder die Ernte zerstören. Culex pipiens‑Mücken sind berüchtigte Überträger von Viren und Parasiten, die Menschen, Vögel und andere Tiere betreffen. In den Tests wurden adulte Blattläuse über mit Wirkstoff behandelte Blattstücke exponiert, während Mückenlarven in Wasser mit bekannten Konzentrationen der jeweiligen Verbindung schwammen. Durch das Messen der Sterblichkeit bei verschiedenen Dosen schätzten die Forschenden LC50‑Werte — die Konzentration, die nötig ist, um die Hälfte der getesteten Insekten zu töten — und verglichen diese mit gängigen kommerziellen Insektiziden.
Was am besten funktionierte und was nicht
Zwei Vertreter der neuen Familie stachen hervor. Verbindungen mit schwefelreichen Ringsystemen, bezeichnet als 2‑Thioxoimidazolidin und 2‑Thioxothiazolidin, zeigten sehr starke Aktivität gegen beide Schädlinge, mit erforderlichen Dosen, die denen führender Referenzprodukte ähnlich oder sogar niedriger waren. Moleküle mit einem phenylsubstituierten Pyrazolonring schnitten ebenfalls gut ab, wenn auch etwas weniger eindrucksvoll. Dagegen waren voluminösere Designs, wie solche mit stark substituiertem Pyrimidinring oder einem Indolinonfragment, deutlich schwächer, obwohl sie chemische Gruppen trugen, die in anderen Insektiziden oft wirksam sind. Insgesamt waren die neuen Verbindungen bei Mückenlarven wirksamer als bei adulten Blattläusen, was darauf hindeutet, dass die Larvenhaut und innere Gewebe dieser chemischen Familie gegenüber besonders empfindlich sind.
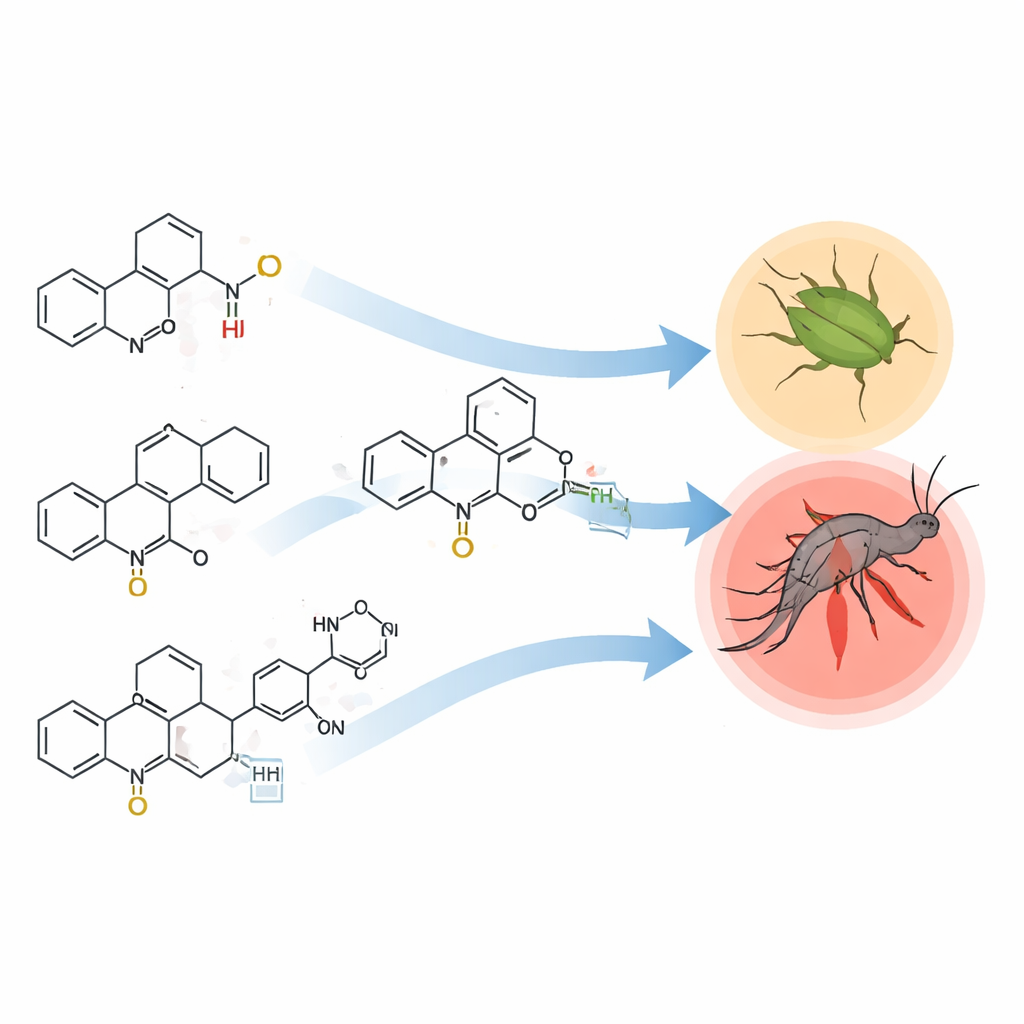
Wie Form und Zusammensetzung die Wirksamkeit steuern
Da alle Moleküle denselben Benzo[h]chinolin‑Kern teilten, konnten die Forschenden klar erkennen, wie kleine strukturelle Änderungen die Leistung beeinflussen. Schwefelatome in den angehängten Ringen schienen die Aktivität zu steigern, wahrscheinlich weil sie die Moleküle lipophiler machen und so das Durchdringen von Insektenbarrieren erleichtern oder die Wechselwirkung mit Schlüsselenzymen und Proteinen verstärken. Das Anfügen eines flachen Phenylrings an bestimmten Positionen half ebenfalls, vermutlich indem es die Anpassung des Moleküls an sein biologisches Ziel verbesserte. Sehr sperrige oder starre Anbauteile hingegen verhinderten offenbar engen Kontakt mit diesen Zielen oder bremsten das Eindringen in Insektentissue. Diese Muster bilden eine Struktur‑Aktivitäts‑Beziehung, eine Art Regelwerk, das Molekülform mit insektizider Stärke verknüpft.
Was das für die zukünftige Schädlingsbekämpfung bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft, dass das Team ein vielversprechendes neues chemisches Gerüst für die nächste Generation von Insektiziden identifiziert hat, zusammen mit klaren Hinweisen, wie man es abstimmen kann. Kompakte, schwefelhaltige Anhänge am Benzo[h]chinolin‑Kern führten zu den stärksten Effekten, besonders gegen Mückenlarven, während übergroße Seitenketten die Aktivität abschwächten. Diese Erkenntnisse können Chemikerinnen und Chemikern helfen, noch selektivere und potentere Kandidaten zu entwickeln und Konstruktionen zu vermeiden, die wahrscheinlich nicht wirken. Bevor irgendeines dieser Moleküle in Feldanwendungen oder Mückenbekämpfungsprogrammen eingesetzt werden kann, sind jedoch umfassende Sicherheitsprüfungen für Menschen, Wildtiere und die Umwelt erforderlich. Dennoch stellt diese Studie einen wichtigen Schritt dar, das Instrumentarium zur Bekämpfung resistenter Schädlinge auf eine fundiertere, gezieltere Weise zu erweitern.
Zitation: El-Helw, E.A.E., Abdel-Haleem, D.R., Khalil, A.K. et al. Exploring insecticidal activity and SAR study of newly synthesized Benzo[h]quinoline-based heterocycles against Aphis craccivora Koch. and Culex pipiens L. Larvae. Sci Rep 16, 13401 (2026). https://doi.org/10.1038/s41598-026-48683-0
Schlüsselwörter: Insektizide, Mückenbekämpfung, Blattlaus‑Schädlinge, heterocyclische Chemie, Pestizidresistenz