Clear Sky Science · fr
Effets comparés du resvératrol intranasal et intrapéritonéal sur l’axe œil–cerveau dans un modèle rat de neurotoxicité induite par le cisplatine
Protéger le cerveau et les yeux pendant un traitement contre le cancer
Des médicaments anticancéreux comme le cisplatine sauvent des vies, mais ils peuvent laisser des survivants avec des troubles nerveux et visuels durables. Cette étude pose une question pratique à portée réelle : un composé naturel que l’on trouve dans le raisin, le resvératrol, peut-il aider à protéger à la fois le cerveau et l’œil des effets toxiques du cisplatine — et le mode d’administration, par voie nasale ou par injection intrapéritonéale, fait-il une différence ?
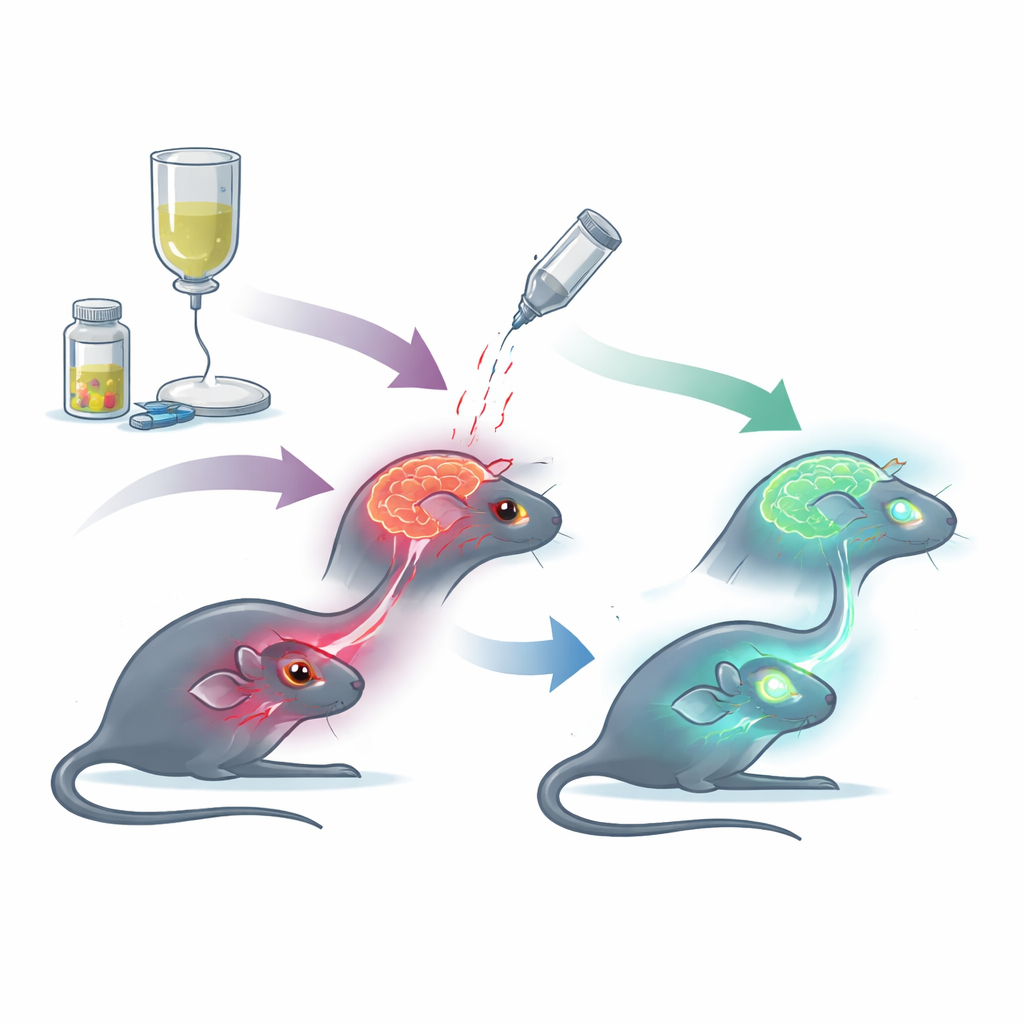
Pourquoi l’œil raconte une histoire cérébrale
La rétine, au fond de l’œil, est essentiellement une avant-poste du cerveau. Elle se développe à partir du même tissu, partage des vaisseaux sanguins et des barrières protectrices similaires, et peut être imagée de façon non invasive. Les lésions observées dans la rétine reflètent souvent ce qui se passe plus profondément dans le cerveau. Le cisplatine, un agent chimiothérapeutique largement utilisé, est connu pour endommager les neurones, perturber les barrières hémato-encéphalique et blesser les tissus rétiniens et cornéens, entraînant parfois des troubles visuels. En raison de ces liens étroits, les auteurs ont focalisé leur attention sur « l’axe œil–cerveau » comme système unifié pour suivre la neurotoxicité induite par le cisplatine et tester des stratégies de protection possibles.
Un aide dérivé du raisin et deux voies d’administration
Le resvératrol est un composé d’origine végétale surtout connu dans le raisin et le vin. Il a été étudié pour ses propriétés antioxydantes, anti-inflammatoires et cytoprotectrices. Cependant, pris par voie orale, il est rapidement dégradé, si bien qu’une fraction minime atteint le cerveau. Les chercheurs ont donc comparé deux façons alternatives d’administrer le resvératrol à des rats traités par cisplatine : intrapéritonéale (injection dans la cavité abdominale, une voie systémique standard) et intranasale (gouttes dans le nez, visant à emprunter des voies nerveuses vers le cerveau tout en contournant le foie et certaines barrières). Des femelles rats ont été réparties en quatre groupes : témoins sains, cisplatine seul, cisplatine plus resvératrol intranasal, et cisplatine plus resvératrol intrapéritonéal.
Ce qui s’est passé dans le cerveau et l’œil
Le cisplatine seul a déclenché une cascade de dommages. Dans les tissus cérébraux et oculaires, les marqueurs d’attaque oxydative des lipides ont augmenté, et l’enzyme protectrice catalase a diminué, indiquant un fort stress oxydatif. Dans l’œil, un marqueur de lésion de l’ADN appelé 8-OHdG a fortement augmenté, et les cellules sanguines ont présenté davantage de cassures d’ADN. Dans le cerveau, l’activité enzymatique liée à la neurotransmission (acétylcholinestérase) était anormalement élevée, signalant une perturbation de la communication chimique. Au niveau génétique, le cisplatine a réduit l’expression d’IL-10, un signal anti-inflammatoire apaisant, tout en augmentant nettement l’expression de la caspase-8, un moteur de la mort cellulaire programmée. Les niveaux circulants de Nrf2, un régulateur majeur des défenses antioxydantes, ont également chuté. À l’examen microscopique, des régions cérébrales et des structures oculaires présentaient des lésions structurelles évidentes, incluant des neurones en dégénérescence et des couches rétiniennes endommagées.
Comment le resvératrol a atténué l’impact
Tant le resvératrol intranasal qu’intrapéritonéal ont atténué bon nombre de ces changements nocifs. Le stress oxydatif dans le cerveau et l’œil a diminué, avec une réduction de la peroxydation lipidique et une activité catalase plus élevée. Les lésions de l’ADN dans l’œil et les cellules sanguines ont été réduites, et les niveaux de Nrf2 ont augmenté, cohérent avec une réponse antioxydante interne renforcée. Dans le cerveau, le resvératrol a déplacé l’équilibre loin de la mort cellulaire et de l’inflammation : l’expression d’IL-10 a augmenté bien au-delà des niveaux observés avec le cisplatine seul, tandis que l’expression de la caspase-8 a diminué. L’activité de l’acétylcholinestérase est revenue vers la normale, suggérant une préservation améliorée de la signalisation nerveuse. Les coupes tissulaires des animaux traités montraient des lésions structurelles plus légères dans le cerveau et l’œil, avec davantage de neurones intacts et des altérations rétiniennes et cornéennes moins sévères. Dans l’ensemble, le resvératrol intrapéritonéal a offert la protection combinée la plus forte, en particulier pour les dommages à l’ADN, l’inflammation et l’apoptose, mais l’administration intranasale a obtenu des effets antioxydants et neuroprotecteurs globalement comparables.
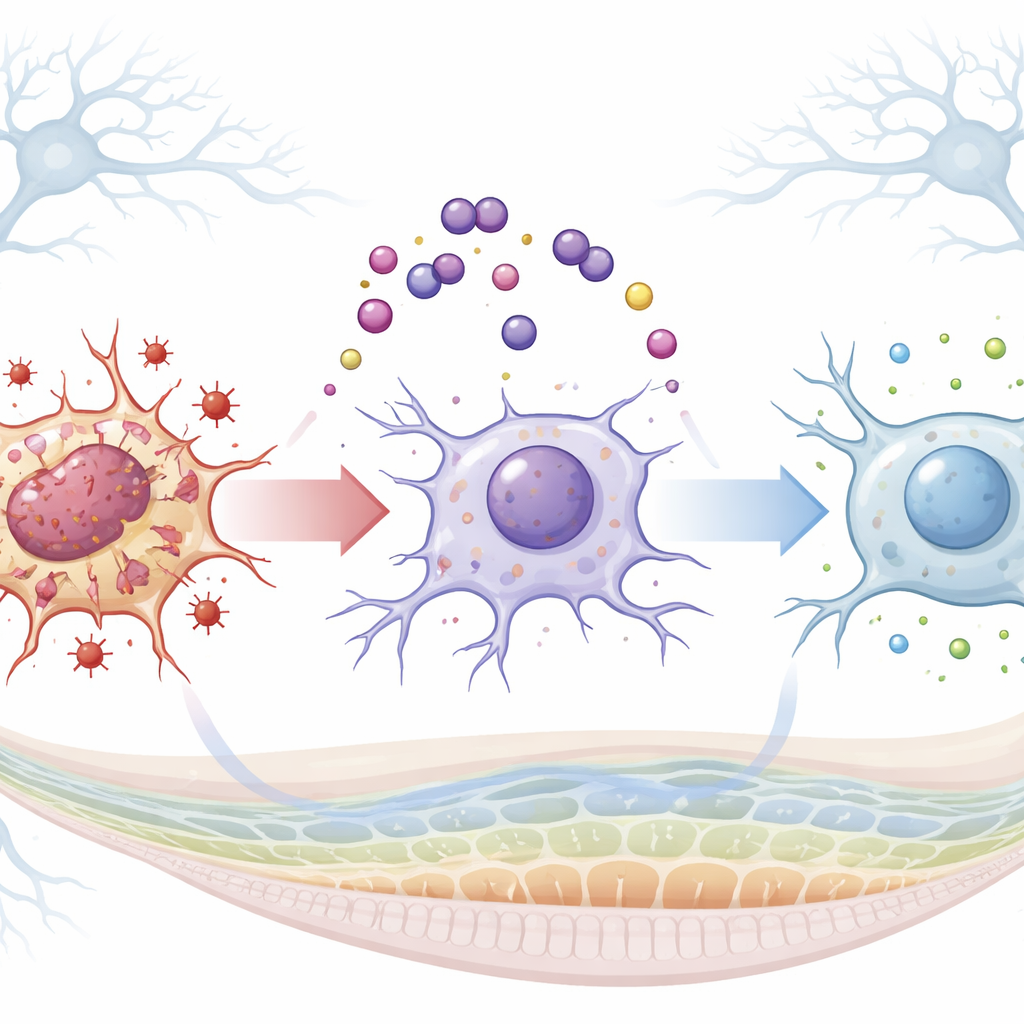
Ce que cela pourrait signifier pour les patients
Cette étude animale suggère que le resvératrol peut réduire de manière significative les dommages collatéraux du cisplatine au cerveau et aux yeux en limitant le stress oxydatif, en calmant l’inflammation et en freinant la mort cellulaire. Bien que l’injection dans la cavité abdominale ait produit la protection la plus robuste au total, l’administration intranasale — non invasive et potentiellement plus confortable — a quand même offert des bénéfices notables et pourrait mieux refléter la façon dont une voie nez‑vers‑cerveau serait utilisable chez l’humain. Ce travail ne se traduit pas encore directement en pratique clinique, mais il met en lumière une stratégie prometteuse : associer des agents protecteurs soigneusement choisis à des traitements anticancéreux puissants, administrés de façon intelligente, pour préserver le système nerveux tout en maintenant l’efficacité antitumorale.
Citation: Ibrahim Fouad, G., Aly, H.F., Mabrouk, M.I. et al. Comparative effects of intranasal and intraperitoneal resveratrol on the eye–brain axis in a cisplatin-induced neurotoxic rat model. Sci Rep 16, 13780 (2026). https://doi.org/10.1038/s41598-026-48629-6
Mots-clés: neurotoxicité par le cisplatine, resvératrol, axe œil–cerveau, administration intranasale de médicaments, stress oxydatif