Clear Sky Science · fr
Exosomes dérivés de cellules souches mésenchymateuses et fibrine riche en plaquettes injectable améliorent la cicatrisation du SDFT dans un modèle de tendinite chez l’âne
Pourquoi la guérison des tendons déchirés est importante
Les lésions tendineuses sont une cause majeure d’interruption de l’entraînement et de retraite précoce chez les chevaux de course et les équidés de travail, et des problèmes similaires touchent les sportifs humains. Une fois endommagés, les tendons cicatrisent souvent par du tissu fibreux rigide plutôt que de retrouver leur élasticité d’origine, ce qui favorise la récidive. Cette étude explore une nouvelle approche pour aider les tendons blessés chez l’âne à cicatriser davantage comme un tissu sain, en utilisant deux produits naturels dérivés du sang et des cellules qui pourraient un jour bénéficier aux chevaux et peut‑être même aux humains.
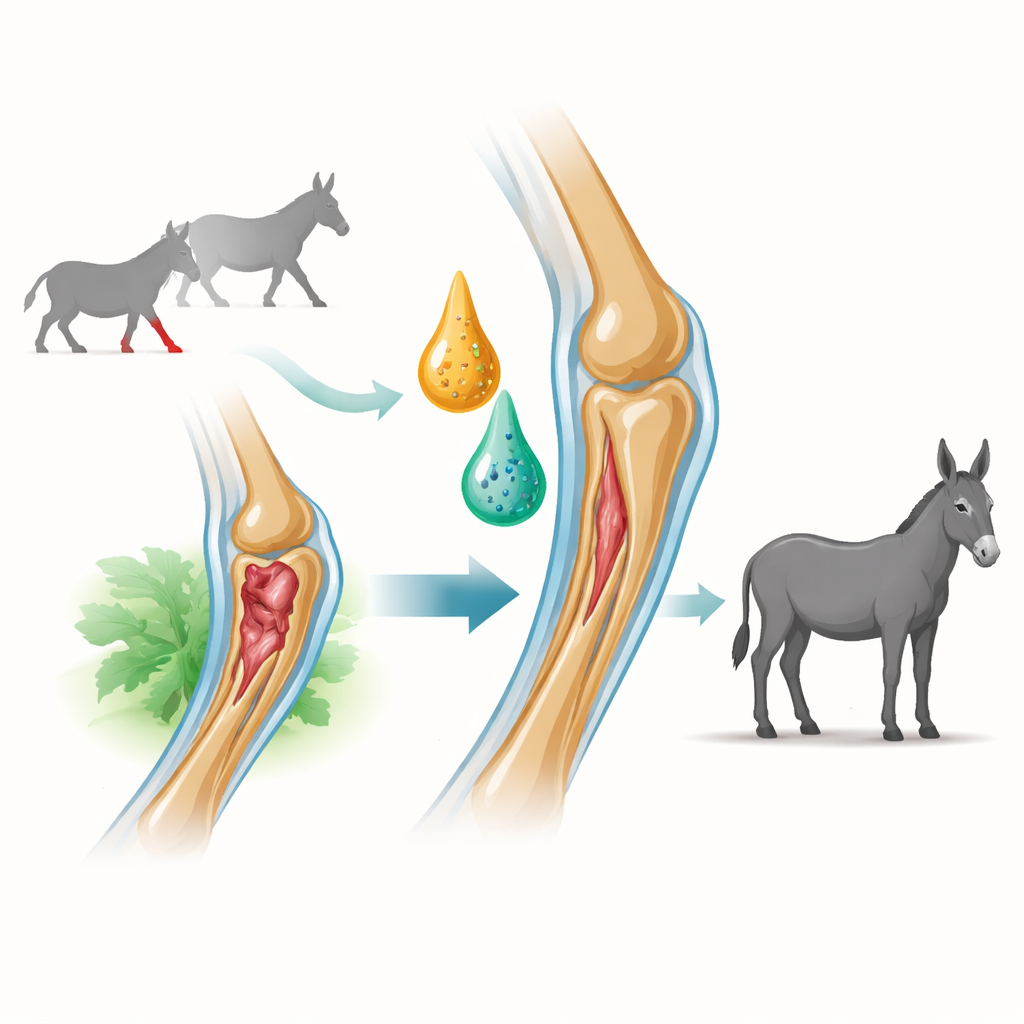
Un regard approfondi sur les blessures de la jambe chez l’âne
La recherche s’est concentrée sur le tendon fléchisseur digital superficiel, une structure cordiforme qui aide à soutenir le poids du corps et à stocker de l’énergie lors du mouvement. Chez les chevaux de sport, ce tendon est un site fréquent de surmenage. Pour reproduire ce problème de manière contrôlée, les chercheurs ont créé de petites lésions standardisées dans les tendons des antérieurs des ânes en utilisant une enzyme qui fragilise le tissu. Ce modèle reproduit la douleur, le gonflement et les dommages microscopiques observés dans la tendinite en conditions réelles, tout en permettant de tester soigneusement, côte à côte, de nouveaux traitements.
Deux aides naturelles pour la réparation
L’équipe a testé une forme injectable de fibrine riche en plaquettes (I‑PRF) et de petits paquets libérés par les cellules souches, appelés exosomes. L’I‑PRF est fabriquée à partir du sang de l’animal et contient des plaquettes emprisonnées dans un réseau fibrineux mou qui libère lentement des facteurs de croissance pendant environ deux semaines. Les exosomes ont été préparés à partir de cellules souches issues de la moelle osseuse ; ces vésicules nanométriques transportent des molécules de signalisation capables d’apaiser l’inflammation et d’orienter les cellules locales vers la reconstruction du tissu. Les ânes ont été assignés au hasard pour recevoir du sérum physiologique (placebo), de l’I‑PRF seul, ou un mélange d’I‑PRF et d’exosomes injecté directement dans le tendon lésé une semaine après la lésion.
Suivi de la guérison de la surface à la résistance
Sur 20 semaines, les chercheurs ont suivi la récupération à l’aide de plusieurs méthodes complémentaires. Les cliniciens ont noté l’alégement, la douleur et la façon dont chaque animal portait le poids sur le membre lésé. Les échographies ont mesuré la taille du noyau lésé, la réflectivité du tendon et l’alignement des fibres internes. À des moments prédéfinis, certains tendons ont été examinés au microscope pour évaluer l’organisation des fibres, la néovascularisation et les types de collagène présents. Enfin, à la fin de l’étude, des bandes de tendon ont été étirées jusqu’à rupture pour mesurer la force et l’allongement qu’elles pouvaient supporter par rapport au tissu normal.
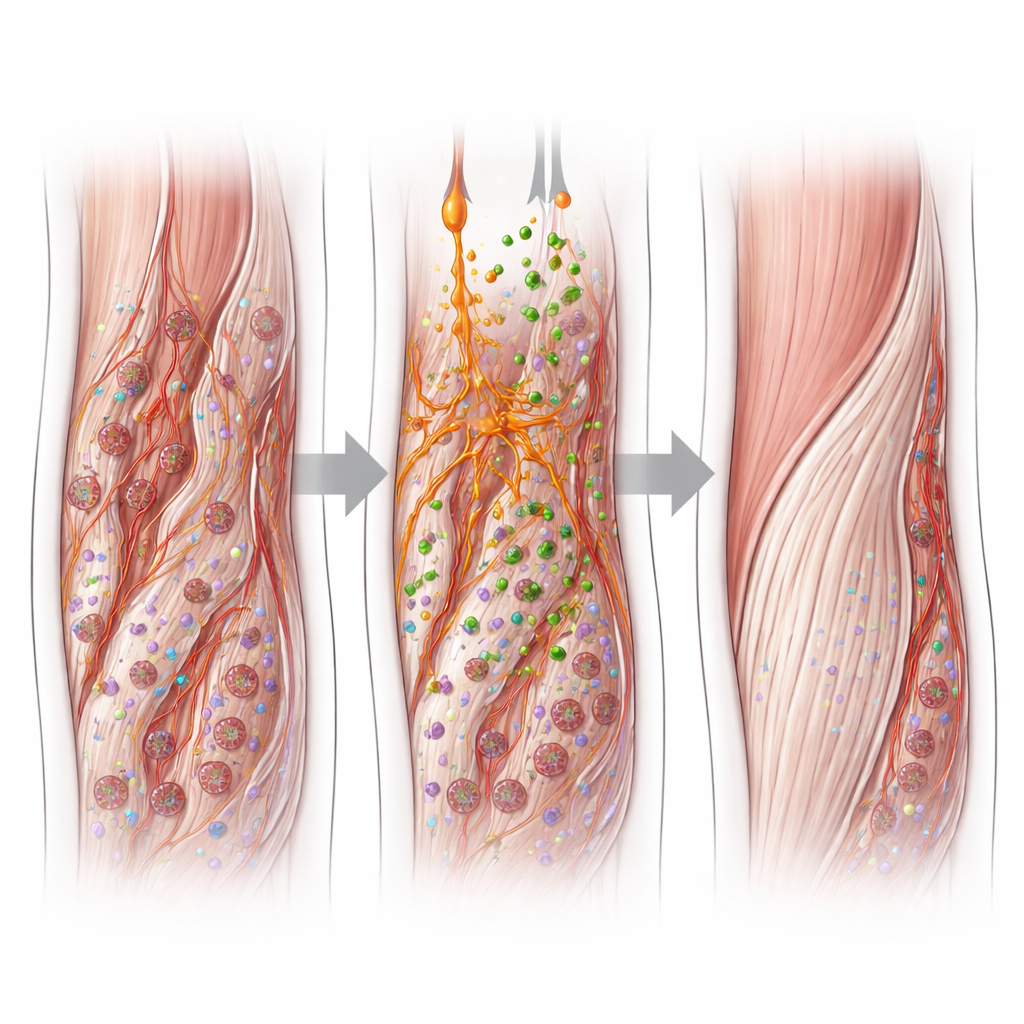
Ce que les traitements ont modifié à l’intérieur du tendon
Tous les groupes se sont améliorés au fil du temps, mais le modèle et la qualité de la cicatrisation différaient. Les tendons traités par la combinaison I‑PRF et exosomes ont montré la réduction la plus rapide de la taille de la lésion centrale à l’échographie et un retour plus précoce vers un aspect plus uniforme et quasi normal. Au microscope, ces tendons présentaient des fibres mieux alignées, moins de vaisseaux sanguins anormaux et une densité cellulaire plus équilibrée. Surtout, ils contenaient davantage de collagène de type I — la forme solide et résistante présente dans les tendons sains — et moins de collagène de type III, associé à un tissu cicatriciel plus faible. L’I‑PRF seul a produit des bénéfices intermédiaires, tandis que le groupe sérum physiologique a eu tendance à développer des zones plus dures et nodulaires avec des fibres désorganisées et une proportion plus élevée de collagène de type cicatriciel.
Des changements microscopiques à la résistance en conditions réelles
Les tests mécaniques ont révélé que, bien qu’aucun des tendons lésés n’atteigne complètement la résistance des tendons non lésés au terme de 20 semaines, ceux traités par I‑PRF plus exosomes ont supporté la plus grande contrainte avant rupture et pouvaient s’allonger davantage avant de se déchirer. Les ânes de ce groupe présentaient également une forme de tendon presque normale à la palpation et un port du poids plus équilibré au repos. Ensemble, ces résultats suggèrent qu’associer un échafaudage plaquettaire à action prolongée à des exosomes dérivés de cellules souches peut orienter la réparation tendineuse loin d’une cicatrisation fragile vers une reconstruction plus fonctionnelle. Les auteurs soulignent qu’il faut des études plus longues sur des blessures naturellement survenues, mais ces travaux ouvrent la voie à une stratégie biologique prometteuse pour aider les tendons à haut risque chez les athlètes équins et possiblement humains à cicatriser plus forts et plus durablement.
Citation: Najeb, M., Samy, A., Rizk, A. et al. Mesenchymal stem cell derived exosomes and injectable platelet-rich fibrin enhance SDFT healing in a donkey tendonitis model. Sci Rep 16, 12013 (2026). https://doi.org/10.1038/s41598-026-44967-7
Mots-clés: guérison des tendons, fibrine riche en plaquettes, exosomes de cellules souches, médecine sportive équine, thérapie régénérative