Clear Sky Science · fr
Un nouveau champignon isolé, Talaromyces sp. MC-F2, solubilise efficacement le phosphate grâce à une régulation métabolique dépendante du milieu
Pourquoi le « nourrissement » végétal enfermé compte
Une grande partie du phosphore présent dans les sols agricoles est piégée dans des minéraux difficilement solubles que les plantes ne peuvent pas utiliser, même après des années d’apport d’engrais. Cela gaspille de l’argent, nuit aux cours d’eau et laisse les cultures sous-alimentées. L’étude décrite ici présente un champignon du sol nouvellement découvert capable de libérer ce phosphore caché et explique, de façon inhabituelle par son niveau de détail, comment le champignon modifie sa chimie interne selon son environnement pour accomplir efficacement cette tâche.
Un nouvel allié venu du sous-sol
Les chercheurs ont prélevé des sols de terres agricoles dans l’est de la Chine et ont recherché des microbes capables de dissoudre les minéraux phosphatés solides. Ils ont isolé un champignon prometteur qu’ils ont nommé Talaromyces sp. MC-F2. Sur boîtes de culture en laboratoire, cette souche formait des halos clairs autour de ses colonies, signe visuel qu’elle dissolvait le phosphate tricalcique présent dans le milieu de culture. L’observation microscopique et l’analyse de l’ADN ont confirmé que l’organisme appartient au genre Talaromyces, un groupe de champignons apparentés à des espèces mieux connues comme Penicillium, mais beaucoup moins étudiés pour leur capacité à rendre les nutriments du sol plus disponibles pour les plantes.
Transformer le phosphore lié à la roche en nourriture prête pour les plantes
Pour évaluer la capacité du nouveau champignon à libérer du phosphore, l’équipe a cultivé MC-F2 dans trois milieux liquides standard : Pikovskaya (PVK), NBRIP et bouillon dextrose-pomme de terre (PDB), chacun contenant des quantités différentes de phosphate tricalcique. Dans toutes les conditions, le champignon a fortement abaissé le pH du liquide et entraîné de grandes quantités de phosphore du minéral solide vers la solution. La performance la plus marquée a été observée en milieu NBRIP, où les concentrations finales de phosphore dissous étaient systématiquement plus élevées que dans les deux autres milieux pour la même charge minérale. Cela montre que le champignon et l’environnement chimique qui l’entoure agissent de concert pour déterminer la quantité de phosphore exploitable par les plantes.
Des outils acides et de nouveaux cristaux
Le champignon accomplit la majeure partie de son travail en sécrétant des acides organiques — de petites molécules acides qui attaquent les surfaces minérales. Les analyses chimiques ont montré que MC-F2 produisait des quantités particulièrement importantes d’acide gluconique et d’acide malique, l’équilibre entre ces deux acides évoluant en fonction de la concentration minérale. Dans un milieu plus riche et contenant davantage de minéral, la production d’acide malique augmentait fortement, tandis que l’acide gluconique avait tendance à diminuer. À mesure que ces acides dissolvaient le phosphate tricalcique, le calcium était libéré et se combinait avec l’oxalate produit par le champignon pour former de nouveaux cristaux d’oxalates de calcium hydratés. Ces minéraux secondaires, confirmés par diffraction des rayons X et microscopie électronique, ont beaucoup moins de tendance à enfermer de nouveau le phosphore, contribuant à le maintenir sous des formes accessibles aux cultures.
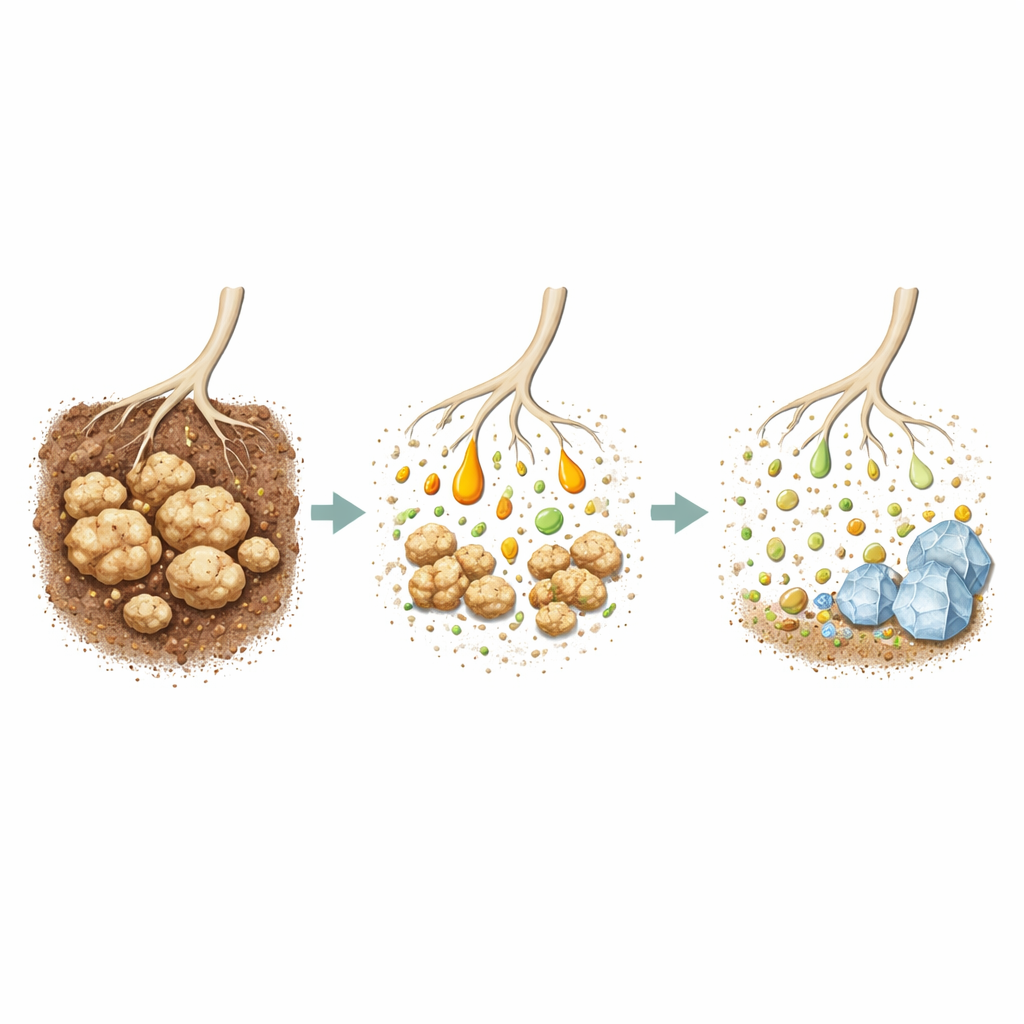
À l’intérieur de l’usine fongique
Pour comprendre comment le champignon ajuste sa chimie selon les milieux et les charges minérales, les chercheurs ont utilisé la métabolomique non ciblée — un inventaire large de centaines de petites molécules à l’intérieur et autour des cellules. Ils ont constaté que la composition nutritive et la quantité de phosphate tricalcique remodelaient fortement les voies métaboliques centrales. En NBRIP, le cycle qui gère une grande partie de l’énergie et du flux de carbone de la cellule (cycle TCA) était particulièrement activé, avec des intermédiaires comme le malate et le citrate en hausse de plusieurs fois. Ces changements concordent avec les pics observés de sécrétion d’acide malique et de libération de phosphore. D’autres voies, notamment celles liées aux acides aminés et au transport des molécules à travers les membranes cellulaires, étaient également régulées à la hausse ou à la baisse selon le niveau de stress minéral subi par le champignon, révélant une stratégie flexible plutôt qu’un mécanisme unique et rigide.
Des flacons de laboratoire aux champs plus verts
Dans l’ensemble, ce travail montre que Talaromyces sp. MC-F2 est un outil naturel puissant pour convertir le phosphore enfermé dans la roche en nutriments disponibles pour les plantes, principalement par la production adaptée d’acides organiques qui modifient à la fois la chimie de la solution et les minéraux eux-mêmes. En cartographiant la façon dont son métabolisme répond à différentes conditions, l’étude ouvre la voie à la conception de milieux, de formulations, ou même de souches améliorées qui maximisent la libération de phosphore. Pour les agriculteurs et les planificateurs environnementaux, ce champignon représente une étape prometteuse vers des biofertilisants capables de réduire la dépendance aux intrants phosphorés synthétiques, d’exploiter le phosphore « héritage » déjà présent dans les sols et de diminuer la pollution, le tout en tirant parti du travail discret mais sophistiqué des microbes du sol.
Citation: Xia, M., Bao, P., He, S. et al. A new isolated fungus Talaromyces sp. MC-F2 efficiently solubilizes phosphate through media-dependent metabolic regulation. Sci Rep 16, 14121 (2026). https://doi.org/10.1038/s41598-026-44554-w
Mots-clés: champignons solubilisant le phosphate, biofertilisant, phosphore du sol, Talaromyces, acides organiques