Clear Sky Science · de
Ein neuer isolierter Pilz Talaromyces sp. MC-F2 löst Phosphat effizient durch medienabhängige Stoffwechselregulation
Warum eingeschlossene Pflanzennahrung wichtig ist
Ein großer Teil des Phosphors im Ackerboden steckt in schwer löslichen Mineralen, die Pflanzen nicht nutzen können, selbst nach jahrelanger Düngung. Das verschwendet Geld, schadet Gewässern und führt zu unterernährten Kulturen. Die hier beschriebene Studie stellt einen neu entdeckten Bodenpilz vor, der diesen verborgenen Phosphor freisetzt, und erklärt ungewöhnlich detailliert, wie der Pilz seine innere Chemie je nach Umgebung so anpasst, dass er die Arbeit effizient verrichtet.
Ein neuer Helfer aus dem Untergrund
Die Forschenden entnahmen Bodenproben von Ackerland in Ostchina und suchten nach Mikroben, die feste Phosphatminerale auflösen können. Sie isolierten einen vielversprechenden Pilz, den sie Talaromyces sp. MC-F2 nannten. Auf Agarplatten bildete dieser Stamm klare Zonen um die Kolonien — ein sichtbares Zeichen dafür, dass er das in Nährmedien enthaltene Tricalciumphosphat auflöste. Mikroskopie und DNA-Analysen bestätigten, dass der Organismus zur Gattung Talaromyces gehört, einer Gruppe von Pilzen, die mit bekannteren Arten wie Penicillium verwandt sind, aber hinsichtlich ihrer Fähigkeit, Bodennährstoffe für Pflanzen verfügbar zu machen, deutlich weniger untersucht wurden.
Gesteinsgebundenen Phosphor in pflanzenverfügbares Futter verwandeln
Um zu prüfen, wie gut der neue Pilz Phosphor freisetzen kann, kultivierte das Team MC-F2 in drei standardmäßigen Flüssigmedien: Pikovskaya (PVK), NBRIP und Potato-Dextrose-Broth (PDB), die jeweils unterschiedliche Mengen an Tricalciumphosphat enthielten. Unter allen Bedingungen senkte der Pilz den pH-Wert der Flüssigkeit stark ab und bewirkte, dass große Mengen Phosphor vom festen Mineral in die Lösung übergingen. Die beste Leistung zeigte sich im NBRIP-Medium, wo die Endkonzentrationen gelösten Phosphors beständig höher lagen als in den beiden anderen Medien bei gleicher Mineralbeladung. Das zeigt, dass sowohl der Pilz als auch die umgebende chemische Matrix gemeinsam bestimmen, wie viel pflanzenverfügbarer Phosphor entsteht.
Saure Werkzeuge und neue Kristalle
Der Pilz arbeitet vorwiegend, indem er organische Säuren sezerniert — kleine, saure Moleküle, die Minerale angreifen. Chemische Analysen zeigten, dass MC-F2 besonders große Mengen an Gluconsäure und Äpfelsäure (Malat) produzierte, wobei das Verhältnis zwischen ihnen sich mit der Mineralstoffkonzentration verschob. In nährstoffreicheren Medien mit höherer Mineralmenge stieg die Produktion von Äpfelsäure stark an, während die Gluconsäure tendenziell abnahm. Beim Auflösen des Tricalciumphosphats wurde Calcium freigesetzt, das sich mit vom Pilz gebildetem Oxalat verband und neue Kristalle von Calciumoxalathydraten bildete. Diese sekundären Minerale, bestätigt durch Röntgenbeugung und Elektronenmikroskopie, binden Phosphor deutlich weniger stark, was dazu beiträgt, ihn in Formen zu halten, die Pflanzen nutzen können.
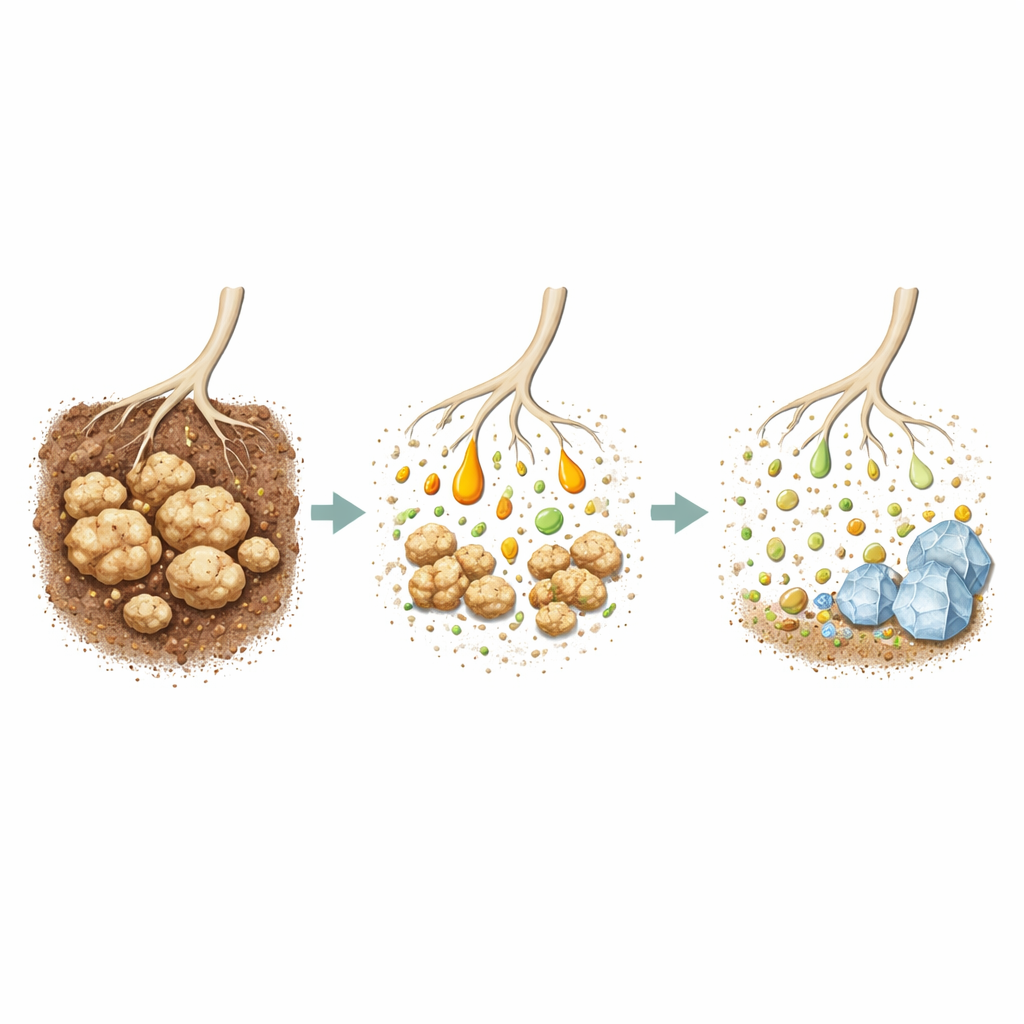
Im Inneren der Pilzfabrik
Um zu verstehen, wie der Pilz seine Chemie an verschiedene Medien und Mineralbelastungen anpasst, nutzten die Forschenden ungerichtete Metabolomik — eine breite Untersuchung von Hunderten kleiner Moleküle innerhalb und um die Zellen. Sie stellten fest, dass die Mischung der Nährstoffe und die Menge an Tricalciumphosphat zentrale Stoffwechselwege stark umgestalteten. Im NBRIP-Medium war der Zyklus, der einen Großteil des Energie- und Kohlenstoffflusses der Zelle steuert (Zitratzyklus/TCA-Zyklus), besonders aktiviert, mit Zwischenprodukten wie Malat und Zitrat, die mehrere Male anstiegen. Diese Veränderungen korrelierten mit den beobachteten Spitzen in der Sekretion von Äpfelsäure und der Freisetzung von Phosphor. Auch andere Wege, einschließlich solcher für Aminosäuren und den Molekültransport über Zellmembranen, wurden je nach ausgebrachter Mineralbelastung hoch- oder herunterreguliert, was eine flexible Strategie statt eines starren Mechanismus offenbarte.
Von Laborkolben zu grüneren Feldern
Insgesamt zeigt die Arbeit, dass Talaromyces sp. MC-F2 ein wirksames natürliches Mittel ist, um gesteinsgebundenen Phosphor in pflanzenverfügbare Nährstoffe umzuwandeln, hauptsächlich durch die gezielte Produktion organischer Säuren, die sowohl die Lösungchemie als auch die Minerale selbst verändern. Indem die Studie aufzeigt, wie sein Stoffwechsel auf unterschiedliche Bedingungen reagiert, weist sie den Weg zu optimierten Medien, Formulierungen oder sogar verbesserten Stämmen, die die Phosphorfreisetzung maximieren. Für Landwirte und Umweltschutzplaner stellt dieser Pilz einen vielversprechenden Schritt hin zu Biodüngern dar, die die Abhängigkeit von synthetischen Phosphorzufuhren verringern, in den Böden bereits vorhandenen „Legacy“-Phosphor nutzbar machen und Verschmutzung reduzieren können — alles durch das stillvolle, aber ausgeklügelte Wirken von Bodenmikroben.
Zitation: Xia, M., Bao, P., He, S. et al. A new isolated fungus Talaromyces sp. MC-F2 efficiently solubilizes phosphate through media-dependent metabolic regulation. Sci Rep 16, 14121 (2026). https://doi.org/10.1038/s41598-026-44554-w
Schlüsselwörter: phosphatlösende Pilze, Biodünger, Phosphor im Boden, Talaromyces, organische Säuren