Clear Sky Science · fr
Expression du récepteur immunitaire CCR7 dans le cancer du sein inflammatoire
Pourquoi cette étude est importante
Le cancer du sein inflammatoire est l’une des formes les plus rares mais aussi les plus agressives du cancer du sein. Il tend à se propager précocement par les petits vaisseaux lymphatiques de la peau, entraînant un gonflement et une rougeur rapides du sein. Cette étude pose une question simple mais essentielle : un interrupteur de « repérage » cellulaire spécifique, appelé CCR7, aide-t-il les cellules du cancer du sein inflammatoire à trouver et envahir ces canaux lymphatiques et les ganglions lymphatiques voisins ? Si oui, cet interrupteur pourrait devenir une nouvelle cible pour des thérapies ciblées à l’avenir.
Un schéma de propagation dangereux
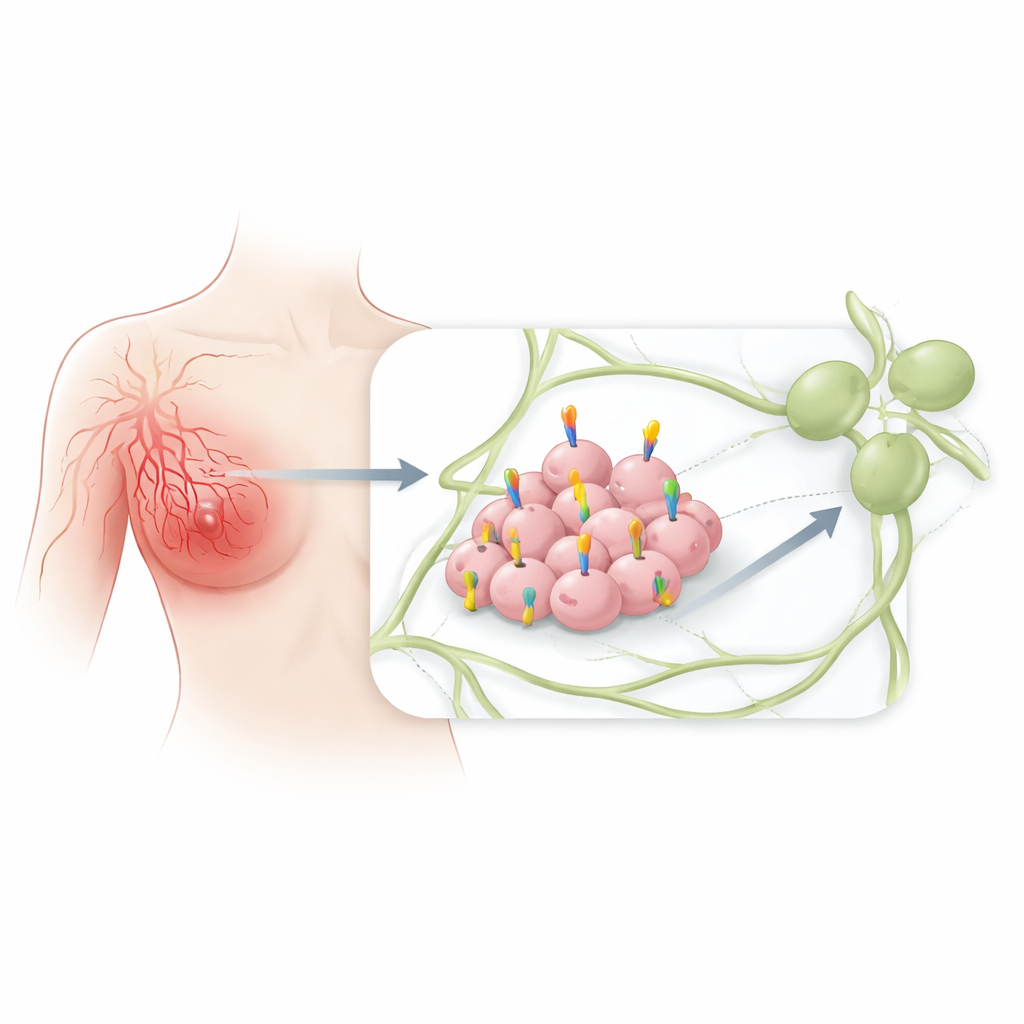
Contrairement aux cancers du sein plus familiers qui forment généralement une masse distincte, le cancer du sein inflammatoire se manifeste souvent par un sein douloureux, enflé et décoloré. Au microscope, les canaux lymphatiques de la peau sont remplis de grappes de cellules tumorales. Parce que ces vaisseaux se raccordent directement aux ganglions lymphatiques et au reste de l’organisme, comprendre ce qui attire les cellules cancéreuses dans ce réseau est crucial pour expliquer pourquoi cette maladie se propage si rapidement et est plus difficile à guérir.
L’interrupteur de « repérage » cellulaire CCR7
CCR7 est un récepteur que l’on trouve normalement sur certaines cellules immunitaires, les aidant à circuler par les vaisseaux lymphatiques jusqu’aux ganglions lymphatiques, où les réponses immunitaires sont coordonnées. Il fonctionne comme une serrure reconnaissant des « clés » chimiques libérées dans les tissus lymphatiques. Des travaux antérieurs sur d’autres cancers ont suggéré que lorsque les cellules tumorales commencent à utiliser ce même système serrure‑clé, elles peuvent migrer plus facilement dans les vaisseaux lymphatiques et ensemencer des sites distants. Cependant, le rôle de CCR7 dans le cancer du sein inflammatoire n’avait pas été cartographié en détail avant cette étude.
Suivre CCR7 dans des modèles et des échantillons de patients
Les chercheurs ont d’abord analysé des modèles expérimentaux. Chez des souris dont le tissu mammaire avait été préparé par un régime riche en graisses et des modifications des schémas d’allaitement — des conditions qui augmentent l’inflammation et l’activité lymphatique — ils ont trouvé des niveaux plus élevés de signaux liés à CCR7 dans la glande mammaire. Ils ont ensuite examiné des lignées cellulaires de cancer du sein en laboratoire et observé que les cellules de cancers inflammatoires et non inflammatoires produisaient la protéine CCR7, suggérant que ce récepteur est largement disponible aux cellules tumorales. Ensuite, en utilisant une grande base de données internationale de profils géniques tumoraux, ils ont comparé 137 cancers du sein inflammatoires avec 252 cas non inflammatoires. L’activité génique de CCR7 était significativement plus élevée dans les tumeurs inflammatoires, tout comme celle de son principal partenaire chimique, CCL21, qui est abondant dans les cellules lymphatiques.
Quelles tumeurs montrent le signal le plus fort
Tous les cancers du sein inflammatoires ne se ressemblent pas. Lorsque l’équipe a regroupé les tumeurs selon des marqueurs cliniques courants, l’activité génique de CCR7 était particulièrement élevée chez celles dépourvues de récepteurs aux œstrogènes et chez celles classées comme HER2‑positives ou de type basal — des sous‑types déjà connus pour avoir des pronostics plus défavorables. CCL21, le principal signal partenaire de CCR7, avait également tendance à être plus élevé dans les tumeurs HER2‑positives. Cependant, lorsque les scientifiques ont étudié les données de survie sur l’ensemble du grand jeu de données, ils n’ont pas trouvé de lien simple entre des niveaux géniques plus élevés de CCR7 ou de CCL21 et la survie globale, suggérant que la manière et l’emplacement d’utilisation de la protéine à la surface cellulaire peuvent importer davantage que le seul niveau d’expression génique.
Voir CCR7 directement dans le tissu tumoral
Pour vérifier ce que cela donne dans de vraies tumeurs, les chercheurs ont coloré des micro‑réseaux tissulaires issus d’échantillons de mastectomie de cancers du sein inflammatoires. Presque tous les échantillons contenant suffisamment de tissu tumoral montraient CCR7 sur les cellules cancéreuses, le plus souvent sous la forme d’un anneau fort et continu le long de la surface cellulaire. De nombreuses tumeurs avaient presque toutes leurs cellules colorées. Cette présence généralisée soutient l’idée que CCR7 fait partie de la trousse d’outils de base des cellules de cancer du sein inflammatoire, même si le petit nombre de patients limitait la possibilité d’associer les motifs de marquage aux résultats cliniques comme la récidive ou la survie.
Ce que cela signifie pour les traitements futurs
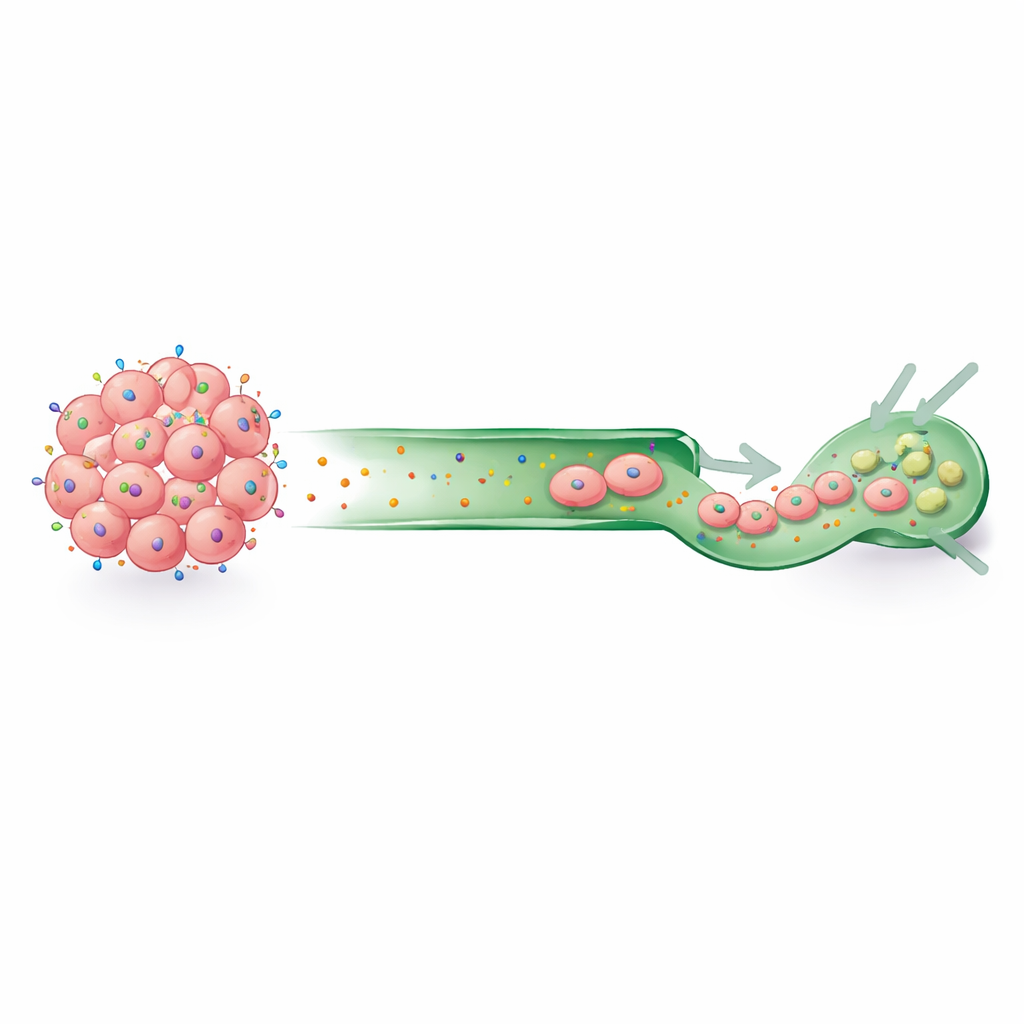
Pris ensemble, les résultats décrivent CCR7 comme à la fois fréquent et particulièrement actif au niveau génique dans le cancer du sein inflammatoire, en particulier dans les sous‑types plus difficiles à traiter. Son partenariat avec CCL21 et son rôle connu dans le repérage vers les vaisseaux lymphatiques suggèrent qu’il peut aider les cellules cancéreuses à envahir et à circuler par les canaux lymphatiques. L’étude met en avant CCR7 comme un candidat prometteur pour des thérapies ciblées, telles que des conjugués anticorps‑médicament qui délivreraient des charges toxiques directement aux cellules exprimant CCR7. Bien que des travaux supplémentaires soient nécessaires sur des cohortes plus larges pour confirmer comment CCR7 influence la dissémination et les résultats, cette recherche jette les bases pour transformer un moteur clé de l’invasion lymphatique en une vulnérabilité thérapeutique potentielle.
Citation: Chen, J.H., Balema, W., Krishnamurthy, S. et al. CCR7 immune cell receptor expression in inflammatory breast cancer. Sci Rep 16, 13513 (2026). https://doi.org/10.1038/s41598-026-43437-4
Mots-clés: cancer du sein inflammatoire, CCR7, propagation lymphatique, cancer du sein HER2-positif, thérapie ciblée