Clear Sky Science · de
CCR7-Expression von Immunzellenrezeptoren beim inflammatorischen Mammakarzinom
Warum diese Studie wichtig ist
Das inflammatorische Mammakarzinom gehört zu den seltensten, aber zugleich aggressivsten Formen von Brustkrebs. Es neigt dazu, früh über die feinen Lymphgefäße der Haut zu streuen, was zu rascher Schwellung und Rötung der Brust führt. Diese Studie stellt eine einfache, aber bedeutsame Frage: Trägt ein spezifischer „Homing“-Schalter an Zellen, genannt CCR7, dazu bei, dass Zellen des inflammatorischen Brustkrebses diese Lymphbahnen und benachbarte Lymphknoten finden und besiedeln? Wenn ja, könnte dieser Schalter ein neues Ziel für künftige zielgerichtete Therapien werden.
Ein gefährliches Ausbreitungsmuster
Im Gegensatz zu den bekannteren Brustkrebserkrankungen, die meist als klar tastbare Knoten auftreten, zeigt sich das inflammatorische Mammakarzinom häufig als schmerzhafte, geschwollene und verfärbte Brust. Unter dem Mikroskop sind die Lymphkanäle der Haut mit Tumorzell-Clustern gefüllt. Da diese Gefäße direkt mit Lymphknoten und dem übrigen Körper verbunden sind, ist es entscheidend zu verstehen, was Krebszellen in dieses Netzwerk zieht, um nachzuvollziehen, warum diese Krankheit so schnell streut und schwerer zu heilen ist.
Der Zell-“Homing“-Schalter CCR7
CCR7 ist ein Rezeptor, der normalerweise auf bestimmten Immunzellen vorkommt und ihnen hilft, über Lymphgefäße zu den Lymphknoten zu gelangen, wo Immunantworten koordiniert werden. Er wirkt wie ein Schloss, das chemische „Schlüssel“ erkennt, die in lymphatischem Gewebe freigesetzt werden. Frühere Forschungen bei anderen Krebsarten legten nahe, dass Tumorzellen, die dieses Schloss-Schlüssel-System nutzen, leichter in Lymphgefäße eindringen und in entfernten Bereichen Samen bilden können. Die Rolle von CCR7 beim inflammatorischen Mammakarzinom war vor dieser Studie jedoch nicht detailliert untersucht worden.
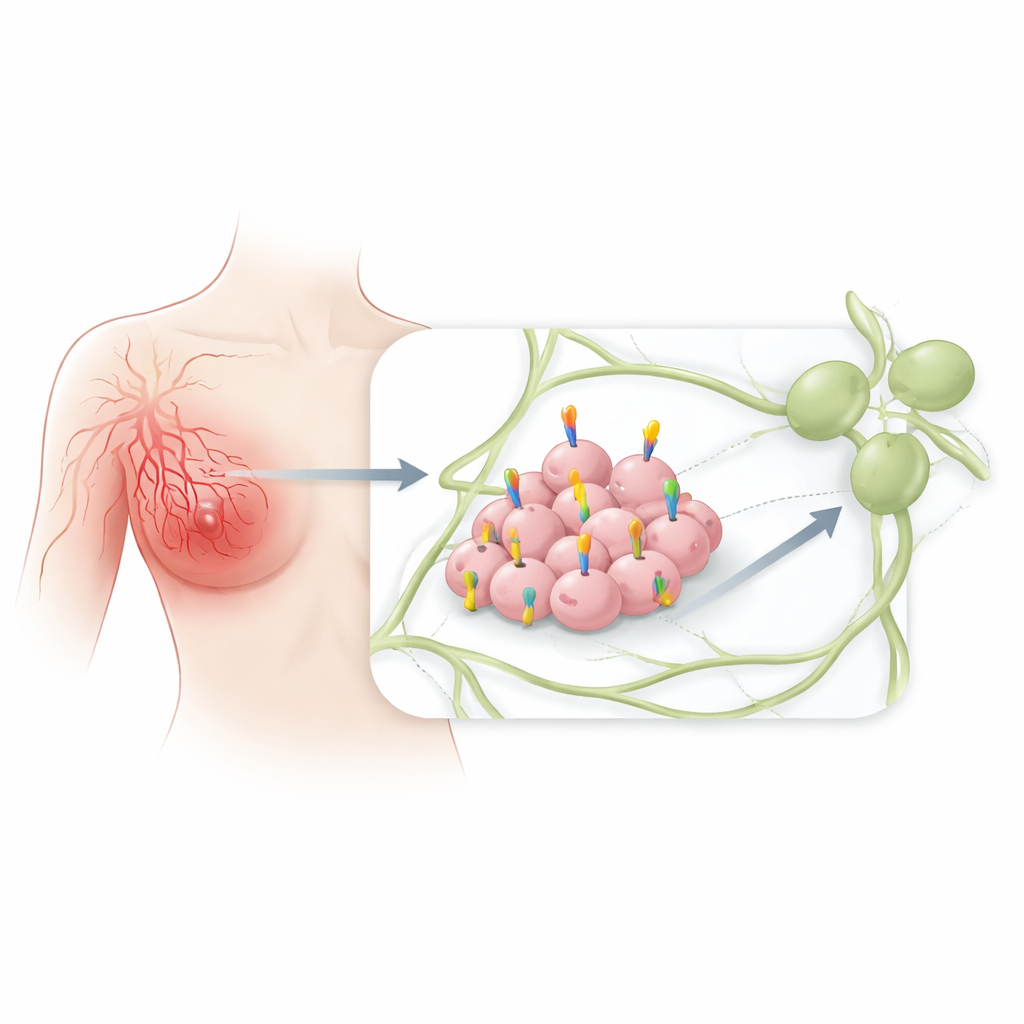
CCR7 in Modellen und Patient*innenproben verfolgen
Die Forschenden untersuchten zunächst experimentelle Modelle. Bei Mäusen, deren Brustgewebe durch eine fettreiche Ernährung und veränderte Stillmuster – Bedingungen, die Entzündung und lymphatische Aktivität erhöhten – geprägt war, fanden sie erhöhte CCR7-ähnliche Signale in der Mamma. Anschließend untersuchten sie Brustkrebszelllinien im Labor und stellten fest, dass sowohl inflammatorische als auch nicht-inflammatorische Brustkrebszellen CCR7-Protein produzierten, was darauf hindeutet, dass dieser Rezeptor Tumorzellen allgemein zur Verfügung steht. Dann verglichen sie mithilfe einer großen internationalen Datenbank von Tumorgenprofilen 137 inflammatorische Brustkrebserkrankungen mit 252 nicht-inflammatorischen Fällen. Die CCR7-Genaktivität war in inflammatorischen Tumoren signifikant erhöht, ebenso wie die Aktivität des wichtigsten chemischen Partners CCL21, der in lymphatischen Zellen reichlich vorhanden ist.
Welche Tumoren das stärkste Signal zeigen
Nicht alle inflammatorischen Brustkrebserkrankungen sind gleich. Als das Team die Tumoren anhand gängiger klinischer Marker gruppierte, war die CCR7-Genaktivität besonders hoch in solchen ohne Östrogenrezeptoren und in solchen, die in die HER2-positiven oder basal-like Kategorien fielen – Subtypen, die bereits für schlechtere Prognosen bekannt sind. CCL21, das wichtigste Partnersignal für CCR7, war ebenfalls tendenziell in HER2-positiven Tumoren erhöht. Als die Wissenschaftler*innen jedoch die Überlebensdaten der großen Datensammlung betrachteten, fanden sie keinen einfachen Zusammenhang zwischen höheren CCR7- oder CCL21-Genlevels und dem Gesamtüberleben. Das deutet darauf hin, dass möglicherweise wichtiger ist, wie und wo das Protein an der Zelloberfläche genutzt wird, als allein der Genausdruck.
CCR7 direkt im Tumorgewebe sichtbar machen
Um zu prüfen, wie sich das in echten Tumoren darstellt, färbten die Forschenden Gewebemikroarrays aus Mastektomieproben von inflammatorischem Brustkrebs. Fast jede Probe mit ausreichend Tumorgewebe zeigte CCR7 an den Krebszellen, meist als starkes, kontinuierliches Band an der Zelloberfläche. Viele Tumoren hatten nahezu alle Zellen gefärbt. Dieses weit verbreitete Vorkommen stützt die Idee, dass CCR7 zur grundlegenden Werkzeugkiste inflammatorischer Brustkrebszellen gehört, selbst wenn die geringe Patientenzahl die Möglichkeit einschränkte, Färbemuster mit klinischen Ergebnissen wie Rezidiv oder Überleben zu verknüpfen.
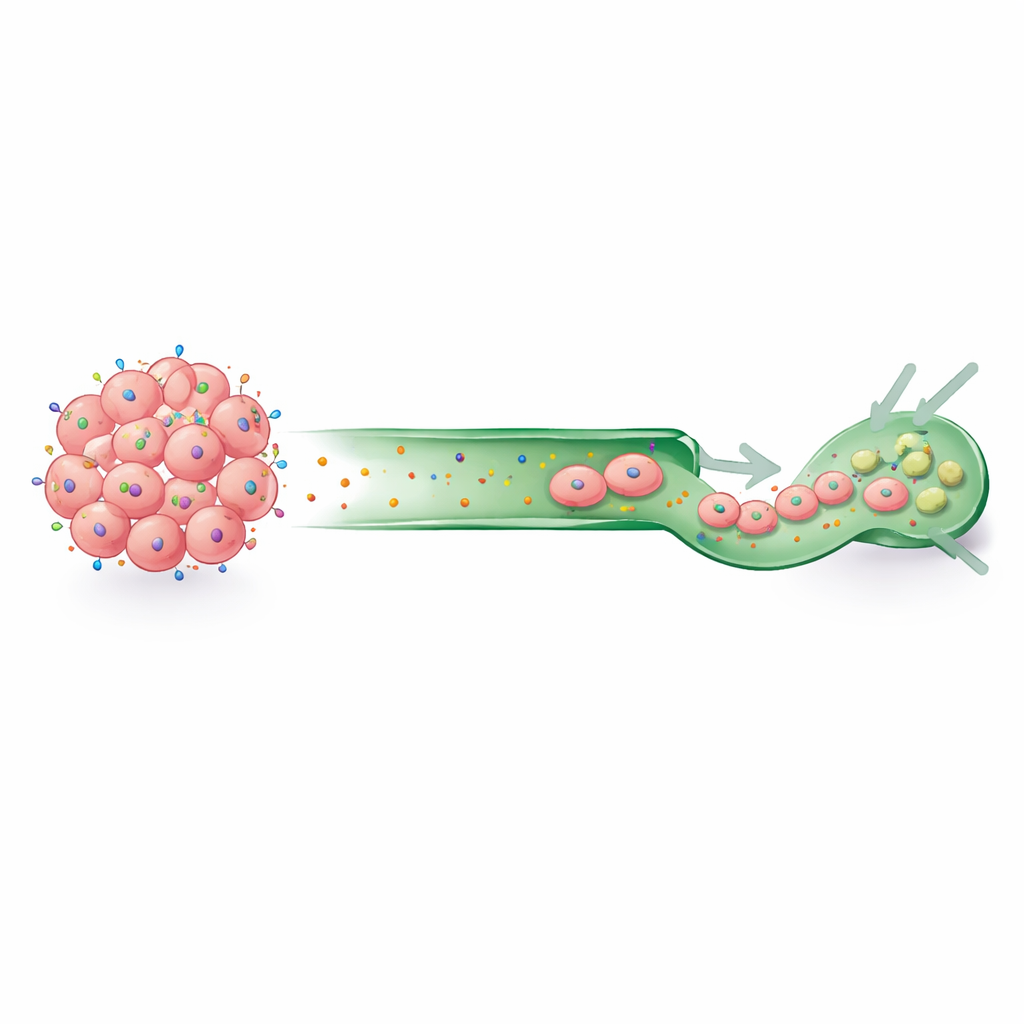
Was das für künftige Behandlungen bedeutet
In der Summe zeichnen die Ergebnisse CCR7 als häufig und insbesondere auf Genebene aktiv beim inflammatorischen Mammakarzinom, vor allem in schwerer zu behandelnden Subtypen. Seine Partnerschaft mit CCL21 und seine bekannte Rolle beim Anheuern in Lymphgefäße lassen vermuten, dass es Krebszellen helfen könnte, in Lymphkanäle einzudringen und sich dort zu verbreiten. Die Studie hebt CCR7 als vielversprechenden Kandidaten für zielgerichtete Therapien hervor, etwa Antikörper-Wirkstoff-Konjugate, die toxische Wirkstoffe direkt an CCR7-exprimierende Zellen liefern. Während weitere Arbeiten in größeren Patientengruppen nötig sind, um zu bestätigen, wie CCR7 Ausbreitung und Verlauf beeinflusst, schafft diese Forschung die Grundlage, einen Schlüsseltreiber lymphatischer Invasion in eine potenzielle therapeutische Verwundbarkeit zu verwandeln.
Zitation: Chen, J.H., Balema, W., Krishnamurthy, S. et al. CCR7 immune cell receptor expression in inflammatory breast cancer. Sci Rep 16, 13513 (2026). https://doi.org/10.1038/s41598-026-43437-4
Schlüsselwörter: inflammatorisches Mammakarzinom, CCR7, lymphatische Ausbreitung, HER2-positiver Brustkrebs, zielgerichtete Therapie