Clear Sky Science · fr
Vers une détection automatisée robuste des arythmies cardiovasculaires par apprentissage auto-supervisé et transformers vision unidimensionnels
Pourquoi des moniteurs cardiaques plus intelligents comptent
Les maladies cardiaques sont la première cause de mortalité dans le monde, et les médecins enregistrent aujourd’hui des centaines de millions de tracés cardiaques, ou ECG, chaque année. Ces lignes sinueuses peuvent révéler des troubles du rythme dangereux, mais il est impossible de faire examiner manuellement chaque tracé par un expert. Cet article explore comment l’intelligence artificielle moderne peut apprendre directement à partir d’énormes collections d’ECG — dont la plupart n’ont jamais été étiquetés par un humain — pour reconnaître les rythmes anormaux de manière plus précise, plus fiable et suffisamment rapide pour une surveillance en temps réel sur des appareils courants.
Apprendre à partir d’océans de battements cardiaques non étiquetés
Les systèmes informatiques traditionnels pour lire les ECG nécessitent de nombreux exemples soigneusement annotés et peinent encore face à des données réelles bruitées. Les auteurs exploitent à la place une ressource massive que les hôpitaux et les dispositifs portables génèrent déjà : des millions d’enregistrements ECG bruts jamais annotés. Ils conçoivent une méthode permettant à un modèle d’IA de s’enseigner les motifs d’activité cardiaque normale et anormale en prédisant des parties manquantes du signal, un mode d’entraînement connu sous le nom d’apprentissage auto‑supervisé. En maîtrisant d’abord le « langage » général des battements cardiaques à partir de 8,2 millions d’enregistrements non étiquetés, le système peut ensuite être affiné avec un ensemble beaucoup plus réduit de cas annotés par des experts pour identifier de nombreux troubles du rythme.
Transformer les tracés de battements en segments compréhensibles pour le modèle
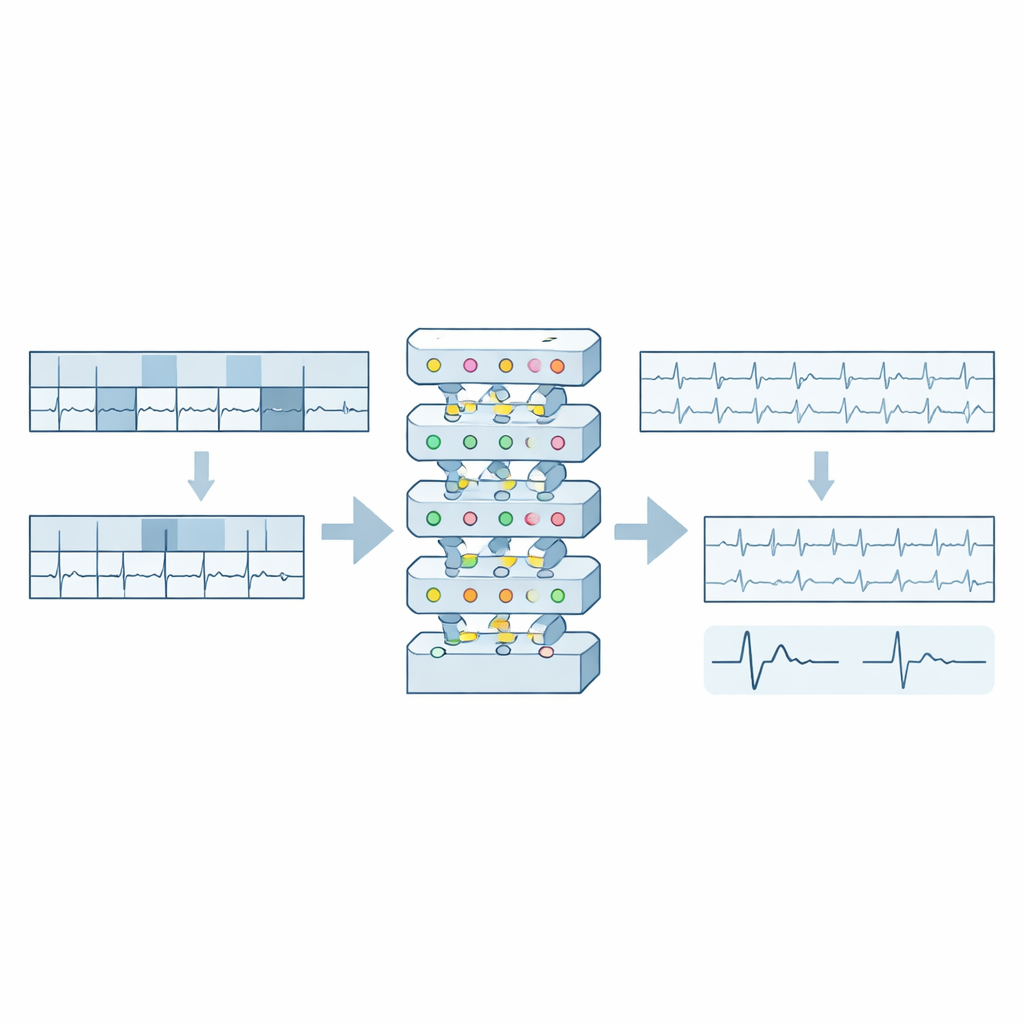
La plupart des approches précédentes convertissaient les signaux ECG en images puis utilisaient des systèmes basés sur l’imagerie, ce qui gaspille de l’espace et atténue les détails fins. Ce travail conserve les données dans leur forme unidimensionnelle naturelle. Les auteurs présentent PatchECG, un modèle qui découpe chaque ECG de 10 secondes en petits « patchs » d’une demi‑seconde par dérivation, puis en masque environ 40 %. La tâche d’entraînement du modèle consiste à reconstruire les patchs manquants à partir du contexte restant, l’obligeant à apprendre comment les ondes et les rythmes se déroulent dans le temps. Cette stratégie préserve les variations subtiles de l’ECG cruciales pour le diagnostic, comme de minuscules décalages dans les segments associés aux infarctus, tout en évitant la perte d’information liée à la compression des signaux en images basse résolution.
Surpasser des méthodes établies avec moins de calcul
Après un auto‑entraînement sur des données non étiquetées, PatchECG est affiné pour plusieurs tâches diagnostiques réelles : reconnaître des dizaines de problèmes de rythme et structurels dans un jeu de référence largement utilisé, combiner plusieurs jeux de données publics pour constituer la plus grande collection d’ECG étiquetés à ce jour, et détecter un type dangereux d’infarctus du myocarde appelé STEMI. Dans ces évaluations, PatchECG égalise ou dépasse des systèmes existants performants, y compris des réseaux récurrents sophistiqués et des transformers basés sur l’imagerie, tout en utilisant environ le cinquième du temps de calcul d’un concurrent de premier plan. Le modèle se distingue particulièrement par la cohérence de ses prédictions entre différents groupes de patients et jeux de données, avec des intervalles d’incertitude beaucoup plus serrés que les approches plus anciennes. Cette stabilité est importante pour instaurer la confiance dans des outils susceptibles, à terme, d’orienter des décisions de traitement urgentes.
Gérer des données désordonnées et des déséquilibres de conditions
Les jeux de données ECG réels sont loin d’être parfaits : certains diagnostics sont rares, de nombreuses étiquettes sont incertaines voire erronées, et les enregistrements sont souvent contaminés par des mouvements et des bruits électriques. Les auteurs montrent que leur entraînement auto‑supervisé rend PatchECG plus robuste à ces problèmes. Lorsqu’ils analysent les performances par diagnostic, ils constatent que les classes avec une confiance d’expert plus faible dans les étiquettes sont aussi plus difficiles pour le modèle, ce qui suggère que l’outil pourrait aider à signaler des entrées douteuses pour une revue humaine. Ils expérimentent également des techniques modernes d’affinage qui ne mettent à jour que de petites portions du réseau et des augmentations des données au moment du test. Ensemble, ces mesures apportent un gain modeste mais significatif — plus de 2 points de pourcentage sur des mesures clés de précision — sans alourdir le coût calculatoire.
Ce que cela signifie pour les soins cardiaques futurs
En termes simples, cette étude montre qu’un modèle d’IA unidimensionnel soigneusement conçu peut apprendre les rythmes du cœur à partir de millions d’ECG non étiquetés, puis appliquer cette connaissance pour détecter rapidement et efficacement des problèmes dangereux. En évitant le détour par des images, PatchECG conserve davantage de détails d’intérêt médical et fonctionne plus rapidement, ce qui en fait un candidat solide pour des systèmes de surveillance continue, du lit d’hôpital à la montre connectée. Bien que des essais cliniques restent nécessaires avant un déploiement, ce travail pose les bases d’une analyse automatisée d’ECG plus fiable, évolutive et largement accessible, capable d’aider à détecter des arythmies potentiellement mortelles avant qu’elles ne deviennent fatales.
Citation: Chatterjee, M., Chan, A.D.C. & Komeili, M. Toward robust automated cardiovascular arrhythmia detection using self-supervised learning and 1-dimensional vision transformers. Sci Rep 16, 11793 (2026). https://doi.org/10.1038/s41598-026-41549-5
Mots-clés: électrocardiogramme, détection d’arythmie, apprentissage auto-supervisé, modèles Transformer, IA médicale