Clear Sky Science · fr
Une chaîne hybride pour la segmentation de l’artère carotide utilisant YOLOv11n et des modèles de contours
Pourquoi c’est important pour la prévention des AVC
Les AVC surviennent souvent sans signes avant‑coureurs, mais beaucoup débutent silencieusement au niveau du cou, où les artères carotides apportent le sang au cerveau. Les médecins peuvent repérer des lésions précoces dans ces artères par échographie, un examen rapide et indolore, mais tracer manuellement le canal sanguin sur chaque image est long et subjectif. Cette étude présente une méthode entièrement automatique capable de délimiter rapidement l’artère carotide dans les vues échographiques courantes, même sur du matériel modeste, dans le but d’accélérer l’évaluation du risque d’AVC, d’en fiabiliser les résultats et d’en faciliter le déploiement en clinique de routine. 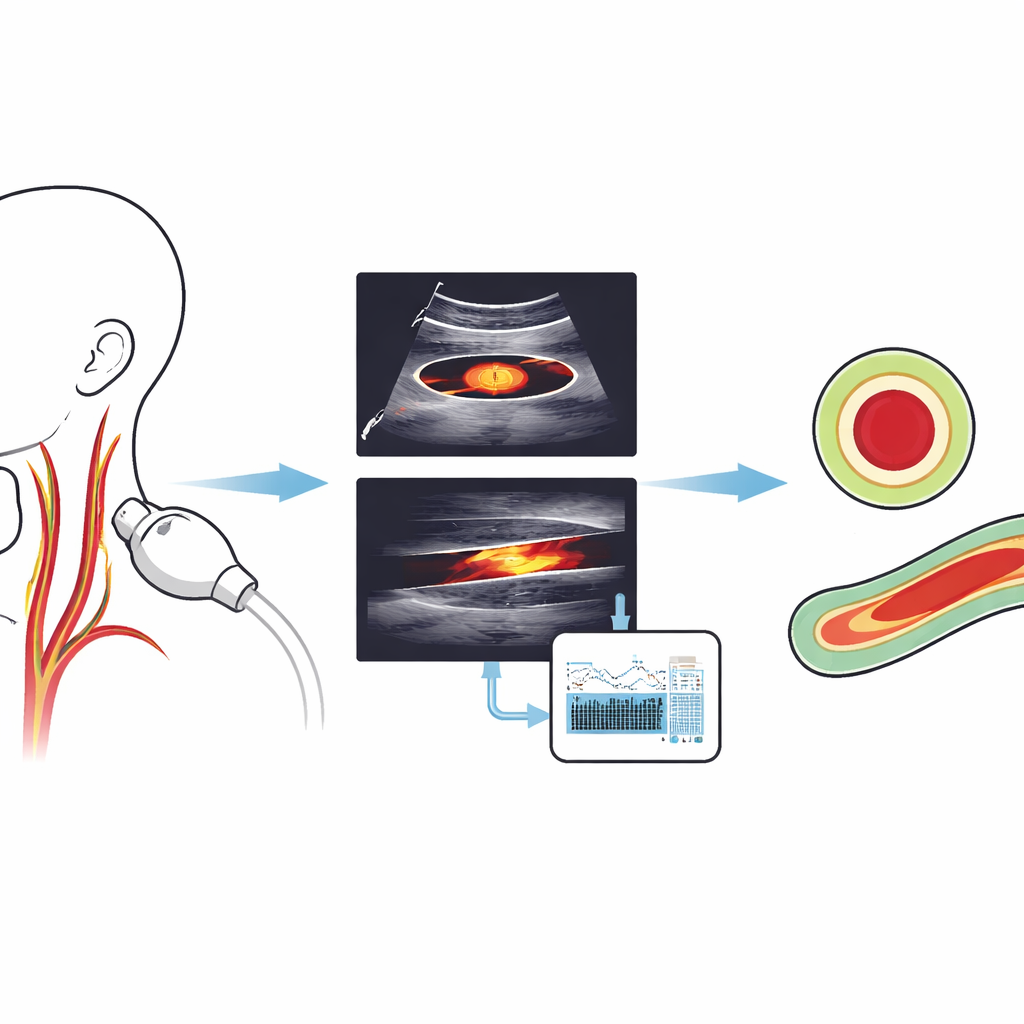
Dangers cachés dans les vaisseaux du cou
Les artères carotides peuvent se rétrécir à mesure que des dépôts graisseux s’accumulent dans leurs parois, réduisant l’apport sanguin au cerveau et augmentant le risque d’AVC. Comme les symptômes n’apparaissent souvent qu’après des lésions avancées, le dépistage régulier des personnes à risque — comme les personnes âgées, les fumeurs et les patients atteints de diabète ou de maladies cardiaques — est essentiel. L’imagerie par échographie est idéale pour ce dépistage : peu coûteuse, sûre et largement disponible. Cependant, les images sont bruyantes et de faible contraste, et des structures voisines comme la veine jugulaire peuvent ressembler à tort à l’artère. En conséquence, dessiner la frontière interne exacte du vaisseau — le « lumen » — reste une tâche difficile et chronophage pour les humains comme pour les machines.
Un assistant numérique en trois étapes pour les médecins
Les auteurs ont conçu une chaîne hybride qui imite la façon dont un technicien attentif analyserait les images échographiques, mais de façon automatique. D’abord, un détecteur compact d’apprentissage profond, une version moderne de la famille YOLO (« You Only Look Once »), analyse chaque image et trace un cadre qui encadre précisément le lumen de la carotidienne, tant en coupe transversale (vue circulaire) qu’en vue longitudinale (vue tubulaire). Cette étape concentre l’attention sur la bonne région du cou et s’est révélée extrêmement fiable : le modèle manque presque jamais le vaisseau sur les données de test.
Ensuite, pour les images en coupe transversale, le système améliore la qualité de l’échographie à l’intérieur de ce cadre via une séquence de filtres finement ajustés. Il lisse le motif granuleux de speckle tout en préservant les contours, renforce le contraste local pour faire ressortir la paroi artérielle, ajuste la luminosité, débruite à plus grande échelle, puis affine enfin la frontière. Ces opérations reconfigurent le « paysage d’énergie » perçu par l’algorithme de suivi de contour qui suit, faisant de la véritable arête du lumen le chemin le plus attractif pour la courbe plutôt que le bruit aléatoire. 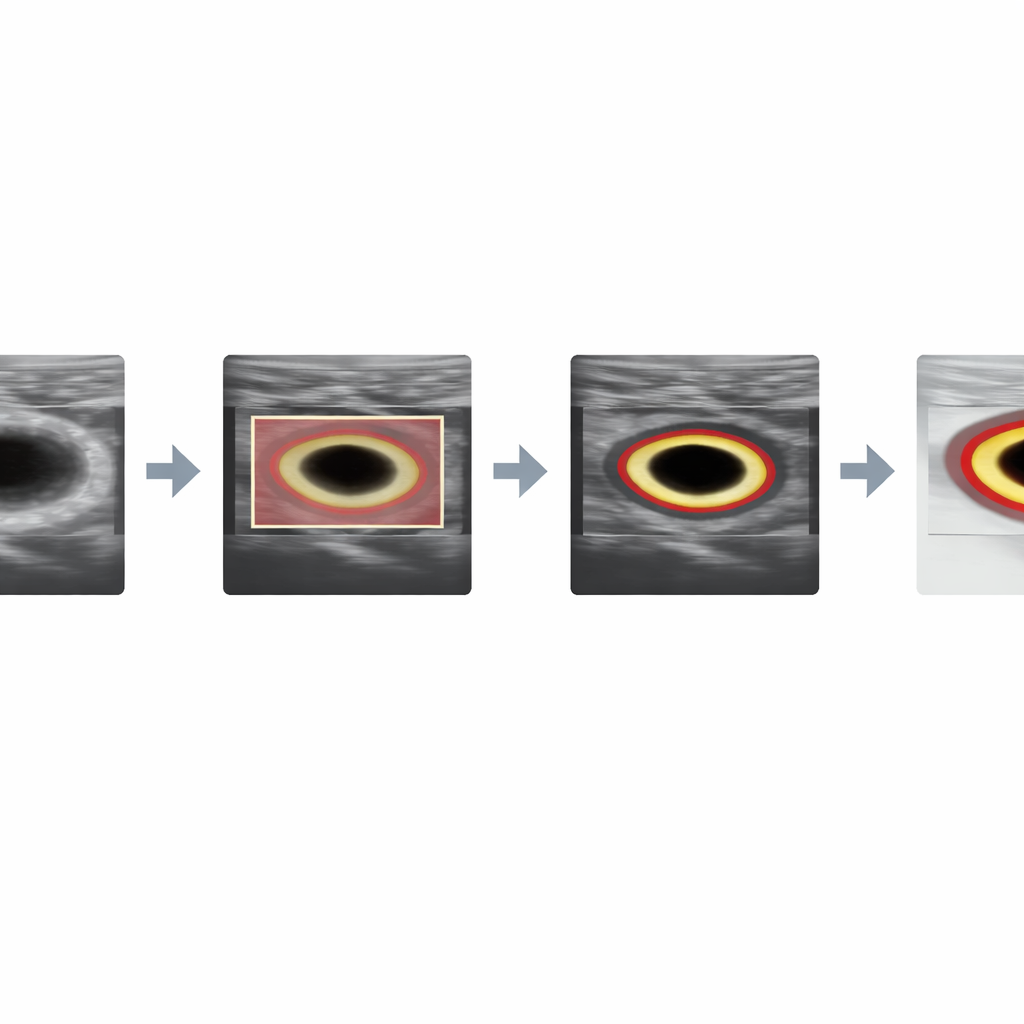
Des contours intelligents qui se verrouillent sur le bon vaisseau
Une fois les images en coupe transversale nettoyées, un modèle de contour actif classique — parfois appelé « snake » — démarre depuis le cadre du détecteur et glisse progressivement vers la frontière la plus proche et la plus marquée. Parce que le prétraitement a amplifié la véritable arête du vaisseau et réduit les artefacts parasites, le snake s’ajuste proprement autour du lumen. Pour les images longitudinales, le défi est différent : le cadre initial du détecteur peut contenir à la fois l’artère carotide et la veine jugulaire, qui apparaissent toutes deux sombres car remplies de sang. Pour éviter cette confusion, les auteurs extraient automatiquement un second cadre plus précis en scannant à l’intérieur du premier la zone la plus sombre et la plus uniforme, typique de l’intérieur de l’artère, puis en l’étendant de manière contrôlée. Cette région raffinée initialise un modèle de contour Chan–Vese, une méthode qui fait croître une frontière en se basant sur les différences d’intensité des pixels à l’intérieur et à l’extérieur de la courbe. Correctement initialisé, il peut suivre le long lumen légèrement incurvé tout en ignorant les veines voisines.
Quel est le gain réel en performance ?
L’équipe a testé son système sur deux jeux de données publics : plus d’un millier d’images en coupe transversale et des dizaines d’images longitudinales, chacune accompagnée de contours du lumen tracés par des experts pour comparaison. Ils ont utilisé une validation croisée en cinq plis et des jeux de test séparés pour éviter le surapprentissage et simuler la performance sur des patients non vus. Pour les coupes transversales, la méthode atteint un score Dice — mesure du recouvrement entre contours automatiques et experts — d’environ 91 %, avec une précision globale proche de 99,6 %. Pour les images longitudinales, le score Dice monte à environ 95 % et la précision à environ 97,7 %. Une étude d’ablation, où certaines parties de la chaîne ont été volontairement retirées, a montré que la localisation initiale ainsi que le prétraitement sur mesure ou la génération d’un masque affiné étaient indispensables ; sans eux, la performance chutait fortement ou les algorithmes devenaient numériquement instables.
Ce que cela implique pour les soins futurs
Pour un non‑spécialiste, ces chiffres signifient qu’un système informatique peu coûteux peut désormais tracer le canal porteur de sang dans les examens échographiques carotidiens presque aussi fidèlement qu’un spécialiste entraîné, et le faire en moins d’une seconde pour les vues en coupe transversale, même sur un ordinateur portable basique. En combinant un réseau de détection moderne avec des méthodes de suivi de courbe bien comprises, l’approche offre à la fois rapidité et interprétabilité. Si elle était largement adoptée et étendue pour analyser la plaque en plus du lumen, de tels outils pourraient aider à transformer l’échographie cervicale de routine en un système d’alerte précoce plus efficace pour les AVC, en fournissant aux cliniciens des mesures cohérentes et objectives partout où des appareils à ultrasons sont utilisés.
Citation: Salama, G.M., Safy, M., Hassanin, D.A. et al. A hybrid pipeline for carotid artery segmentation using YOLOv11n and contour models. Sci Rep 16, 9808 (2026). https://doi.org/10.1038/s41598-026-41007-2
Mots-clés: échographie carotidienne, dépistage des AVC, segmentation d’images médicales, apprentissage profond en médecine, imagerie vasculaire