Clear Sky Science · de
Eine hybride Pipeline zur Segmentierung der Halsschlagader mithilfe von YOLOv11n und Konturmodellen
Warum das für die Schlaganfallprävention wichtig ist
Schlaganfälle treten oft unerwartet auf, beginnen aber vielerorts still im Hals, wo die Halsschlagadern das Gehirn mit Blut versorgen. Ärztinnen und Ärzte können frühe Schäden an diesen Arterien im Ultraschall erkennen, einem schnellen und schmerzfreien Verfahren, doch das sorgfältige Nachzeichnen des Blutkanals von Hand in jedem Bild ist langsam und subjektiv. Diese Studie stellt eine vollautomatische Computermethode vor, die die Halsschlagader in gängigen Ultraschallansichten rasch umreißen kann, selbst auf bescheidener Hardware. Ziel ist, die frühzeitige Einschätzung des Schlaganfallrisikos schneller, verlässlicher und leichter in die tägliche Praxis überführbar zu machen. 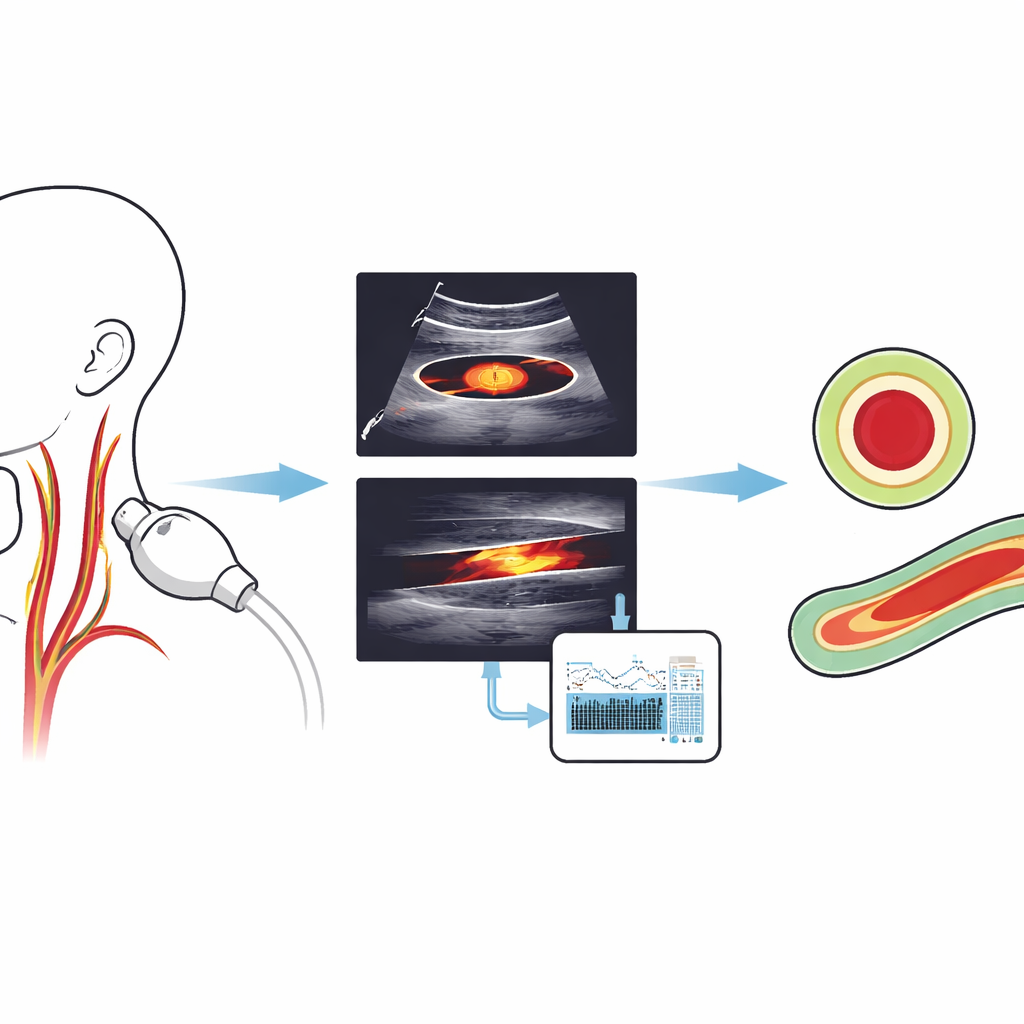
Verborgene Gefahren in den Halsgefäßen
Die Karotis kann sich verengen, wenn sich fettige Ablagerungen in ihren Wänden ansammeln, was den Blutfluss zum Gehirn einschränkt und das Schlaganfallrisiko erhöht. Da Symptome häufig erst nach schwerer Schädigung auftreten, ist die regelmäßige Untersuchung gefährdeter Personen—etwa älterer Menschen, Raucherinnen und Raucher sowie Patientinnen und Patienten mit Diabetes oder Herzkrankheiten—essenziell. Die Ultraschalldiagnostik eignet sich besonders für solche Screenings: Sie ist kostengünstig, sicher und weit verbreitet. Die Bilder sind jedoch verrauscht und kontrastarm, und benachbarte Strukturen wie die Jugularvene können der Arterie täuschend ähnlich sehen. Daher bleibt das präzise Zeichnen der inneren Gefäßgrenze—des sogenannten Lumens—sowohl für Menschen als auch für Maschinen eine schwierige und zeitaufwändige Aufgabe.
Ein dreistufiger digitaler Assistent für Ärztinnen und Ärzte
Die Autoren entwarfen eine hybride Pipeline, die nachahmt, wie ein sorgfältiger Techniker Ultraschallbilder analysiert, dies jedoch automatisch erledigt. Zuerst durchsucht ein kompakter Deep‑Learning-Detektor, eine moderne Variante der YOLO‑(„You Only Look Once“) Objekt‑Erkennungsfamilie, jedes Bild und zieht ein Rechteck, das das Lumen der Karotis eng umschließt, sowohl in der Querschnittsaufnahme (kreisförmige Ansicht) als auch in der Längsaufnahme (röhrenförmige Ansicht). Dieser Schritt fokussiert die Aufmerksamkeit auf die richtige Halsregion und erwies sich als äußerst verlässlich: Das Modell verfehlte das Gefäß in den Testdaten fast nie.
Für Querschnittsbilder verbessert das System anschließend die Bildqualität innerhalb dieses Rechtecks durch eine sorgfältig abgestimmte Abfolge von Filtern. Es glättet das körnige Specklemuster unter Bewahrung von Kanten, verstärkt lokalen Kontrast, damit die Gefäßwand hervortritt, passt die Helligkeit an, entrauscht auf breiterer Ebene und schärft schließlich die Begrenzung. Diese Operationen verändern die „Energielandschaft“, die das nachfolgende Konturverfolgungs‑Algorithmus sieht, so dass die echte Lumenkante zum attraktivsten Pfad für die Kurve wird und nicht das zufällige Rauschen. 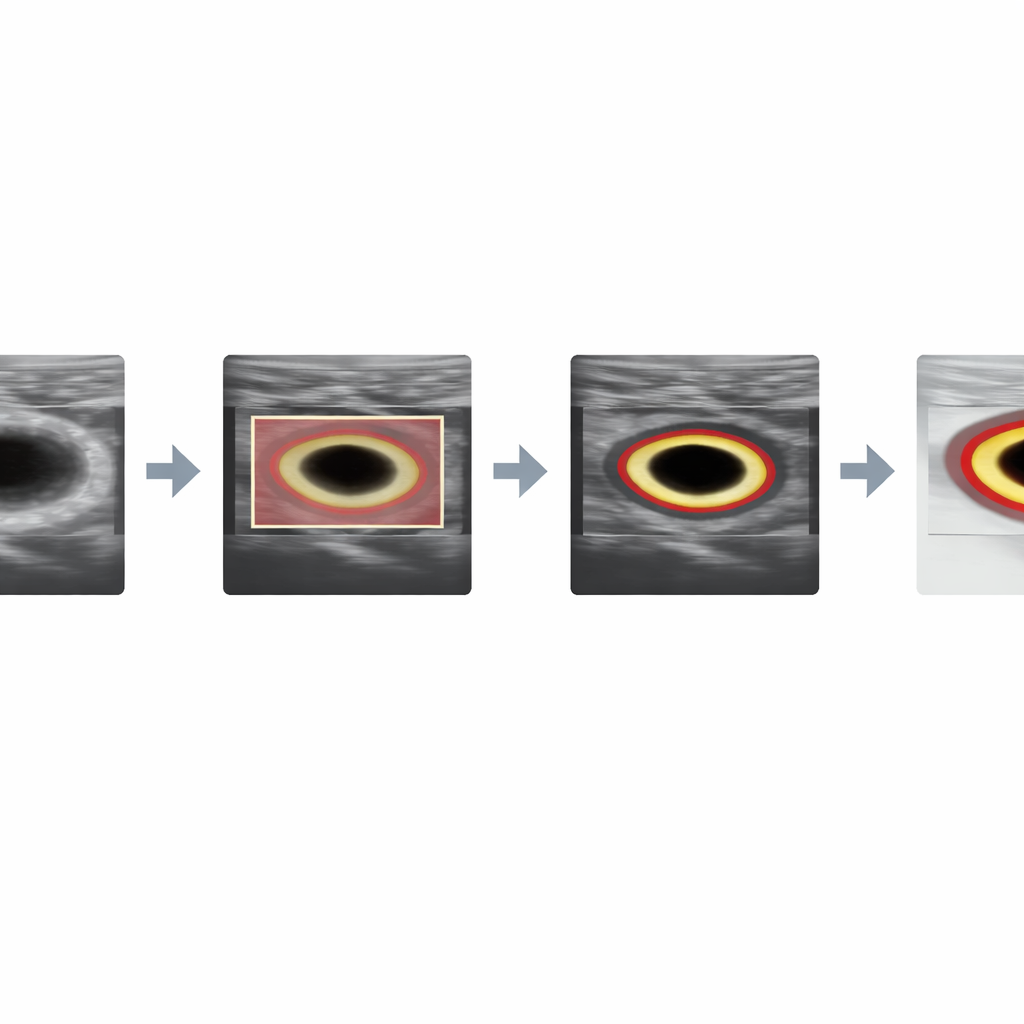
Intelligente Konturen, die das richtige Gefäß erfassen
Nachdem die Querschnittsbilder bereinigt sind, startet ein klassisches aktives Konturmodell—manchmal „Snake“ genannt—vom Detektorrechteck und gleitet schrittweise zur nächststarken Grenze. Weil die Vorverarbeitung die echte Gefäßkante verstärkt und ablenkende Artefakte reduziert hat, legt sich die Snake ordentlich um das Lumen. Bei den Längsaufnahmen ist die Herausforderung anders: Das ursprüngliche Detektorrechteck kann sowohl die Karotis als auch die Jugularvene enthalten, die beide wegen des blutgefüllten Inneren ähnlich dunkel erscheinen. Um diese Verwechslung zu vermeiden, schneiden die Autoren automatisch ein zweites, präziseres Rechteck aus, indem sie innerhalb des ersten nach dem dunkelsten, homogensten Bereich scannen—typisch für das Arterieninnere—und dieses dann kontrolliert vergrößern. Diese verfeinerte Region initialisiert ein Chan–Vese‑Konturmodell, eine Methode, die eine Grenze entsprechend der Intensitätsunterschiede innerhalb und außerhalb der Kurve wachsen lässt. Richtig gestartet kann es das lange, sanft gekrümmte Lumen verfolgen und benachbarte Venen ignorieren.
Wie gut funktioniert das tatsächlich?
Das Team testete sein System an zwei öffentlichen Datensätzen: über tausend Querschnittsbilder und Dutzende Längsbilder, jeweils mit Experten‑Lumenumrissen zum Vergleich. Sie nutzten Fünffach‑Cross‑Validation und getrennte Testmengen, um Überanpassung zu vermeiden und die Leistung an unbekannten Patienten zu simulieren. Bei Querschnitten erreichte die Methode einen Dice‑Score—ein Maß für die Überlappung zwischen automatischen und Expertenumrissen—von etwa 91 % bei einer Gesamtgenauigkeit nahe 99,6 %. Bei Längsaufnahmen stieg der Dice‑Score auf rund 95 % und die Genauigkeit auf etwa 97,7 %. Eine Ablationsstudie, in der Teile der Pipeline gezielt entfernt wurden, zeigte, dass sowohl die anfängliche Lokalisierung als auch die maßgeschneiderte Vorverarbeitung beziehungsweise die verfeinerte Maskengenerierung wesentlich sind; ohne sie brach die Leistung deutlich ein oder die Algorithmen wurden numerisch instabil.
Was das für die zukünftige Versorgung bedeutet
Für Nicht‑Spezialisten bedeuten diese Zahlen, dass ein kostengünstiges Computersystem jetzt den blutführenden Kanal in Karotis‑Ultraschallaufnahmen fast so treu nachzeichnen kann wie ein geschulter Spezialist—und dies in unter einer Sekunde für Querschnittsansichten selbst auf einem einfachen Laptop. Durch die Kombination eines modernen Detektionsnetzwerks mit gut verstandenen Kurvenverfolgungsmethoden bietet der Ansatz sowohl Geschwindigkeit als auch Interpretierbarkeit. Wenn solche Werkzeuge breit angenommen und erweitert werden, um nicht nur das Lumen, sondern auch Plaques zu analysieren, könnten sie routinemäßigen Halsultraschall in ein leistungsfähigeres Frühwarnsystem für Schlaganfälle verwandeln und Klinikpersonal überall dort mit konsistenten, objektiven Messungen unterstützen, wo Ultraschallgeräte eingesetzt werden.
Zitation: Salama, G.M., Safy, M., Hassanin, D.A. et al. A hybrid pipeline for carotid artery segmentation using YOLOv11n and contour models. Sci Rep 16, 9808 (2026). https://doi.org/10.1038/s41598-026-41007-2
Schlüsselwörter: Karotis-Ultraschall, Schlaganfall-Screening, medizinische Bildsegmentierung, Tiefe Lernverfahren in der Medizin, Gefäßbildgebung