Clear Sky Science · fr
Détection automatique de la malperfusion vasculaire fœtale via augmentation de données et amélioration d’algorithme
Pourquoi de minuscules indices dans le placenta comptent
Avant et après la naissance, le placenta soutient discrètement la vie du bébé en régulant le passage du sang, de l’oxygène et des nutriments entre la mère et le fœtus. Quand ce flux est perturbé, comme dans une affection appelée malperfusion vasculaire fœtale, les risques de retard de croissance, d’accouchement prématuré, voire de mort fœtale in utero augmentent. Pourtant, aujourd’hui, repérer les lésions caractéristiques dans le tissu placentaire repose encore sur l’examen visuel des lames au microscope par des spécialistes, un processus long et susceptible de varier d’un pathologiste à l’autre. Cette étude examine comment l’intelligence artificielle moderne peut aider à lire ces motifs tissulaires subtils de façon plus cohérente, ouvrant la voie à des soins plus rapides et plus fiables durant la grossesse.
Des motifs cachés dans la ligne de vie du nourrisson
La malperfusion vasculaire fœtale survient lorsque le flux sanguin du fœtus à travers le placenta est obstrué de façon chronique, souvent en raison de problèmes du cordon ombilical, de caillots ou d’hypertension. Au microscope, cela se manifeste par une constellation de petites lésions — vaisseaux bouchés, villosités endommagées ou dépeuplées, et de petites zones de thrombus ou de cicatrisation. Reconnaître ces motifs après l’accouchement peut alerter les cliniciens sur les risques de santé à long terme du nouveau‑né et guider une surveillance plus rapprochée lors de grossesses ultérieures. Mais les lésions varient beaucoup en taille et en apparence, et elles peuvent être disséminées sur de larges sections du placenta. Dans les hôpitaux encombrés ou les régions où les spécialistes sont rares, cela complique le diagnostic cohérent et augmente la probabilité que des signaux d’alerte importants passent inaperçus.
Apprendre aux ordinateurs à lire des images tissulaires
Les chercheurs se sont donné pour objectif de construire un système automatisé capable de détecter ces lésions à partir d’images numériques de tissu placentaire coloré. Ils ont commencé avec des échantillons provenant de 310 grossesses compliquées par un diabète gestationnel, créant près de deux mille images recadrées capturant sept types de lésions courantes associées à la malperfusion vasculaire fœtale. Parce que les modèles d’apprentissage profond performants exigent généralement bien plus de données que ce que la médecine peut facilement fournir, l’équipe s’est tournée vers un cadre d’imagerie médicale appelé MONAI. Ce logiciel génère des variations réalistes des images existantes — légers retournements, étirements, flous, renforcement, et modifications de couleur et de contraste qui imitent les différences réelles dans la préparation des lames et le numériseur — tout en préservant les structures diagnostiques clés. Doubler ainsi les données d’entraînement a donné au modèle une « expérience » plus riche de la façon dont une même lésion peut apparaître dans des conditions légèrement différentes.
Comment fonctionne le système de vision amélioré
Au‑dessus de cette bibliothèque d’images étendue, l’équipe a amélioré un réseau de détection d’objets rapide connu sous le nom de YOLOv11. Les versions standard de tels réseaux peuvent peiner à détecter les anomalies très petites et aux bords fins, fréquentes dans les maladies placentaires, en particulier quand chaque image couvre une vaste surface. Les auteurs ont ajouté un module d’attention LocalWindow, qui segmente conceptuellement les caractéristiques de l’image en nombreuses petites fenêtres et permet au modèle de concentrer sa puissance de calcul à l’intérieur de chaque patch. Dans ces fenêtres, une série d’étapes d’attention met en avant les formes et textures les plus informatives — comme de subtiles altérations des parois vasculaires ou des bords villositaires — tout en atténuant l’arrière‑plan uniforme. Cette conception aide le système à cibler les petites lésions sans être submergé par le tissu normal environnant, à la manière d’un pathologiste qui réduit mentalement son champ d’attention à un coin suspect d’une lame.
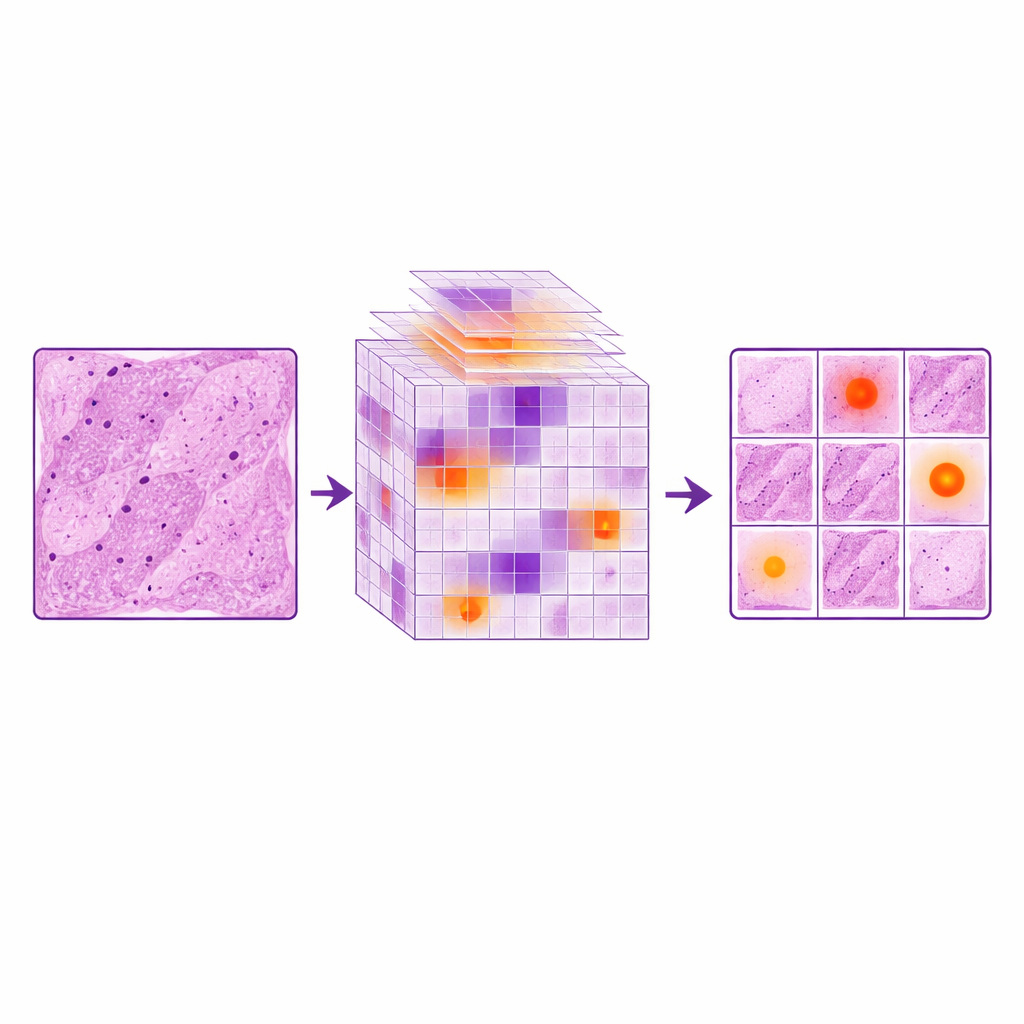
Mesurer les gains en précision et en fiabilité
Pour évaluer l’apport de chaque composant, les chercheurs ont comparé trois configurations : le modèle YOLOv11 original, le même modèle entraîné sur des images simplement dupliquées, et les versions améliorées utilisant MONAI et le module LocalWindow séparément ou conjointement. La simple répétition d’images a en réalité détérioré les performances, suggérant que le modèle commençait à mémoriser les exemples limités au lieu d’apprendre des règles générales. En revanche, l’augmentation basée sur MONAI a réduit de façon drastique les lésions manquées et amélioré plusieurs scores de précision. Le module d’attention LocalWindow a encore renforcé la capacité du système à détecter des lésions de tailles différentes. Lorsque les deux stratégies ont été combinées, le modèle a obtenu ses meilleurs résultats, avec des indicateurs clés en hausse d’environ 6 à 10 % par rapport à la référence et dépassant plusieurs autres méthodes de détection populaires. Ses performances globales se rapprochaient de celles d’un pathologiste de niveau intermédiaire, tout en restant suffisamment rapides pour un usage pratique.
Ce que cela signifie pour les mères et les bébés
En associant une expansion réaliste des données à une façon plus ciblée de « regarder » le tissu, l’étude montre que les ordinateurs peuvent apprendre à signaler les lésions liées au flux sanguin placentaire avec une confiance croissante. Les auteurs soutiennent que de tels outils ne remplaceront pas les experts humains, mais pourront agir comme des assistants infatigables — présélectionnant les lames, mettant en évidence les régions suspectes et aidant à standardiser les comptes rendus entre hôpitaux. Cela pourrait être particulièrement précieux dans les centres où les pathologistes formés sont peu nombreux, où les problèmes placentaires subtils sont facilement négligés. Bien que le travail actuel ait été mené dans un seul hôpital et repose sur un jeu de données modeste, il trace une voie vers des systèmes multi‑centres plus larges qui soutiennent des soins de grossesse plus cohérents et fondés sur les données pour les grossesses à risque.
Citation: Li, X., Jiang, Z., Chen, F. et al. Automated detection of fetal vascular malperfusion via data augmentation and algorithm improvement. Sci Rep 16, 11042 (2026). https://doi.org/10.1038/s41598-026-39942-1
Mots-clés: placenta, malperfusion vasculaire fœtale, pathologie computationnelle, apprentissage profond, résultats de grossesse