Clear Sky Science · de
Automatisierte Erkennung fetaler vaskulärer Malperfusion durch Datenaugmentation und Algorithmusverbesserung
Warum winzige Hinweise in der Plazenta wichtig sind
Vor und nach der Geburt erhält die Plazenta still und unauffällig das Leben eines Babys, indem sie Blut, Sauerstoff und Nährstoffe zwischen Mutter und Fötus vermittelt. Wird dieser Fluss gestört, wie bei einer als fetale vaskuläre Malperfusion bezeichneten Erkrankung, steigen die Risiken für Wachstumsstörungen, Frühgeburt oder sogar Totgeburt. Noch immer beruht das Erkennen typischer Schäden im Plazentagewebe darauf, dass Experten Mikroskoppräparate visuell durchsuchen — ein zeitaufwändiger Prozess, der von Pathologe zu Pathologe variieren kann. Diese Studie untersucht, wie moderne künstliche Intelligenz helfen kann, diese subtilen Gewebemuster konsistenter zu lesen und so einen Schritt zu schnellerer und verlässlicherer Schwangerenvorsorge zu leisten.
Versteckte Muster in der Lebensader des Babys
Fetale vaskuläre Malperfusion entsteht, wenn der Blutfluss vom Fötus durch die Plazenta chronisch behindert ist, häufig durch Probleme mit der Nabelschnur, Blutgerinnsel oder Bluthochdruck. Unter dem Mikroskop zeigt sich dies als Konstellation kleiner Läsionen — verschlossene Gefäße, beschädigte oder entleerte Chorionzotten sowie winzige Bereiche mit Gerinnseln oder Vernarbung. Das Erkennen dieser Muster nach der Entbindung kann Ärzte auf langfristige Gesundheitsrisiken eines Neugeborenen hinweisen und eine engere Überwachung bei zukünftigen Schwangerschaften lenken. Die Läsionen variieren jedoch stark in Größe und Erscheinungsbild und können über große Plazentasektionen verstreut sein. In vielbeschäftigten Kliniken oder an Orten mit wenigen Spezialisten erschwert das eine konsistente Diagnostik und erhöht die Wahrscheinlichkeit, dass wichtige Warnsignale übersehen werden.
Computern beibringen, Gewebebilder zu lesen
Die Forschenden wollten ein automatisiertes System entwickeln, das diese Läsionen in digitalen Bildern gefärbten Plazentagewebes erkennt. Sie begannen mit Proben aus 310 Schwangerschaften mit Gestationsdiabetes und erstellten fast zweitausend zugeschnittene Bilder, die sieben häufige Läsionstypen erfassten, die mit fetaler vaskulärer Malperfusion in Verbindung stehen. Da leistungsstarke Deep‑Learning‑Modelle in der Regel weitaus mehr Daten verlangen, als in der Medizin leicht verfügbar sind, nutzte das Team ein medizinisches Bildverarbeitungs‑Framework namens MONAI. Diese Software erzeugt realistische Variationen vorhandener Bilder — subtile Spiegelungen, Dehnungen, Unschärfen, Schärfungen sowie Veränderungen von Farbe und Kontrast, die reale Unterschiede in Präparation und Scan widerspiegeln — und erhält dabei die diagnostisch relevanten Strukturen. Durch das Verdoppeln der Trainingsdaten erhielt das Modell eine breitere „Erfahrung“ darüber, wie dieselbe Läsion unter leicht veränderten Bedingungen erscheinen kann.
Wie das schlauere Sehsystem funktioniert
Auf dieser erweiterten Bildbibliothek bauten die Forschenden eine Verbesserung eines schnellen Objekterkennungsnetzwerks namens YOLOv11 auf. Standardversionen solcher Netze haben häufig Schwierigkeiten mit den winzigen, fein umrandeten Abnormalitäten, die bei Plazentakirankaere vorkommen, insbesondere wenn jedes Vollbild eine große Fläche abdeckt. Die Autor:innen fügten ein LocalWindow‑Attention‑Modul hinzu, das bildlich gesprochen die Bildmerkmale in viele kleine Fenster aufteilt und dem Modell erlaubt, seine Rechenleistung innerhalb jedes Fensters zu konzentrieren. Innerhalb dieser Fenster betonen mehrere Attention‑Stufen die informationsreichsten Formen und Texturen — etwa subtile Veränderungen an Gefäßwänden oder an den Rändern der Zotten — und reduzieren gleichförmigen Hintergrund. Dieses Design hilft dem System, sich auf kleine Läsionen zu fokussieren, ohne vom umgebenden Normalgewebe überwältigt zu werden, ähnlich wie ein Pathologe seine Aufmerksamkeit mental auf eine verdächtige Stelle eines Präparats richtet.
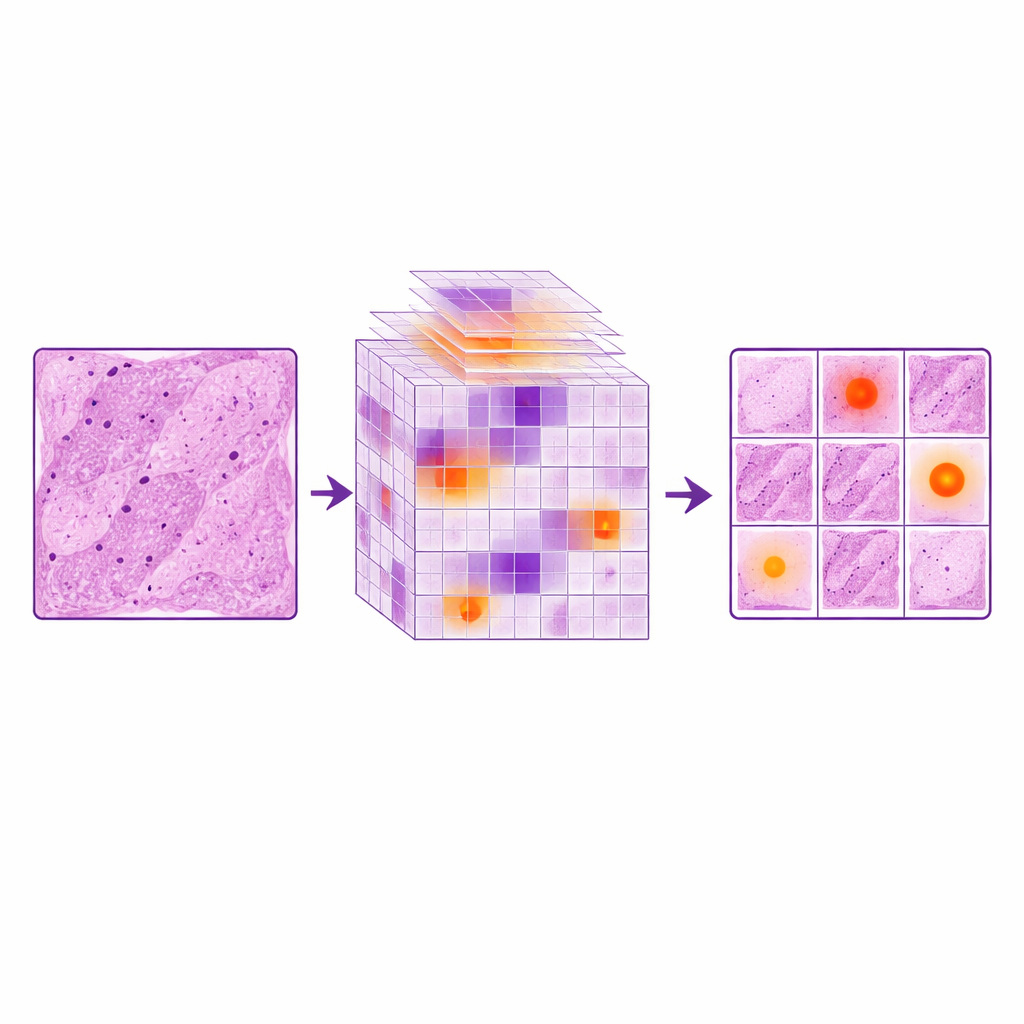
Bewertung von Genauigkeits- und Zuverlässigkeitsgewinnen
Um zu bestimmen, welchen Beitrag jede Komponente leistete, verglichen die Forschenden drei Setups: das ursprüngliche YOLOv11‑Modell, dasselbe Modell, das auf einfach duplizierten Bildern trainiert wurde, und die erweiterten Versionen mit MONAI und LocalWindow‑Attention einzeln oder kombiniert. Allein das Wiederholen von Bildern schädigte die Leistung tatsächlich, was darauf hindeutet, dass das Modell begann, die begrenzten Beispiele auswendig zu lernen, statt allgemeine Regeln zu lernen. Im Gegensatz dazu reduzierte die MONAI‑basierte Augmentation verfehlte Läsionen deutlich und verbesserte mehrere Genauigkeitsmaße. Das LocalWindow‑Attention‑Modul steigerte zusätzlich die Fähigkeit des Systems, Läsionen unterschiedlicher Größe zu erkennen. In Kombination erzielten die beiden Strategien die besten Ergebnisse: Wichtige Messwerte stiegen gegenüber der Referenz um etwa 6–10 Prozent und übertrafen eine Reihe anderer verbreiteter Detektionsmethoden. Die Gesamtleistung näherte sich der eines Pathologen auf mittlerem Niveau an, während das System trotzdem schnell genug für den praktischen Einsatz lief.
Was das für Mütter und Kinder bedeutet
Indem realistische Datenerweiterung mit einer fokussierteren Art des „Schauens“ auf Gewebe kombiniert wird, zeigt die Studie, dass Computer lernen können, Plazentablutflussstörungen zunehmend zuverlässig zu markieren. Die Autor:innen argumentieren, dass solche Werkzeuge menschliche Expert:innen nicht ersetzen, sondern als unermüdliche Assistenten dienen können — Präscreening von Präparaten, Hervorhebung verdächtiger Bereiche und Unterstützung bei der Standardisierung von Berichten zwischen Kliniken. Das könnte besonders in Zentren mit wenigen ausgebildeten Patholog:innen wertvoll sein, wo subtile Plazentaprobleme leicht übersehen werden. Obwohl die vorliegende Arbeit in einem einzelnen Krankenhaus mit einem eher überschaubaren Datensatz durchgeführt wurde, zeigt sie einen Weg zu breiteren, multizentrischen Systemen, die konsistentere, datengestützte Betreuung für gefährdete Schwangerschaften unterstützen.
Zitation: Li, X., Jiang, Z., Chen, F. et al. Automated detection of fetal vascular malperfusion via data augmentation and algorithm improvement. Sci Rep 16, 11042 (2026). https://doi.org/10.1038/s41598-026-39942-1
Schlüsselwörter: Plazenta, fetale vaskuläre Malperfusion, computationale Pathologie, Deep Learning, Schwangerschaftsergebnisse