Clear Sky Science · fr
Profilage épigénétique et transcriptionnel des cellules souches des follicules pileux secondaires pendant la pousse du cachemire
Pourquoi le cachemire doux commence par de minuscules cellules souches
Les pulls en cachemire donnent une sensation de luxe parce que les fibres sont exceptionnellement fines, douces et chaudes. Mais derrière chaque mèche de cachemire se joue un drame microscopique dans la peau des chèvres. Cette étude examine de près les cellules souches qui produisent les fibres de cachemire et les « interrupteurs » chimiques sur leur ADN qui leur indiquent quand se réveiller, travailler ou se reposer. En cartographiant ces interrupteurs dans le génome caprin, les chercheurs ont créé un atlas de référence qui pourrait, en fin de compte, aider les éleveurs, les biologistes et les producteurs textiles à comprendre — et peut‑être améliorer — la production de cachemire.
Du pelage de la chèvre à l’usine vivante de fibres
Le cachemire provient de structures cutanées particulières appelées follicules pileux secondaires, qui fonctionnent comme de minuscules usines produisant des fibres duveteuses et fines. Chaque follicule possède un réservoir de cellules souches capables de régénérer à plusieurs reprises de nouvelles fibres selon un cycle saisonnier, un peu comme un champ qui est replanté chaque année. Chez les chèvres cachemire, ces cycles sont étroitement liés à l’environnement : les fibres commencent à pousser au début du printemps et atteignent une production maximale à l’automne. L’équipe s’est concentrée sur les cellules souches de ces follicules à deux moments clés du cycle — début de la croissance et croissance intermédiaire — pour observer comment leurs systèmes de contrôle internes évoluent au fil du temps.
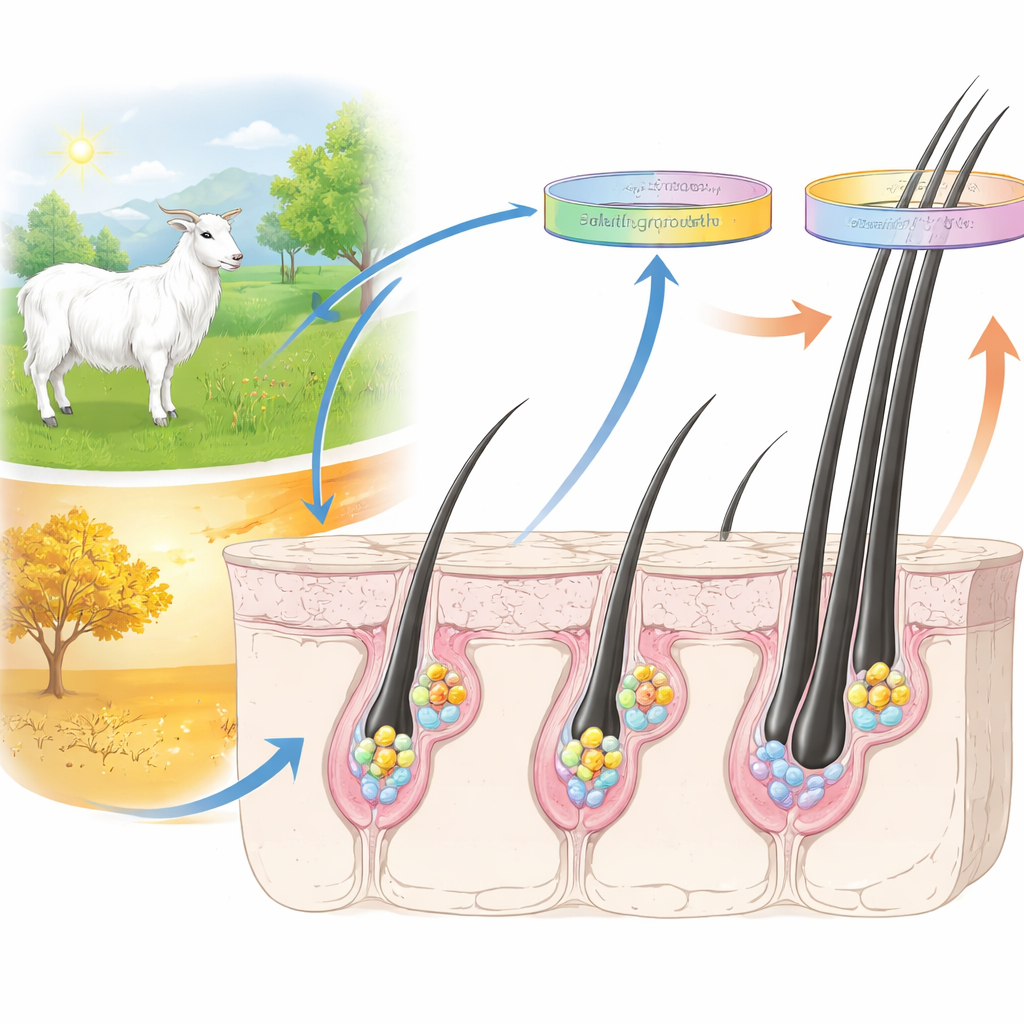
Lire les marques chimiques sur l’ADN
Les chercheurs se sont intéressés aux marques « épigénétiques » — de petites étiquettes chimiques attachées aux protéines qui emballent l’ADN. Ces marques ne modifient pas le code génétique lui‑même, mais influencent fortement les gènes qui sont activés ou réprimés, un peu comme des notes collantes placées sur les pages d’un livre indiquant « lire maintenant » ou « passer ce chapitre ». L’équipe a étudié quatre marques spécifiques sur les protéines histones, connues pour être associées aux gènes actifs, aux gènes silencieux ou aux régions de gènes en activité. Ils ont utilisé une technique appelée ChIP‑seq pour isoler les régions d’ADN portant chacune de ces marques, puis les ont séquencées sur l’ensemble du génome caprin, générant des millions de lectures par échantillon et construisant une carte détaillée de l’emplacement de ces marques.
Relier les motifs épigénétiques à l’activité des gènes
Pour comprendre comment ces étiquettes chimiques influencent réellement le travail des cellules souches, les scientifiques ont également mesuré les gènes activement lus dans les mêmes cellules à l’aide du séquençage ARN. Ils ont ensuite combiné ces deux types de données, comparant la présence ou l’absence de chaque marque d’histone près des points de départ des gènes avec les variations d’activité génique entre le début et la croissance intermédiaire. Les régions marquées par des étiquettes généralement associées aux gènes actifs avaient tendance à se situer près de gènes plus fortement exprimés, tandis que les marques liées à la répression génique montraient l’effet inverse. En utilisant des outils informatiques, ils ont regroupé des régions du génome en états actifs, en attente ou réprimés et ont suivi comment ces états évoluaient au fur et à mesure de la progression de la pousse du cachemire.
Contrôles rigoureux pour des données fiables
Parce que ce travail vise à servir de ressource partagée pour d’autres scientifiques, les auteurs ont consacré un effort substantiel au contrôle de qualité. Ils ont cultivé des cellules souches provenant de chèvres mâles et femelles soigneusement sélectionnées, vérifié l’identité et la pureté de ces cellules avec des marqueurs spécifiques, et assuré que l’ARN et l’ADN extraits étaient d’une très haute qualité. Ils ont ensuite vérifié que les expériences répétées donnaient pratiquement les mêmes résultats, montrant une forte concordance entre les échantillons provenant d’animaux différents. Les motifs des marques d’histones autour des sites de départ des gènes et au niveau de gènes connus pour être liés au poil se comportaient comme prévu, renforçant la confiance biologique que les cartes produites reflètent véritablement la régulation des cellules souches du cachemire.
Ce que cela signifie pour le cachemire et au‑delà
Pour les non‑spécialistes, l’idée principale est que la croissance du cachemire est contrôlée non seulement par les gènes, mais aussi par une couche complexe de marquages chimiques qui contribuent à décider quand ces gènes s’expriment. Cet article ne propose pas un gène miraculeux unique pour améliorer le cachemire ; il offre plutôt un atlas à haute résolution des interrupteurs qui guident les cellules souches pendant la saison de croissance du cachemire. En rendant toutes leurs données brutes et traitées accessibles au public, les chercheurs fournissent une base pour des travaux futurs visant à améliorer le rendement et la qualité des fibres, à explorer comment l’environnement et la sélection façonnent ces motifs épigénétiques, et à appliquer des approches similaires à d’autres animaux, voire à la biologie du cheveu humain.
Citation: Liang, X., Liu, B., Liu, Y. et al. Epigenetic and transcriptional profiling of secondary hair follicle stem cells during cashmere growth. Sci Data 13, 592 (2026). https://doi.org/10.1038/s41597-026-06972-3
Mots-clés: cachemire, cellules souches des follicules pileux, épigénétique, modification des histones, séquençage ARN