Clear Sky Science · de
Epigenetische und transkriptionelle Profilierung sekundärer Haarfollikel-Stammzellen während des Kaschmirwachstums
Warum weiches Kaschmir bei winzigen Stammzellen beginnt
Kaschmirpullover fühlen sich luxuriös an, weil die Fasern außerordentlich fein, weich und warm sind. Hinter jedem Kaschmirfaden spielt sich jedoch ein mikroskopisches Drama in der Haut von Ziegen ab. Diese Studie untersucht die Stammzellen, die Kaschmirfasern erzeugen, sowie die chemischen „Schalter“ auf ihrer DNA, die ihnen sagen, wann sie aktiv werden, arbeiten oder ruhen sollen. Indem die Forschenden diese Schalter im gesamten Ziegen-Genom kartierten, erstellten sie einen Referenzatlas, der Züchtern, Biologen und Textilherstellern helfen könnte, die Kaschmirproduktion zu verstehen — und möglicherweise zu verbessern.
Vom Ziegenfell zur lebenden Faserfabrik
Kaschmir stammt aus speziellen Strukturen in der Haut, den sekundären Haarfollikeln, die wie winzige Fabriken feine Unterwolle produzieren. Jeder Follikel verfügt über ein Reservoir von Stammzellen, die wiederholt neue Fasern im saisonalen Zyklus regenerieren können, ähnlich einem Feld, das jedes Jahr neu bepflanzt wird. Bei Kaschmirziegen sind diese Zyklen stark an die Umwelt gekoppelt: Die Fasern beginnen im frühen Frühling zu wachsen und erreichen bis zum Herbst ihre volle Produktion. Das Team konzentrierte sich auf die Stammzellen dieser Follikel zu zwei wichtigen Zeitpunkten dieses Zyklus — dem frühen Wachstum und dem mittleren Wachstum — um zu sehen, wie sich ihre inneren Steuerungsmechanismen im Laufe der Zeit verändern.
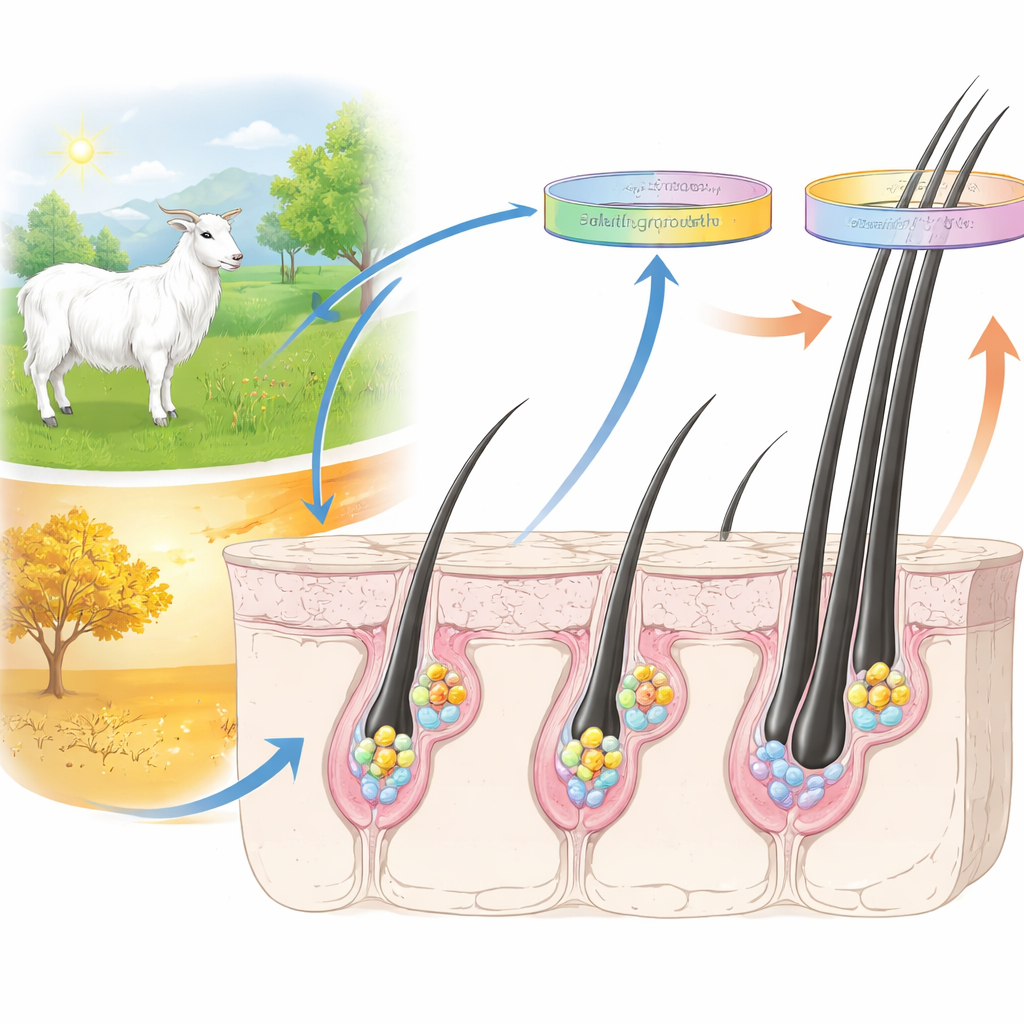
Chemische Markierungen auf der DNA lesen
Die Forschenden interessierten sich für „epigenetische“ Markierungen — kleine chemische Anhängsel an Proteinen, die die DNA verpacken. Diese Markierungen verändern den genetischen Code selbst nicht, beeinflussen aber stark, welche Gene an- oder ausgeschaltet werden, ähnlich Haftzetteln in einem Buch mit der Aufschrift „jetzt lesen“ oder „dieses Kapitel überspringen“. Das Team untersuchte vier spezifische Markierungen an Histonproteinen, die dafür bekannt sind, mit aktiven Genen, stillgelegten Genen oder Genkörpern in Nutzung verbunden zu sein. Sie verwendeten eine Methode namens ChIP-seq, um DNA-Regionen mit jeder Markierung zu isolieren und sequenzierten diese über das gesamte Ziegen-Genom — dabei entstanden Millionen von Reads pro Probe und eine detaillierte Karte der Positionen dieser Markierungen.
Verknüpfung epigenetischer Muster mit Genaktivität
Um zu verstehen, wie diese chemischen Tags die Arbeit der Stammzellen tatsächlich beeinflussen, maßen die Wissenschaftlerinnen und Wissenschaftler zusätzlich, welche Gene in denselben Zellen aktiv abgelesen wurden, mithilfe von RNA-Sequenzierung. Sie kombinierten dann die beiden Datentypen und verglichen, wie das Vorhandensein oder Fehlen jeder Histonmarkierung in der Nähe von Genstartpunkten mit Änderungen der Genaktivität zwischen frühem und mittlerem Wachstum korrelierte. Regionen mit Markierungen, die üblicherweise mit aktiven Genen assoziiert werden, lagen tendenziell in der Nähe stärker exprimierter Gene, während Markierungen, die mit Genstilllegung verbunden sind, das entgegengesetzte Muster zeigten. Mit Hilfe rechnerischer Werkzeuge gruppierten sie Genomregionen in aktive, bereitstehende (poised) oder reprimierte Zustände und verfolgten, wie sich diese Zustände mit dem Fortschreiten des Kaschmirwachstums verschoben.
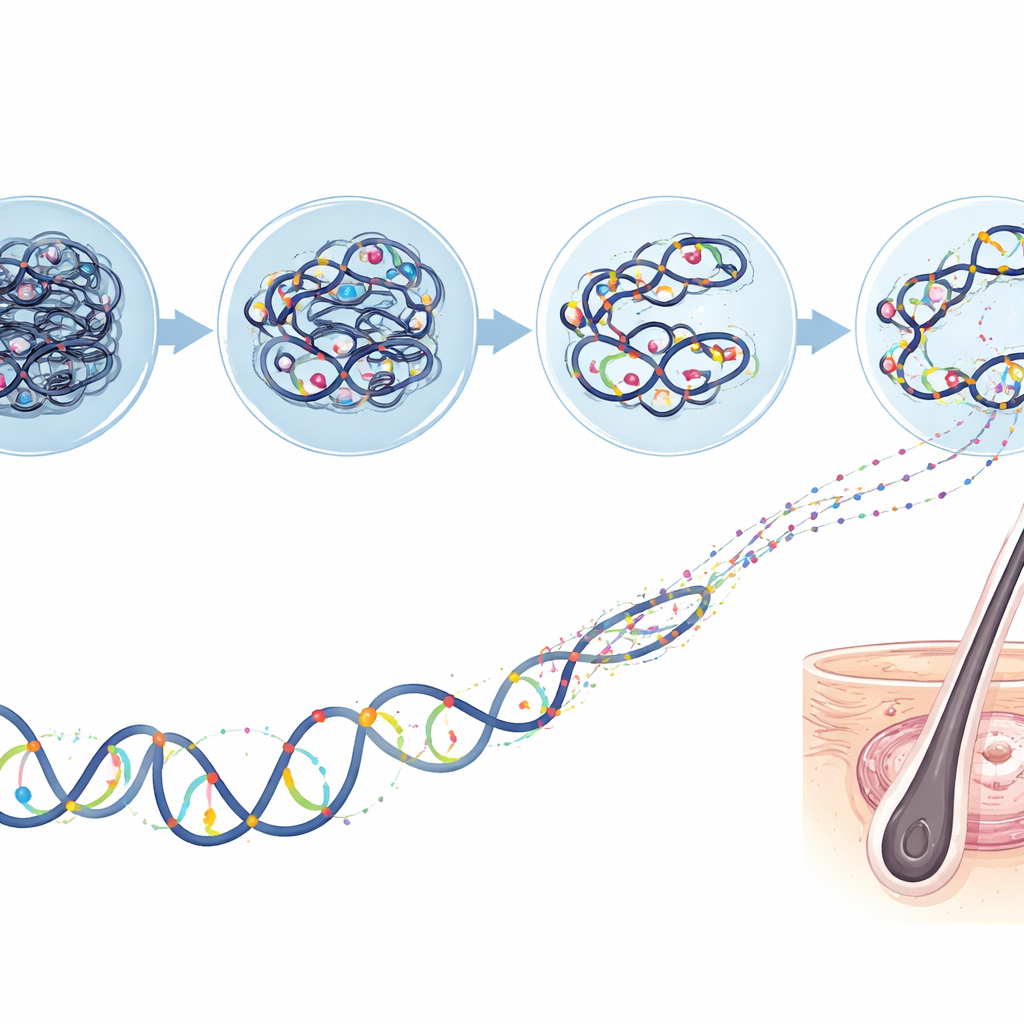
Sorgfältige Kontrollen für verlässliche Daten
Da diese Arbeit als gemeinsame Ressource für andere Forschende gedacht ist, widmeten die Autorinnen und Autoren bedeutende Anstrengungen der Qualitätskontrolle. Sie kultivierten Stammzellen von sorgfältig ausgewählten männlichen und weiblichen Ziegen, überprüften Identität und Reinheit dieser Zellen mit spezifischen Markern und stellten sicher, dass die extrahierte RNA und DNA von sehr hoher Qualität war. Anschließend prüften sie, dass wiederholte Experimente nahezu dieselben Ergebnisse lieferten und zeigten damit eine starke Übereinstimmung zwischen Proben verschiedener Tiere. Die Muster der Histonmarkierungen um Genstartseiten und bei bekannten haarrelevanten Genen verhielten sich wie erwartet, was biologische Zuverlässigkeit dafür lieferte, dass die erzeugten Karten tatsächlich widerspiegeln, wie Kaschmirstammzellen reguliert werden.
Was das für Kaschmir und darüber hinaus bedeutet
Für Nicht-Fachleute lautet die Kernbotschaft, dass das Kaschmirwachstum nicht allein durch Gene gesteuert wird, sondern durch eine komplexe Schicht chemischer Markierungen, die mitentscheidet, wann diese Gene aktiv werden. Diese Arbeit schlägt kein einzelnes Wundergen für besseren Kaschmir vor; stattdessen bietet sie einen hochauflösenden Atlas der Schalter, die Stammzellen durch die Kaschmirwachstumsphase steuern. Indem die Forschenden alle Roh- und Verarbeitungsdaten öffentlich zugänglich machen, schaffen sie eine Grundlage für künftige Arbeiten zur Verbesserung von Faserertrag und -qualität, zur Untersuchung, wie Umwelt und Zucht diese epigenetischen Muster formen, und zur Anwendung ähnlicher Ansätze auf andere Tiere und sogar die menschliche Haarbiologie.
Zitation: Liang, X., Liu, B., Liu, Y. et al. Epigenetic and transcriptional profiling of secondary hair follicle stem cells during cashmere growth. Sci Data 13, 592 (2026). https://doi.org/10.1038/s41597-026-06972-3
Schlüsselwörter: Kaschmir, Haarfollikel-Stammzellen, Epigenetik, Histonmodifikation, RNA-Sequenzierung