Clear Sky Science · fr
Les mutations tumorales prédisent la résistance aux thérapies ciblées anti-HER2 dans le cancer du sein HER2-positif primaire
Pourquoi certains tumeurs mammaires refusent de céder
Pour de nombreuses personnes atteintes d’une forme agressive de cancer du sein dite HER2‑positive, les médicaments modernes ciblant précisément la protéine HER2 ont transformé le pronostic. Pourtant, les cliniciens observent toujours un phénomène déroutant : certaines tumeurs disparaissent avant la chirurgie, tandis que d’autres restent pratiquement inchangées malgré le même traitement puissant. Cette étude posait une question simple mais cruciale : de petites altérations de l’ADN tumorale peuvent‑elles aider à expliquer qui répond et qui ne répond pas ?
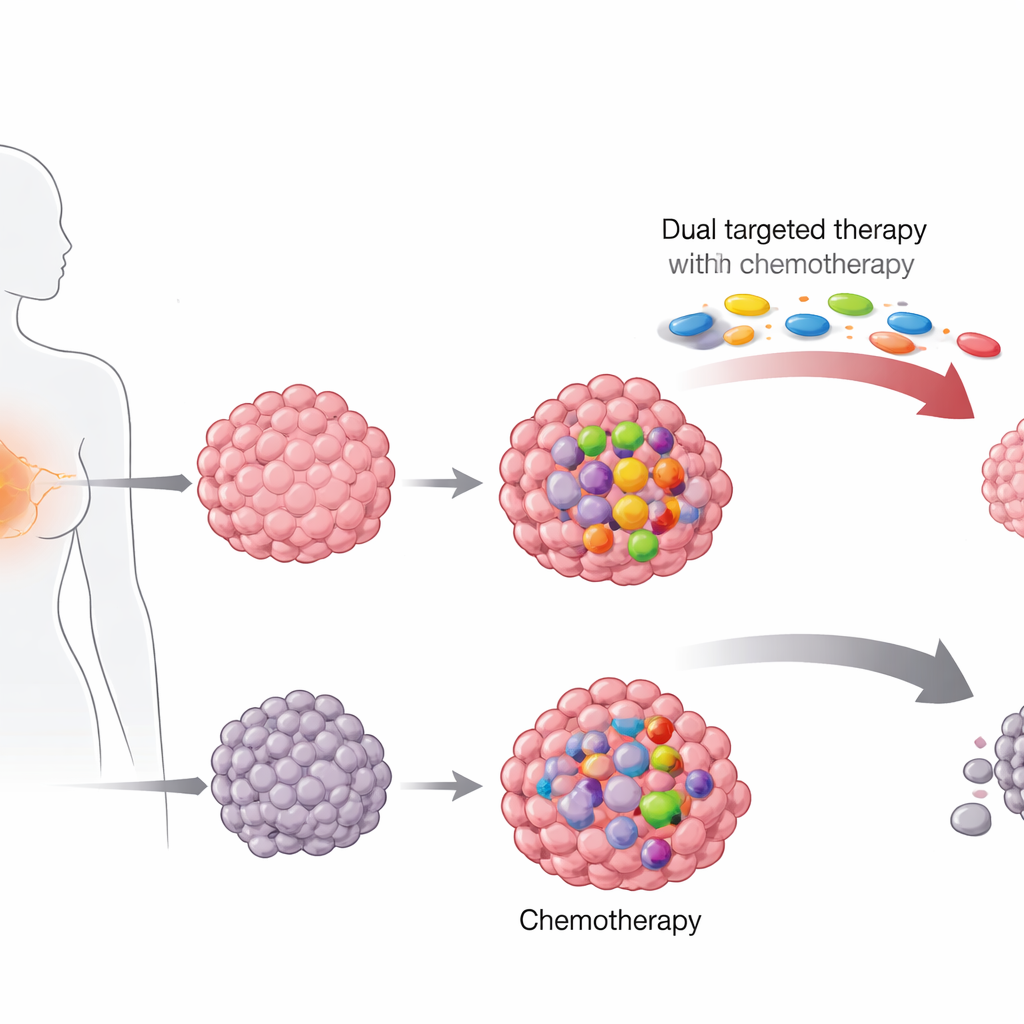
Observer les tumeurs pour y chercher des indices cachés
Les chercheurs ont examiné des échantillons de biopsie conservés provenant de 364 femmes atteintes d’un cancer du sein HER2‑positif ayant participé à deux grands essais thérapeutiques en Allemagne. Un essai, mené avant que les médicaments ciblant HER2 ne soient courants, testait différentes combinaisons de chimiothérapies seules. L’essai plus récent ajoutait un « double blocage » de HER2 avec deux médicaments, le trastuzumab et le pertuzumab, en plus d’une chimiothérapie comportant des taxanes et des anthracyclines. À l’aide du séquençage de nouvelle génération, l’équipe a recherché dans chaque tumeur des mutations ponctuelles dans 17 gènes souvent altérés dans le cancer du sein, en se concentrant particulièrement sur PIK3CA et TP53.
Altérations génétiques fréquentes dans la maladie HER2‑positive
Près des deux tiers des tumeurs présentaient au moins une mutation importante. Les altérations de TP53, un gène qui agit normalement comme un frein sur les cellules endommagées, étaient les plus fréquentes, retrouvées dans presque la moitié des cancers. Les mutations de PIK3CA, qui activent une voie intracellulaire favorisant la croissance, apparaissaient dans environ un quart des tumeurs. Une petite fraction présentait également des mutations dans des gènes liés à une autre voie de signalisation majeure, la voie MAPK. De nombreuses tumeurs portaient plus d’une altération, et les changements de PIK3CA coexistaient souvent avec des mutations de TP53 ou liées à MAPK, suggérant la superposition de plusieurs avantages de croissance au sein d’un même cancer.
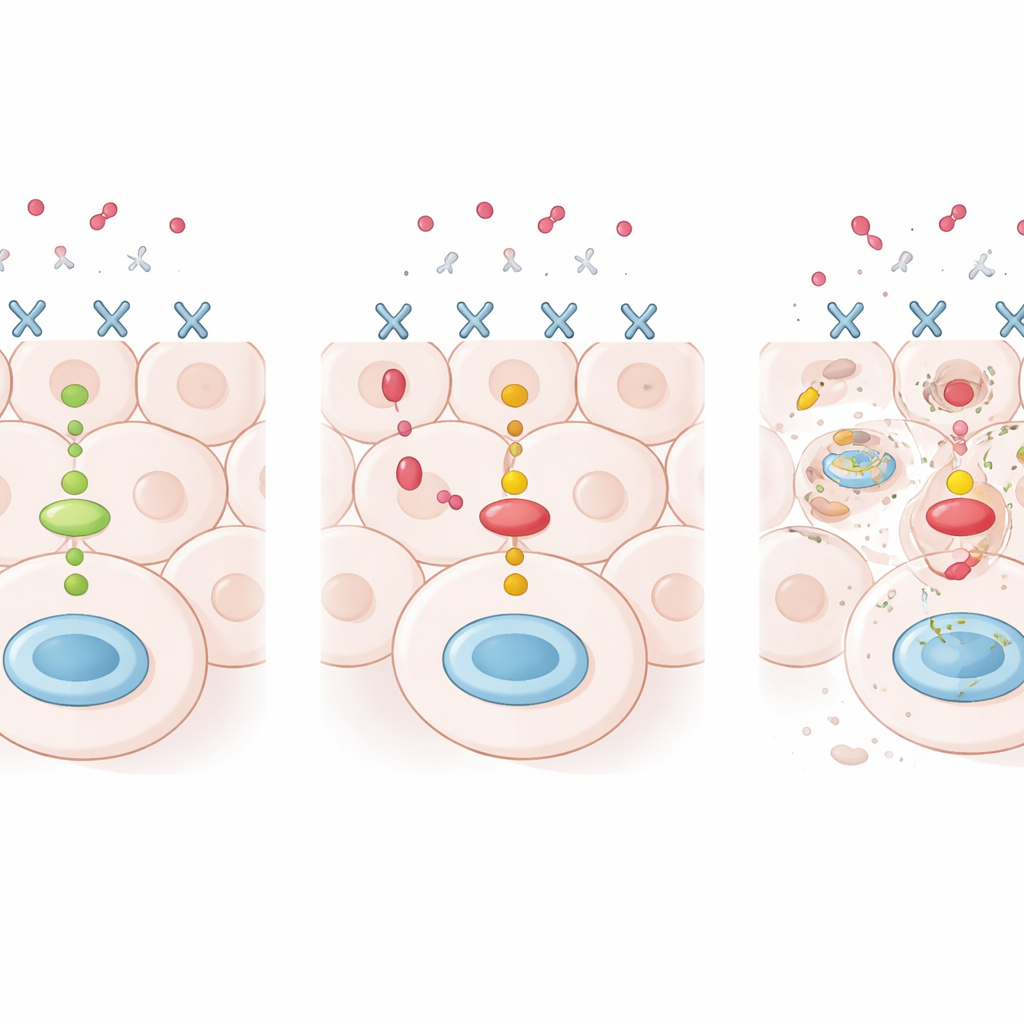
Quelles mutations importent pour la réponse au traitement ?
L’équipe a ensuite comparé ces résultats génétiques avec la mesure dans laquelle chaque tumeur avait disparu après la thérapie, un repère connu sous le nom de réponse pathologique complète. Dans l’essai plus récent qui utilisait le double blocage de HER2, les patientes dont les tumeurs ne portaient pas de mutations PIK3CA étaient beaucoup plus susceptibles d’obtenir cette réponse profonde que celles dont les tumeurs portaient la mutation. Environ deux tiers des femmes dont les tumeurs étaient PIK3CA‑normales n’avaient plus de cancer au moment de la chirurgie, contre moins de la moitié chez celles dont la maladie portait une mutation de PIK3CA. Cet écart persistait même après ajustement pour des facteurs tels que la taille de la tumeur, le statut des récepteurs hormonaux et le taux de prolifération cellulaire. En revanche, les mutations de TP53 et celles liées à MAPK n’ont pas montré de lien significatif avec le succès du traitement.
Indices fournis par différentes bases de chimiothérapie
Le tableau s’est précisé lorsque les chercheurs ont examiné des agents chimiothérapeutiques spécifiques. Dans l’essai à double blocage, les patientes étaient réparties au hasard pour recevoir soit le paclitaxel standard soit une formulation plus concentrée appelée nab‑paclitaxel avant la chirurgie. Parmi les femmes traitées par nab‑paclitaxel, les mutations PIK3CA étaient fortement associées à une mauvaise élimination tumorale : moins de quatre tumeurs mutées sur dix avaient disparu, contre plus de sept sur dix pour les tumeurs sans la mutation. Cette différence a presque disparu dans le groupe paclitaxel, suggérant que l’action à haute dose et ciblant la division cellulaire du nab‑paclitaxel pourrait involontairement favoriser la survie des cellules porteuses de la mutation PIK3CA. Fait marquant, dans l’essai plus ancien où les patientes recevaient une chimiothérapie seule sans médicaments ciblant HER2, le statut PIK3CA n’influençait pas significativement la réponse, ce qui suggère que l’impact principal de la mutation émerge lorsque le signal HER2 est bloqué.
Ce que ces découvertes signifient pour les patientes
Pour les personnes confrontées à un cancer du sein HER2‑positif, l’étude offre une explication plus claire de la raison pour laquelle certaines tumeurs résistent même à des traitements modernes intensifs. Les tumeurs porteuses de mutations PIK3CA semblent capables de contourner le blocage de HER2 en activant un moteur de croissance parallèle à l’intérieur de la cellule, et elles peuvent aussi mieux résister à certaines formes de chimiothérapie. Bien que l’étude n’ait pas eu la taille nécessaire pour démontrer des différences majeures de survie à long terme, ses résultats soutiennent fortement l’utilisation du statut PIK3CA comme guide lors de la planification thérapeutique. À l’avenir, combiner les médicaments ciblant HER2 avec des traitements qui inhibent la voie PIK3CA — ou éviter le nab‑paclitaxel dans les tumeurs porteuses de la mutation — pourrait aider à transformer davantage de réponses partielles en réponses complètes, donnant aux patientes une meilleure chance que leur cancer ne récidive pas.
Citation: Van Mackelenbergh, M.T., Pfarr, N., Weber, K. et al. Tumor mutations predict HER2-targeted therapy resistance in primary HER2-positive breast cancer. npj Breast Cancer 12, 59 (2026). https://doi.org/10.1038/s41523-026-00948-7
Mots-clés: cancer du sein HER2-positif, mutation PIK3CA, résistance aux thérapies ciblées, chimiothérapie néoadjuvante, génomique tumorale