Clear Sky Science · de
Tumormutationen sagen Resistenz gegen HER2‑gerichtete Therapie beim primären HER2‑positiven Brustkrebs voraus
Warum einige Brusttumoren sich nicht zurückziehen
Für viele Menschen mit einer aggressiven Form von Brustkrebs, der als HER2‑positiv bezeichnet wird, haben moderne Medikamente, die das HER2‑Protein gezielt angreifen, die Prognose deutlich verbessert. Dennoch beobachten Ärztinnen und Ärzte ein rätselhaftes Muster: Manche Tumoren schwinden vor der Operation vollständig, andere reagieren kaum, obwohl dieselbe starke Behandlung angewendet wurde. Diese Studie stellte eine einfache, aber entscheidende Frage — können winzige DNA‑Veränderungen im Tumor erklären, wer anspricht und wer nicht?
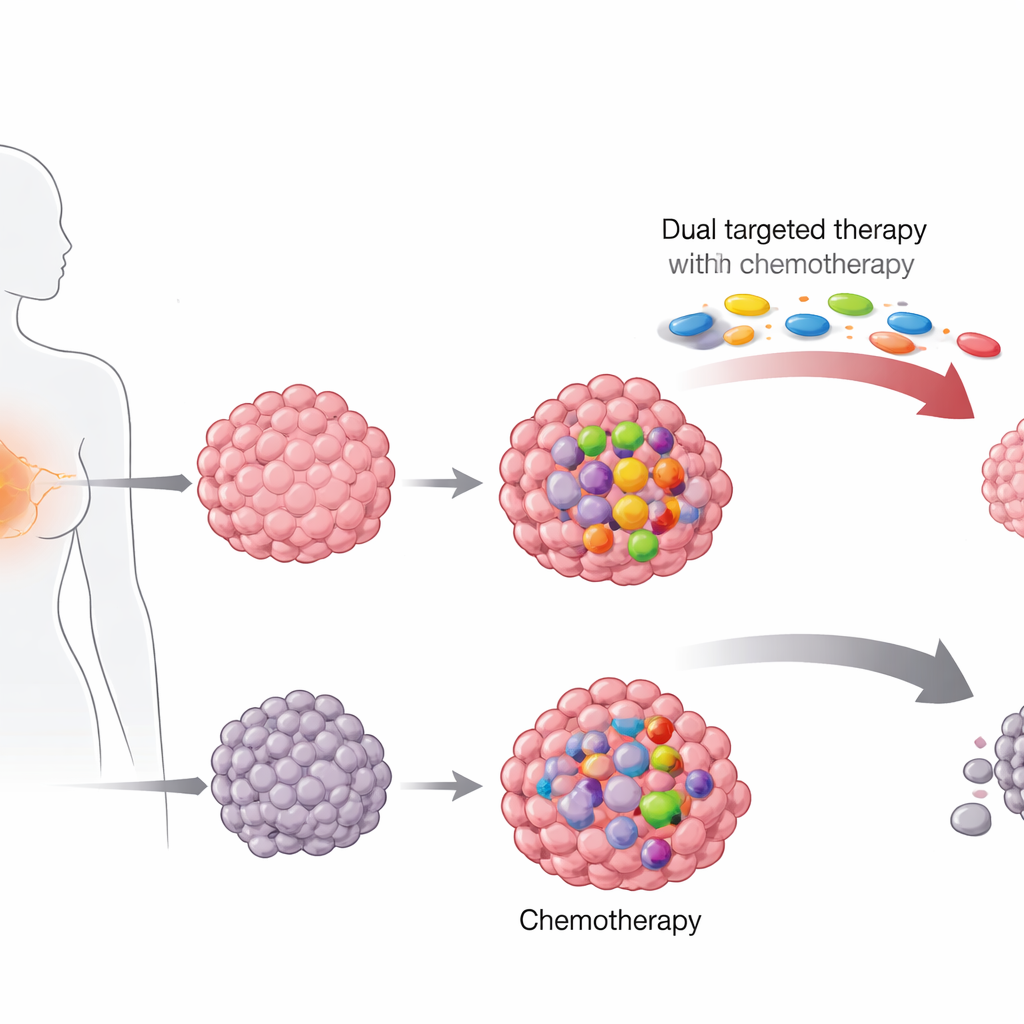
Im Tumor nach verborgenen Hinweisen suchen
Die Forschenden untersuchten eingelagertes Biopsiematerial von 364 Frauen mit HER2‑positivem Brustkrebs, die an zwei großen Behandlungsstudien in Deutschland teilgenommen hatten. Eine Studie, durchgeführt bevor HER2‑gerichtete Medikamente weit verbreitet waren, prüfte verschiedene Chemotherapie‑Kombinationen allein. Die neuere Studie fügte zur Chemotherapie mit Taxanen und Anthrazykline eine „duale Blockade“ von HER2 mittels zweier Wirkstoffe, Trastuzumab und Pertuzumab, hinzu. Mit Next‑Generation‑Sequencing durchsuchte das Team jeden Tumor nach Hot‑Spot‑Mutationen in 17 Genen, die bei Brustkrebs häufig verändert sind, mit besonderem Fokus auf PIK3CA und TP53.
Häufige genetische Veränderungen beim HER2‑positiven Tumor
Fast zwei Drittel der Tumoren wiesen mindestens eine bedeutsame Mutation auf. Veränderungen im TP53‑Gen, das normalerweise als Bremse für beschädigte Zellen fungiert, waren am häufigsten und wurden in fast der Hälfte der Fälle gefunden. Mutationen in PIK3CA, die eine wachstumsfördernde Signalkaskade innerhalb der Zelle aktivieren, traten in etwa einem Viertel der Tumoren auf. Ein kleiner Anteil zeigte Mutationen in Genen, die mit einer weiteren wichtigen Signalroute, dem MAPK‑Weg, verknüpft sind. Viele Tumoren trugen mehr als eine Veränderung; PIK3CA‑Mutationen traten häufig gemeinsam mit TP53‑ oder MAPK‑assoziierten Veränderungen auf, was darauf hindeutet, dass mehrere Wachstums‑Vorteile im selben Tumor überlagert sind.
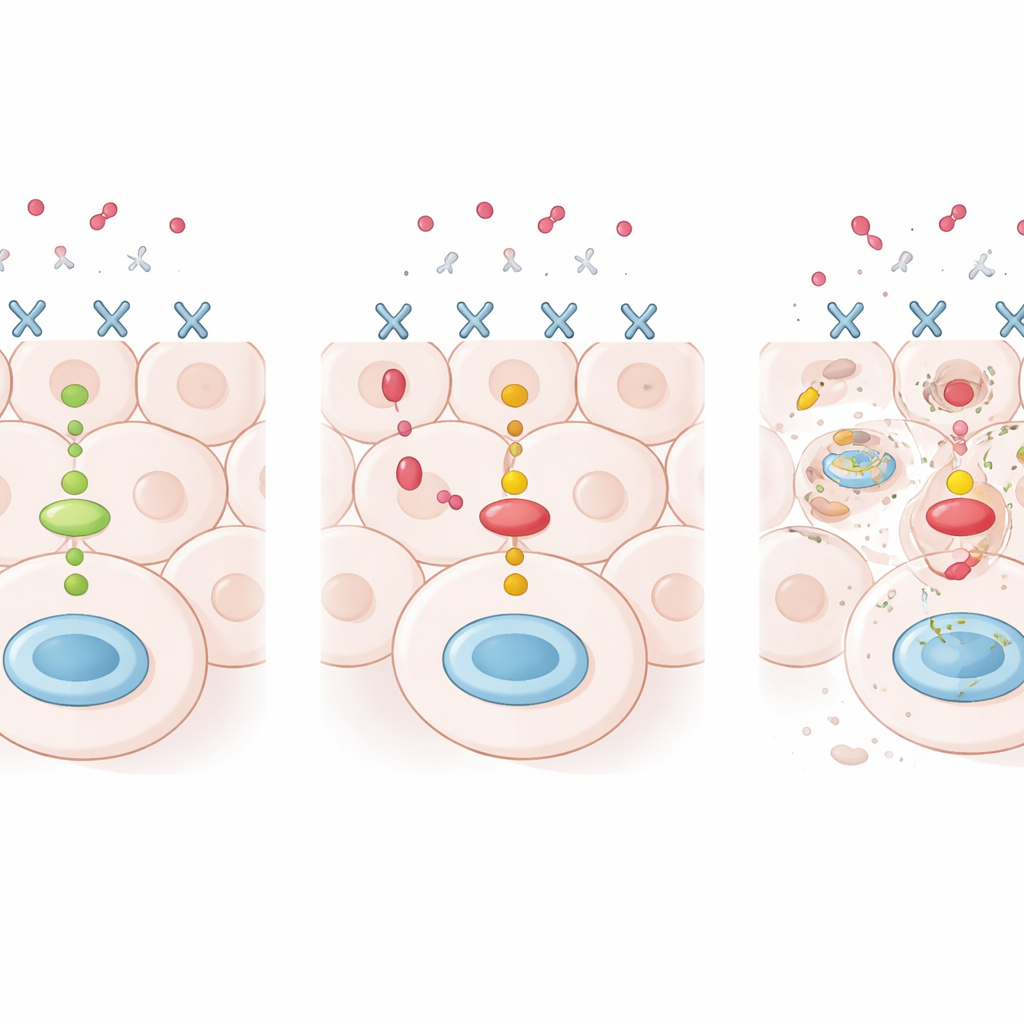
Welche Mutationen sind für die Therapieantwort relevant?
Das Team verglich diese genetischen Befunde mit dem Ausmaß, in dem jeder Tumor nach der Therapie verschwunden war — ein Maß, das als pathologisches Komplettansprechen (pathological complete response) bekannt ist. In der neueren Studie mit dualer HER2‑Blockade hatten Patientinnen, deren Tumoren keine PIK3CA‑Mutationen aufwiesen, deutlich höhere Chancen auf dieses tiefe Ansprechen als diejenigen mit einer PIK3CA‑Mutation. Etwa zwei Drittel der Frauen mit PIK3CA‑normalen Tumoren hatten bei der Operation keinen nachweisbaren Krebs mehr, verglichen mit weniger als der Hälfte derer mit PIK3CA‑mutiertem Tumor. Dieser Unterschied blieb bestehen, selbst nachdem Faktoren wie Tumorgröße, Hormonrezeptorstatus und Zellteilungsrate berücksichtigt wurden. Im Gegensatz dazu zeigten TP53‑ und MAPK‑bezogene Mutationen keinen relevanten Zusammenhang mit dem Therapieerfolg.
Hinweise aus verschiedenen Chemotherapie‑Grundlagen
Das Bild wurde noch deutlicher, als die Forschenden spezifische Chemotherapeutika betrachteten. In der Studie mit dualer Blockade wurden die Patientinnen randomisiert, entweder Standard‑Paclitaxel oder eine konzentriertere Formulierung namens nab‑Paclitaxel vor der Operation zu erhalten. Unter den mit nab‑Paclitaxel behandelten Frauen hing das Ausbleiben des Tumors stark vom PIK3CA‑Status ab: Weniger als vier von zehn Tumoren mit Mutation verschwanden, verglichen mit mehr als sieben von zehn ohne Mutation. Dieser Unterschied verschwand nahezu in der Paclitaxel‑Gruppe, was nahelegt, dass die hochdosierte, auf Zellteilung zielende Wirkung von nab‑Paclitaxel möglicherweise unbeabsichtigt das Überleben von PIK3CA‑mutierten Zellen begünstigt. Auffällig war, dass in der älteren Studie, in der Patientinnen nur eine Chemotherapie ohne HER2‑gerichtete Medikamente erhielten, der PIK3CA‑Status die Antwort nicht wesentlich beeinflusste — was darauf hindeutet, dass die Hauptwirkung der Mutation erst dann sichtbar wird, wenn das HER2‑Signal blockiert ist.
Was diese Ergebnisse für Patientinnen und Patienten bedeuten
Für Betroffene mit HER2‑positivem Brustkrebs liefert die Studie eine klarere Erklärung dafür, warum einige Tumoren selbst auf intensive, moderne Therapien resistent sind. Tumoren mit PIK3CA‑Mutationen scheinen in der Lage zu sein, die HER2‑Blockade zu umgehen, indem sie eine parallele Wachstumsantriebsachse innerhalb der Zelle aktivieren, und sie könnten bestimmten Formen der Chemotherapie better widerstehen. Obwohl die Studie nicht groß genug war, um eindeutige Unterschiede in der Langzeitüberlebensrate zu beweisen, stützen die Ergebnisse stark die Verwendung des PIK3CA‑Status als Orientierungshilfe bei der Therapieplanung. Zukünftig könnte die Kombination von HER2‑gerichteten Medikamenten mit Substanzen, die den PIK3CA‑Weg ausschalten — oder das Vermeiden von nab‑Paclitaxel bei mutationstragenden Tumoren — dazu beitragen, mehr partielle Ansprechen in komplette Antworten zu verwandeln und den Betroffenen bessere Chancen zu geben, dass ihr Krebs nicht zurückkehrt.
Zitation: Van Mackelenbergh, M.T., Pfarr, N., Weber, K. et al. Tumor mutations predict HER2-targeted therapy resistance in primary HER2-positive breast cancer. npj Breast Cancer 12, 59 (2026). https://doi.org/10.1038/s41523-026-00948-7
Schlüsselwörter: HER2‑positiver Brustkrebs, PIK3CA‑Mutation, Resistenz gegen gezielte Therapie, neoadjuvante Chemotherapie, Tumor‑Genomik