Clear Sky Science · fr
Les interneurones somatostatine du cortex moteur modulent de façon adaptative la structure des séquences d’action
Pourquoi le timing de nos mouvements compte
Des actions quotidiennes comme taper au clavier, jouer du piano ou verser du café paraissent automatiques, mais elles reposent sur la capacité du cerveau à enchaîner de nombreux micro-mouvements en séquences fluides et efficaces. Cette étude pose une question apparemment simple : comment le cortex moteur réorganise-t-il ces séquences d’actions lorsque nous nous entraînons, accélérons ou changeons les règles ? En observant un groupe particulier de cellules nerveuses inhibitrices chez la souris pendant qu’elles apprennent différentes tâches d’appui sur un levier, les chercheurs montrent que ces neurones aident à ajuster en temps réel le rythme et la structure des actions complexes.
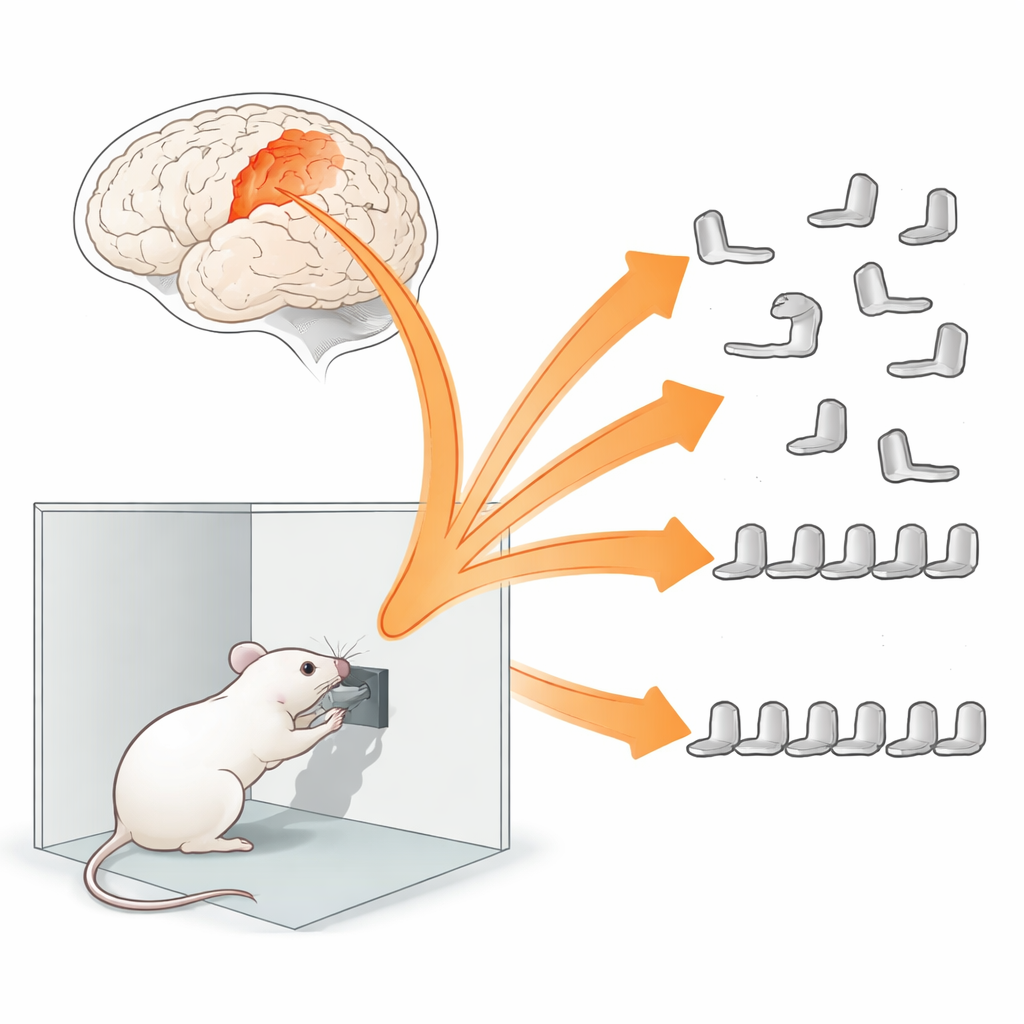
Du mouvement isolé aux actions chaînées
Pour étudier comment se construisent les séquences de mouvements, l’équipe a entraîné des souris en liberté à appuyer sur un levier pour obtenir de la nourriture. Au départ, la tâche était simple : une pression pour une récompense. Puis, les animaux ont dû appuyer quatre fois pour chaque récompense, et finalement condenser ces quatre pressions dans une fenêtre temporelle étroite, formant une séquence rapide et fortement synchronisée. Pendant l’apprentissage, les scientifiques ont utilisé de minuscules microscopes pour enregistrer des signaux calciques — un substitut de l’activité électrique — provenant de neurones spécifiques dans le cortex moteur primaire, la région qui envoie les commandes aux muscles. Ils se sont concentrés sur les interneurones somatostatine, des cellules qui atténuent l’activité des neurones excitateurs voisins et qui seraient impliquées dans la régulation de la plasticité liée à l’apprentissage.
Des cellules spécialisées pour façonner les séquences
Pendant les premières séances sur la tâche simple à pression unique, les interneurones somatostatine des couches profondes du cortex moteur déchargeaient de façon fortement synchronisée et liée à l’action : leur activité augmentait de manière fiable autour de chaque pression. À l’inverse, les neurones pyramidaux voisins — les principales cellules de sortie — s’activaient selon un schéma plus étagé et séquentiel. À mesure que le comportement à pression unique devenait bien appris et routinier après des semaines d’entraînement, les réponses des cellules somatostatine diminuaient et leur corrélation devenait plus faible, alors même que leur capacité globale à générer des signaux calciques restait intacte. Cela suggère que, lorsqu’une tâche devient automatique et immuable, ces interneurones se retirent en grande partie du contrôle instantané de l’action.
Quand les règles changent, le réseau s’adapte
Le tableau a changé radicalement quand les exigences de la tâche se sont renforcées. Lorsque les souris devaient produire des séquences rapides de quatre pressions dans des limites de temps strictes, elles ont réorganisé leur comportement : les pressions sont devenues plus rapides, plus regroupées et plus « efficaces », avec moins de pressions inutiles ne rapportant pas de récompense. En parallèle, l’activité des interneurones somatostatine ne s’est pas estompée ; au contraire, elle s’est redistribuée dans le temps et renforcée. Les chercheurs ont identifié deux sous-schémas distincts dans ces cellules. Un groupe montrait une brève poussée immédiate autour de l’initiation de la séquence, tandis qu’un autre groupe se relâchait plus tard, le timing de leurs pics suivant la durée de chaque séquence particulière. Les séquences plus efficaces et bien structurées s’accompagnaient de signaux somatostatine plus larges et plus soutenus, et différentes « classes » de séquences avec des cinématiques distinctes pouvaient être distinguées uniquement à partir des profils d’activité de ces neurones.
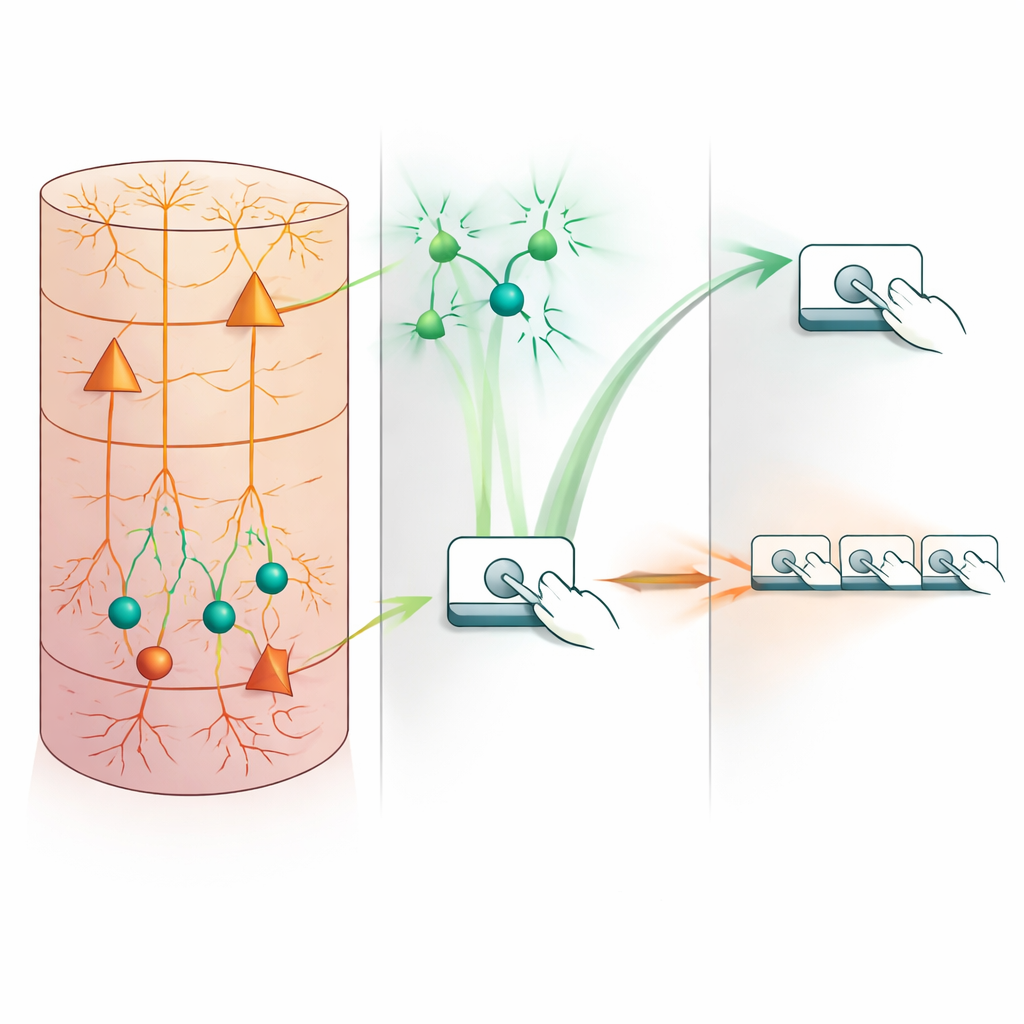
Désactiver les freins perturbe le rythme
La corrélation seule n’établit pas la causalité, les auteurs ont donc demandé ce qui se passe quand les interneurones somatostatine sont délibérément inhibés. En utilisant des outils chimiogénétiques et l’optogénétique en boucle fermée, ils ont atténué sélectivement ces cellules dans le cortex moteur pendant que les souris effectuaient les séquences rapides contraintes par le temps. Dans les deux cas, réduire l’activité somatostatine a fait que les animaux appuyaient plus souvent au sein de chaque séquence mais de manière moins organisée : les pressions s’étalaient davantage dans le temps, les séquences efficaces à haute vitesse devenaient plus rares, et les séquences « incomplètes » qui ne respectaient pas les contraintes temporelles se multipliaient. Il est important de noter que le mouvement global ou la motivation n’étaient pas simplement réduits ; en fait, le taux d’appuis pouvait augmenter, mais ces appuis supplémentaires ne rapportaient pas plus de récompenses. Cela indique une perturbation spécifique de l’organisation temporelle plutôt qu’une perte d’élan ou de force.
Ce que cela implique pour notre façon de bouger
Pris ensemble, ces résultats suggèrent que les interneurones somatostatine des couches profondes du cortex moteur font plus que moduler passivement l’activité : ils contribuent à sculpter le timing et la structure des séquences d’actions complexes, en particulier lorsque les tâches exigent vitesse, précision ou réorganisation flexible. Lorsqu’un mouvement est simple et bien rodé, leur contrôle détaillé peut se relâcher. Mais lorsque le cerveau doit comprimer des actions dans des paquets serrés ou adapter des séquences à de nouvelles règles, ces cellules se réactivent pour affiner le moment où les séquences démarrent, leur durée et l’efficacité avec laquelle elles atteignent l’objectif. Comprendre ce « contrôle temporel » au niveau du circuit pourrait à terme inspirer de nouvelles approches pour traiter les troubles du mouvement, où les actions deviennent lentes, fragmentées ou mal séquencées, en ciblant non seulement la force des commandes motrices mais aussi les réseaux d’interneurones qui maintiennent nos mouvements serrés et efficaces.
Citation: Lee, J.O., Bariselli, S., Sitzia, G. et al. Motor cortex somatostatin interneurons adaptively shape the structure of action sequences. Nat Commun 17, 4116 (2026). https://doi.org/10.1038/s41467-026-70353-y
Mots-clés: cortex moteur, séquences d’action, interneurones inhibiteurs, apprentissage moteur, timing neuronal