Clear Sky Science · de
Somatostatin-Interneurone im motorischen Kortex formen adaptiv die Struktur von Handlungssequenzen
Warum das Timing unserer Bewegungen wichtig ist
Alltägliche Tätigkeiten wie Tippen, Klavierspielen oder Kaffee einschenken wirken mühelos, beruhen aber auf der Fähigkeit des Gehirns, viele kleine Bewegungen zu einer flüssigen, effizienten Sequenz zu verknüpfen. Diese Studie stellt eine auf den ersten Blick einfache Frage: Wie reorganisiert der motorische Kortex des Gehirns diese Handlungssequenzen, wenn wir üben, schneller werden oder die Regeln ändern? Indem die Forschenden eine spezielle Gruppe inhibitorischer Nervenzellen bei Mäusen beobachteten, während diese verschiedene Hebel-Drückaufgaben lernten, zeigen sie, dass diese Neurone das Timing und die Struktur komplexer Aktionen im laufenden Betrieb feinjustieren.
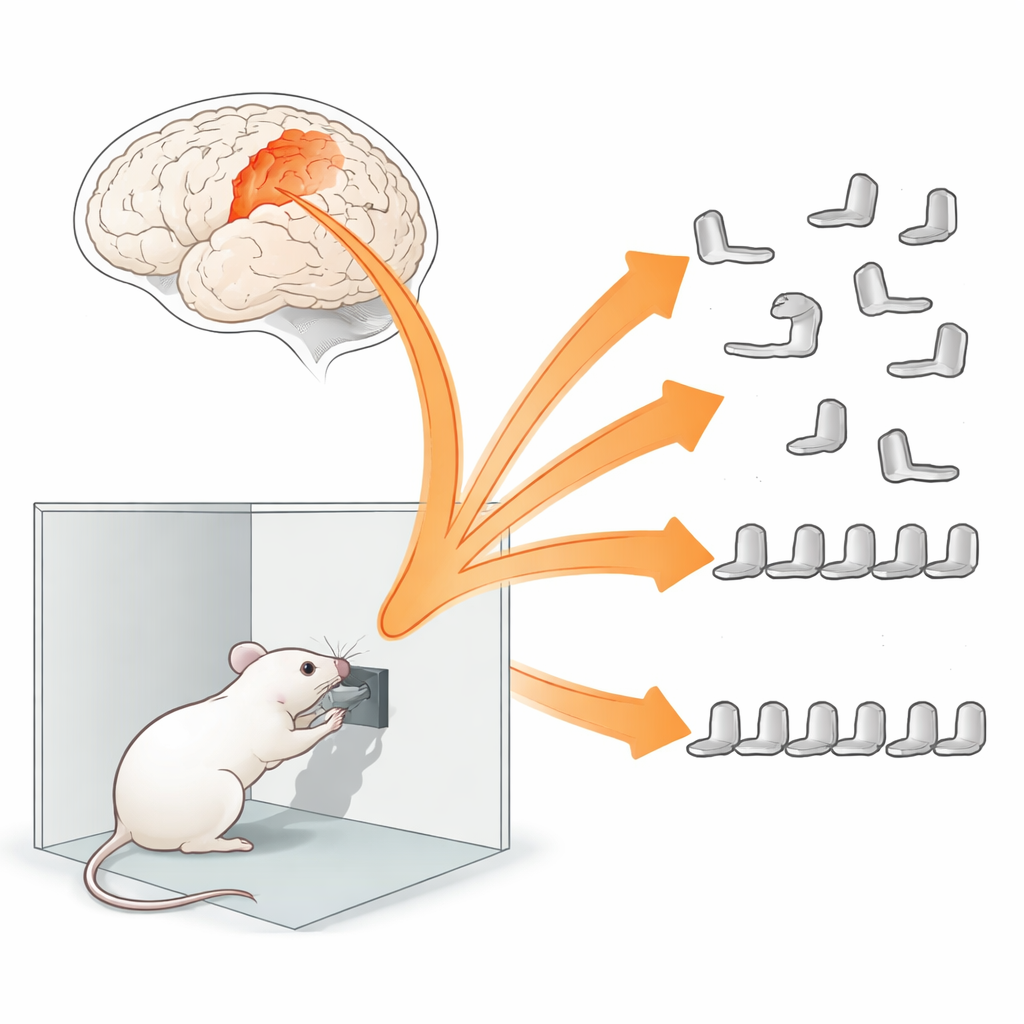
Von einzelnen Bewegungen zu verknüpften Aktionen
Um zu untersuchen, wie Bewegungssequenzen aufgebaut werden, trainierte das Team frei bewegliche Mäuse, einen Hebel für Futter zu drücken. Zunächst war die Aufgabe einfach: ein Druck pro Belohnung. Später mussten die Tiere viermal drücken, um eine Belohnung zu erhalten, und schließlich sollten diese vier Drücke in ein enges Zeitfenster gepackt werden, sodass eine schnelle, dicht getimte Sequenz entstand. Während die Mäuse lernten, nutzten die Wissenschaftler winzige Mikroskope, um Kalziumsignale — einen Proxy für elektrische Aktivität — aus bestimmten Neuronen des primären motorischen Kortex aufzuzeichnen, dem Hirnareal, das Befehle an die Muskeln sendet. Sie konzentrierten sich auf Somatostatin-Interneurone, Zellen, die die Aktivität nahegelegener exzitatorischer Neurone dämpfen und als Regulatoren lernassoziierter Plastizität gelten.
Spezialisierte Zellen zur Formung von Sequenzen
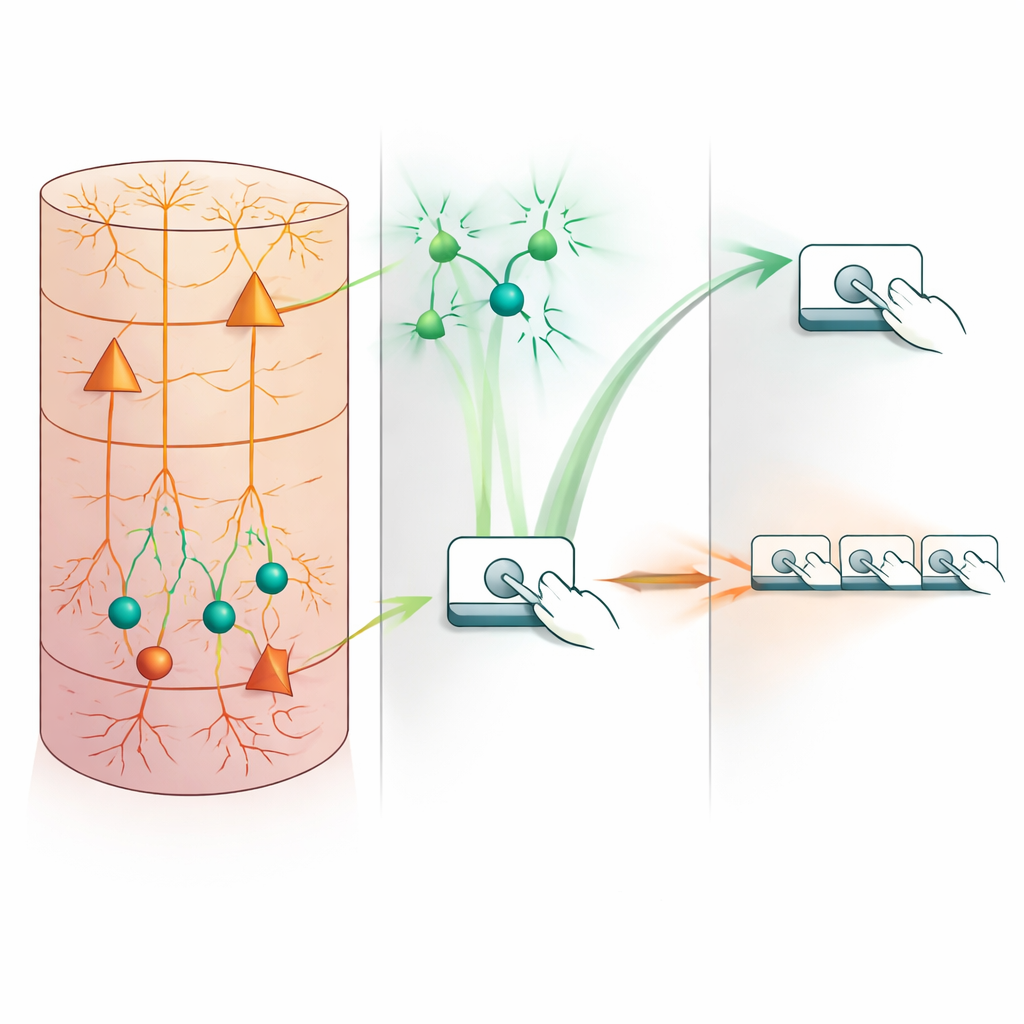
Während der frühen Trainingsphase mit der einfachen Einzeldruckaufgabe feuerten Somatostatin-Interneurone in den tieferen Schichten des motorischen Kortex hoch synchronisiert und akteursgebunden: ihre Aktivität stieg zuverlässig um die Zeit jedes Hebeldrucks herum an. Im Gegensatz dazu wurden nahegelegene Pyramidenzellen — die hauptsächlichen Ausgangszellen — in einem gestaffelteren, sequenziellen Muster aktiviert. Als sich das Einzeldruckverhalten über Wochen zur Routine entwickelte, gingen die Antworten der Somatostatin-Zellen zurück und wurden weniger korreliert, obwohl ihre generelle Fähigkeit, Kalziumsignale zu erzeugen, erhalten blieb. Das deutet darauf hin, dass diese Interneurone bei automatisierten, unveränderten Aufgaben weitgehend aus der unmittelbaren Steuerung der Aktion heraustreten.
Wenn sich die Regeln ändern, passt sich das Netzwerk an
Das Bild änderte sich dramatisch, als die Anforderungen an die Aufgabe stiegen. Als die Mäuse schnelle Vierer-Sequenzen innerhalb strikter Zeitlimits produzieren mussten, reorganisierten sie ihr Verhalten: Die Drücke wurden schneller, dichter gebündelt und „effizienter“, mit weniger verschwendeten Drücken, die keine Belohnung einbrachten. Gleichzeitig verblasste die Aktivität der Somatostatin-Interneurone nicht; stattdessen wurde sie zeitlich umverteilt und verstärkt. Die Forschenden identifizierten zwei unterscheidbare Teilmuster in diesen Zellen. Eine Gruppe zeigte einen kurzen, unmittelbaren Burst bei Sequenzbeginn, während eine andere Gruppe später feuert und deren Spitzenzeitpunkt mit der Dauer der jeweiligen Sequenz mitverschoben war. Effizientere, gut strukturierte Sequenzen gingen mit stärkeren und anhaltenderen Somatostatin-Signalen einher, und verschiedene Sequenz‑„Klassen“ mit unterschiedlicher Kinematik ließen sich allein aus den Aktivitätsprofilen dieser Neurone unterscheiden.
Die Bremsen ausschalten wirbelt das Rhythmusbild durcheinander
Korrelation allein beweist keine Ursache, daher fragten die Autoren als Nächstes, was passiert, wenn Somatostatin-Interneurone bewusst stillgelegt werden. Mithilfe chemogenetischer Werkzeuge und geschlossen‑schleifiger Optogenetik dämpften sie selektiv diese Zellen im motorischen Kortex, während die Mäuse die schnellen, zeitlich gebundenen Sequenzen ausführten. In beiden Fällen führte das Herunterregeln der Somatostatin-Aktivität dazu, dass die Tiere innerhalb jeder Sequenz häufiger drückten, jedoch weniger geordnet: Die Drücke zogen sich zeitlich auseinander, effiziente Hochgeschwindigkeitssequenzen wurden seltener, und „unvollständige“ Sequenzen, die das Zeitkriterium nicht erfüllten, traten häufiger auf. Auffällig war, dass dadurch nicht einfach die Gesamtbewegung oder Motivation vermindert wurde; tatsächlich konnten die Hebeldruckraten steigen, aber die zusätzlichen Drücke brachten keine zusätzlichen Belohnungen. Das weist auf eine spezifische Störung der zeitlichen Organisation hin und nicht auf einen Verlust von Antrieb oder Kraft.
Was das für unsere Bewegung bedeutet
Insgesamt deuten die Befunde darauf hin, dass Somatostatin-Interneurone in den tiefen Schichten des motorischen Kortex mehr tun, als Aktivität nur passiv zu modulieren: Sie helfen, das Timing und die Struktur komplexer Handlungssequenzen zu formen, insbesondere wenn Aufgaben Geschwindigkeit, Präzision oder flexible Reorganisation erfordern. Wenn eine Bewegung einfach und gut eingeübt ist, kann ihre detaillierte Kontrolle nachlassen. Braucht das Gehirn jedoch, Aktionen in kompakte Pakete zu pressen oder Sequenzen an neue Regeln anzupassen, schalten sich diese Zellen wieder ein, um fein abzustimmen, wann Sequenzen beginnen, wie lange sie dauern und wie effizient sie das Ziel erreichen. Das Verständnis dieser schaltkreisbezogenen „Timing‑Kontrolle“ könnte schließlich neue Ansätze zur Behandlung von Bewegungsstörungen informieren, bei denen Aktionen langsam, fragmentiert oder schlecht sequenziert sind, indem nicht nur die Stärke motorischer Befehle, sondern auch die Interneuron‑Netzwerke adressiert werden, die unsere Bewegungen eng und effizient organisiert halten.
Zitation: Lee, J.O., Bariselli, S., Sitzia, G. et al. Motor cortex somatostatin interneurons adaptively shape the structure of action sequences. Nat Commun 17, 4116 (2026). https://doi.org/10.1038/s41467-026-70353-y
Schlüsselwörter: motorischer Kortex, Handlungssequenzen, inhibitorische Interneurone, Bewegungslernen, neuronales Timing