Clear Sky Science · fr
Électrolyse continue durable de l’eau de mer via un catalyseur d’interface atomique et une stratégie en milieu liquide
Transformer l’eau de mer en carburant propre
Alors que le monde cherche des carburants plus propres, l’hydrogène produit à partir de l’eau avec de l’électricité renouvelable apparaît comme une option particulièrement séduisante. Mais les installations hydrogène à grande échelle utilisent généralement de l’eau douce rare, et les tentatives d’utilisation directe de l’eau de mer se heurtent à de sérieux problèmes techniques tels que l’encrassement, la corrosion et des réactions parallèles énergivores. Cette étude présente une méthode pratique pour transformer l’eau de mer ordinaire en un flux continu d’hydrogène sans désalinisation préalable, en combinant un système de filtration ingénieux et un catalyseur très efficace constitué d’atomes métalliques arrangés avec précision.
Pourquoi l’eau de mer est si difficile à utiliser
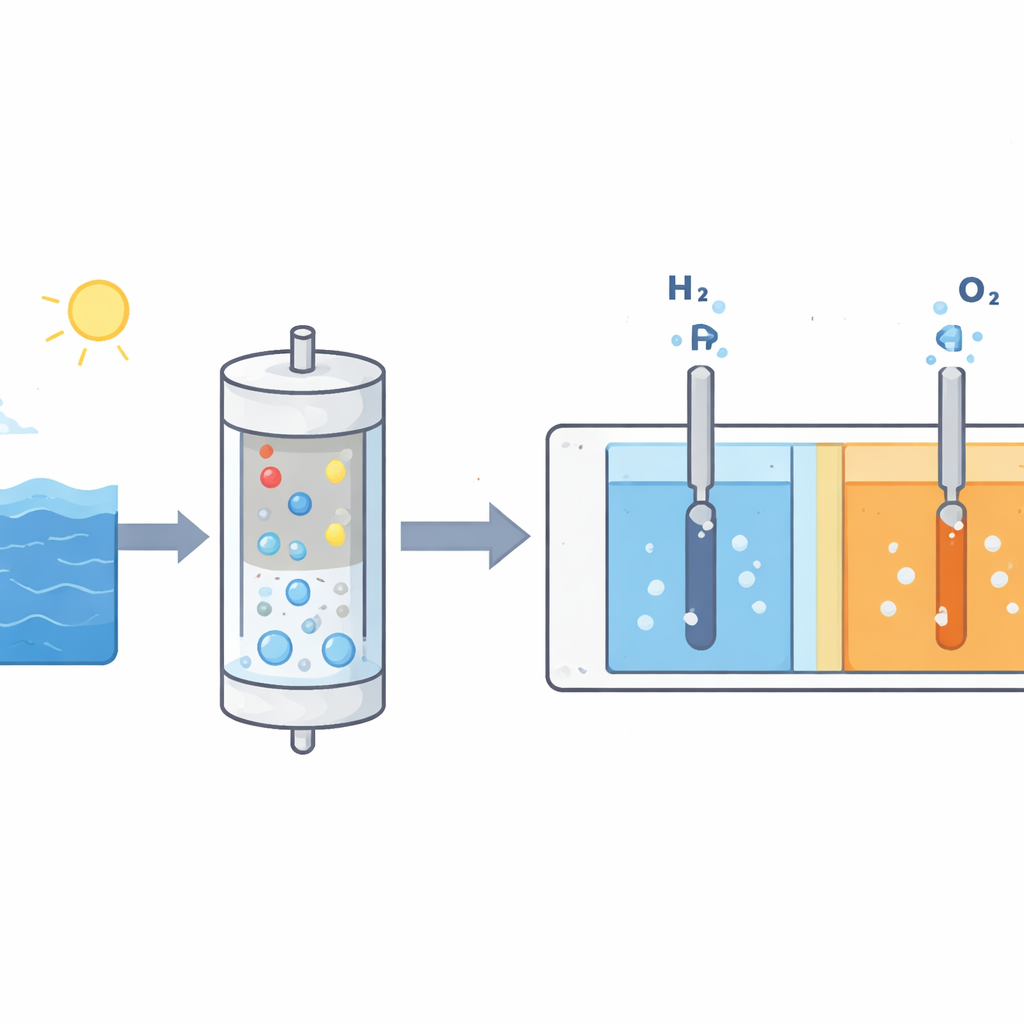
À première vue, l’eau de mer devrait être une matière première idéale pour l’hydrogène : les océans contiennent presque toute l’eau liquide de la Terre. Pourtant, l’électrolyse de l’eau de mer — séparation de l’eau en hydrogène et oxygène par électricité — se comporte très différemment de celle de l’eau pure. À l’électrode négative, l’accumulation locale d’ions hydroxyde provoque la formation de croûtes minérales tenaces de calcium et de magnésium qui encrassent la surface. À l’électrode positive, les ions chlorure peuvent s’oxyder en produits contenant du chlore qui corrodent les pièces et constituent des risques pour la sécurité. Ensemble, ces effets rendent les dispositifs existants inefficients, de courte durée et difficiles à industrialiser.
Un système en deux étapes qui ne laisse passer que l’eau
Les chercheurs ont mis au point un système qui maintient les sels gênants à distance. L’eau de mer est pompée à l’extérieur d’un module « filtre ballon », tandis qu’un électrolyte alcalin concentré circule à l’intérieur. Seules les molécules d’eau peuvent migrer à travers la mince membrane du ballon, entraînées par l’électrolyse en aval dans la cellule. Les sels et autres ions de l’eau de mer restent à l’extérieur. L’eau ainsi transférée entre ensuite dans un électrolyseur à membrane échangeuse d’anions, où elle est scindée en hydrogène et oxygène dans un environnement strictement contrôlé. Comme le débit d’eau à travers le ballon est automatiquement lié au taux de production de gaz, la concentration de l’électrolyte reste quasiment constante sans systèmes de contrôle complexes.
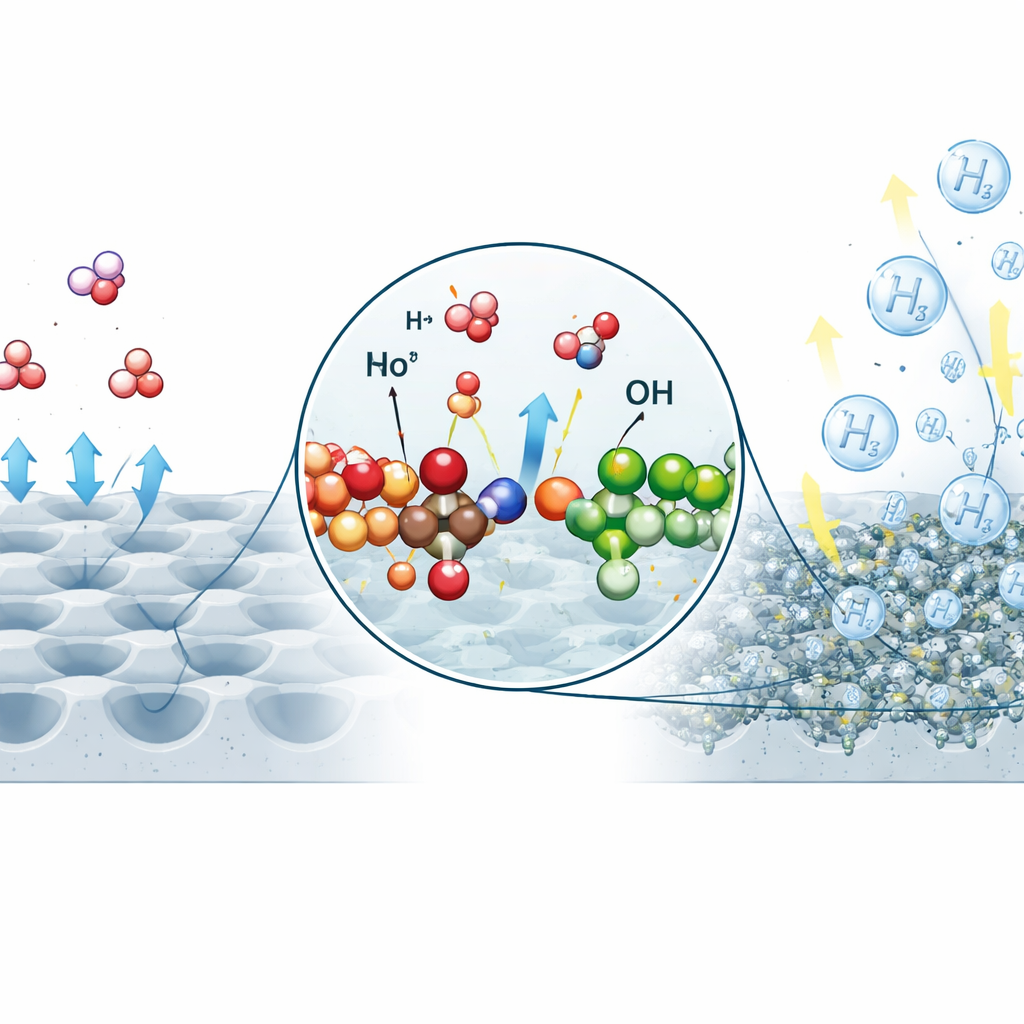
Un catalyseur construit atome par atome
Pour rendre cette eau filtrée efficace à la séparation, l’équipe a conçu un nouveau catalyseur composé d’oxydes de nickel et de molybdène arrangés à l’échelle atomique. À l’aide d’une méthode de préparation en milieu liquide, ils ont fait croître une forêt de petits puits en forme de coupe sur un support en nickel puis formé d’innombrables ponts où des atomes de nickel se relient au molybdène via des atomes d’oxygène. Ces ponts Mo–O–Ni confèrent à chaque site de réaction une double fonction : un côté aide à rompre les molécules d’eau, tandis que l’autre facilite l’assemblage et la libération de l’hydrogène. La microscopie et des mesures avancées par rayons X ont confirmé la structure souhaitée et montré que les atomes de nickel près des ponts adoptent un état électronique favorable à l’accélération de la réaction.
Des réactions rapides, un fonctionnement stable
En essais de laboratoire, le nouveau catalyseur n’a nécessité qu’une très faible surtension pour commencer à produire de l’hydrogène et a maintenu des taux de réaction élevés même à des courants de calibre industriel. Sa surface nano‑rugueuse et très mouillable permet aux bulles de gaz de se détacher rapidement, empêchant qu’elles n’empêchent l’arrivée d’eau fraîche aux sites actifs. Des expériences operando — des mesures effectuées pendant que le catalyseur fonctionne — ont révélé que la structure reste stable en conditions opératoires, et que les régions riches en Mo affaiblissent les liaisons internes de l’eau tandis que les régions riches en Ni facilitent la libération de l’hydrogène. Des simulations informatiques étayent ce tableau en montrant que les ponts atomiques réduisent les barrières énergétiques pour la séparation de l’eau et la libération d’hydrogène par rapport à des matériaux plus simples.
Un système eau de mer → hydrogène durable
Combinés, le filtre ballon et le catalyseur Mo–O–Ni ont formé un système d’électrolyse de l’eau de mer capable de fonctionner en continu à fort courant pendant des milliers d’heures. Des essais avec de l’eau de mer réelle de la mer de Bohai ont montré qu’aucune ion de sel ne s’infiltre pratiquement dans l’électrolyte, qu’aucun sous‑produit contenant du chlore n’a été détecté, et que la tension requise pour maintenir l’appareil en marche n’augmentait que faiblement avec le temps. En termes simples, l’étude démontre une voie réaliste pour transformer l’abondante eau de mer en hydrogène propre sans la désaliniser au préalable, en séparant intelligemment les sels et en ingénierie précise de la manière dont les atomes à la surface d’un catalyseur coopèrent.
Citation: Shi, Z., Shi, W., Zhang, C. et al. Sustainable continuous seawater electrolysis using atomic interface catalyst via liquid-medium strategy. Nat Commun 17, 3940 (2026). https://doi.org/10.1038/s41467-026-70234-4
Mots-clés: électrolyse de l’eau de mer, hydrogène vert, électrocatalyseur, interface nickel‑molybdène, membrane échangeuse d’anions