Clear Sky Science · de
Nachhaltige kontinuierliche Meerwasser‑Elektrolyse mit atomarem Grenzflächenkatalysator durch eine Flüssig‑Medium‑Strategie
Meerwasser in sauberen Brennstoff verwandeln
Während die Welt nach saubereren Brennstoffen sucht, ist Wasserstoff, der mit erneuerbarem Strom aus Wasser gewonnen wird, besonders attraktiv. Großtechnische Wasserstoffanlagen nutzen jedoch üblicherweise knappe Süßwasserressourcen, und der direkte Einsatz von Meerwasser stößt auf ernste technische Probleme wie Verstopfung, Korrosion und verlustreiche Nebenreaktionen. Diese Studie zeigt einen praktischen Weg, gewöhnliches Meerwasser in einen stetigen Strom von Wasserstoff zu verwandeln, ohne das Salz vorher zu entfernen, mithilfe eines raffiniert gestalteten Filtersystems und eines hocheffizienten Katalysators, der aus sorgfältig angeordneten Metallatomen aufgebaut ist.
Warum Meerwasser so schwer zu nutzen ist
Auf den ersten Blick sollte Meerwasser ein ideales Ausgangsmaterial für Wasserstoff sein: Die Ozeane enthalten fast das gesamte flüssige Wasser der Erde. Dennoch verhält sich die Meerwasser‑Elektrolyse—das Spalten von Wasser in Wasserstoff und Sauerstoff mit Strom—anders als die Elektrolyse von reinem Wasser. An der negativen Elektrode führt die lokale Anreicherung an Hydroxidionen dazu, dass gelöstes Calcium und Magnesium hartnäckige Mineralbeläge bilden, die die Oberfläche verschmutzen. An der positiven Elektrode können Chloridionen zu chlorhaltigen Chemikalien oxidiert werden, die Bauteile angreifen und Sicherheitsrisiken bergen. Zusammen machen diese Effekte bestehende Meerwasseranlagen ineffizient, kurzlebig und schwer skalierbar.
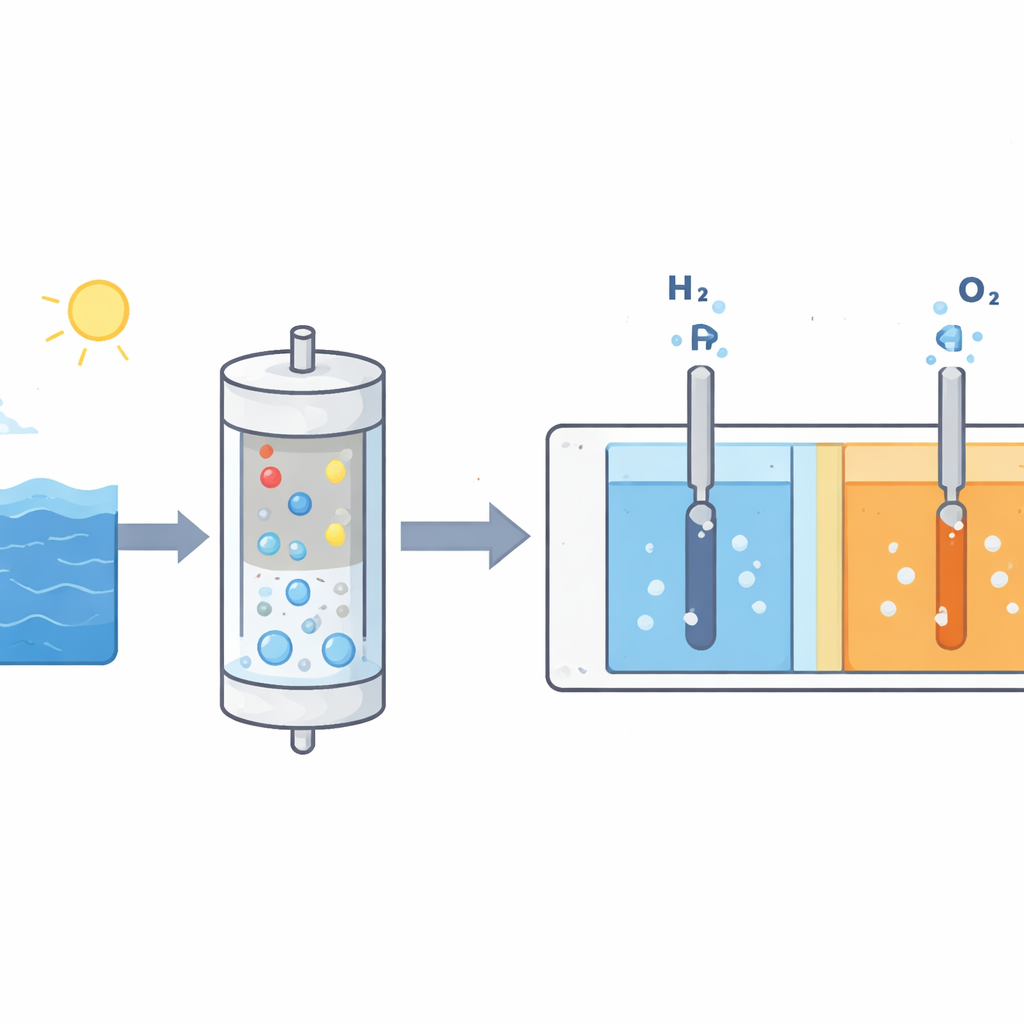
Ein zweistufiges System, das nur Wasser passieren lässt
Die Forscher bauten ein System, das die problematischen Salze auf Distanz hält. Meerwasser wird an der Außenseite eines „Ballon‑Filter“‑Moduls vorbeige pumpt, während innen eine konzentrierte alkalische Elektrolyt‑Lösung zirkuliert. Nur Wassermoleküle dürfen durch die dünne Membran des Ballons wandern, angetrieben durch die laufende Elektrolyse in der nachgeschalteten Zelle. Die Salze und anderen Ionen im Meerwasser verbleiben außen. Das einströmende Wasser gelangt dann in einen Anionenaustauschmembran‑Elektrolyseur, wo es in einer genau kontrollierten Umgebung in Wasserstoff und Sauerstoff gespalten wird. Weil die Rate, mit der Wasser den Ballon durchquert, automatisch an die Gasproduktionsrate gekoppelt ist, bleibt die Elektrolytkonzentration nahezu konstant, ohne komplexe Regelungssysteme.
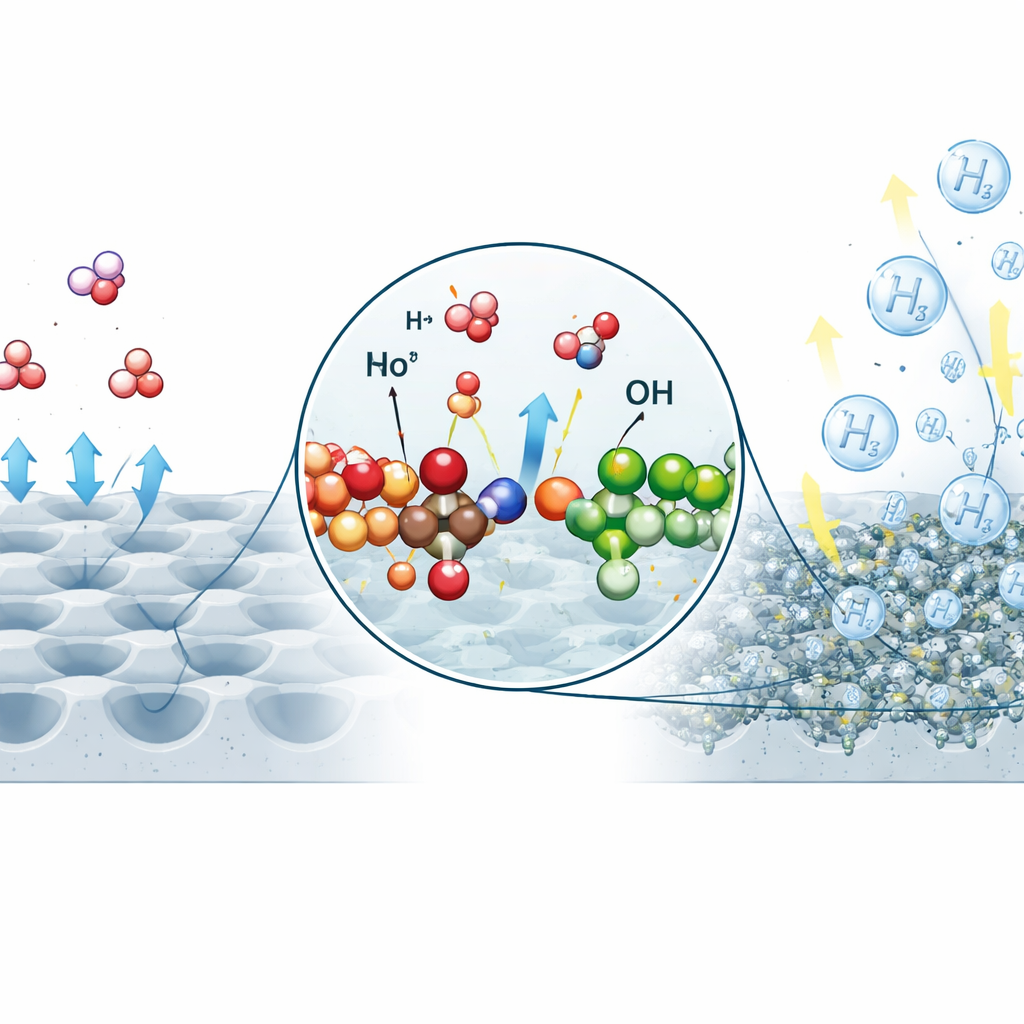
Ein Katalysator, Atom für Atom aufgebaut
Um dieses gefilterte Wasser effizient zu spalten, entwarf das Team einen neuen Katalysator aus Nickel‑ und Molybdänoxiden, angeordnet auf der Skala einzelner Atome. Mittels eines flüssigkeitsbasierten Herstellungsverfahrens wuchsen auf einem Nickelsubstrat eine Art Wald winziger schalenförmiger Mulden, und es bildeten sich zahllose Brücken, an denen Nickelatome über Sauerstoffatome mit Molybdän verbunden sind. Diese Mo–O–Ni‑Brücken verleihen jedem Reaktionszentrum eine doppelte Funktion: Die eine Seite hilft, Wassermoleküle aufzubrechen, die andere Seite unterstützt das Zusammenbauen und Freisetzen von Wasserstoffgas. Mikroskopie und fortgeschrittene Röntgenmessungen bestätigten die beabsichtigte Struktur und zeigten, dass die Nickelatome in der Nähe der Brücken einen elektronischen Zustand annehmen, der ideal ist, um die Reaktion zu beschleunigen.
Schnelle Reaktionen, stabile Betriebsweise
In Laborversuchen benötigte der neue Katalysator nur eine sehr geringe Überspannung, um mit der Wasserstoffproduktion zu beginnen, und hielt hohe Reaktionsraten selbst bei stromdichten Werten im Industriemaßstab aufrecht. Seine nano‑rauhe, stark benetzbare Oberfläche ermöglicht es Gasblasen, schnell abzulösen, wodurch verhindert wird, dass sie frisches Wasser von den aktiven Stellen fernhalten. Operando‑Experimente—Messungen, die während des tatsächlichen Betriebs des Katalysators durchgeführt wurden—zeigten, dass die Struktur unter Betriebsbedingungen stabil bleibt und dass die Mo‑reichen Bereiche die inneren Bindungen des Wassers schwächen, während die Ni‑reichen Bereiche den Wasserstoff leichter freigeben. Computersimulationen stützten dieses Bild, indem sie zeigten, dass die atomaren Brücken die Energiebarrieren sowohl für die Wasserspaltung als auch für die Wasserstofffreisetzung im Vergleich zu einfacheren Materialien senken.
Ein langlebiges Meerwasser‑zu‑Wasserstoff‑System
In Kombination bildeten der Ballonfilter und der Mo–O–Ni‑Katalysator ein Meerwasser‑Elektrolyse‑System, das über Tausende von Stunden kontinuierlich bei hohen Strömen lief. Tests mit echtem Meerwasser aus dem Bohai‑Meer zeigten, dass nahezu keine Salzionen in die Elektrolytflüssigkeit gelangten, keine chlorhaltigen Nebenprodukte nachweisbar waren und die zur Aufrechterhaltung des Betriebs erforderliche Spannung im Zeitverlauf nur geringfügig anstieg. Einfach ausgedrückt demonstriert die Studie einen realistischen Weg, reichlich vorhandenes Meerwasser in sauberen Wasserstoffbrennstoff zu verwandeln, ohne es zuerst zu entsalzen, indem man clever trennt, wo sich die Salze befinden, und präzise gestaltet, wie Atome auf einer Katalysatoroberfläche zusammenarbeiten.
Zitation: Shi, Z., Shi, W., Zhang, C. et al. Sustainable continuous seawater electrolysis using atomic interface catalyst via liquid-medium strategy. Nat Commun 17, 3940 (2026). https://doi.org/10.1038/s41467-026-70234-4
Schlüsselwörter: Meerwasser‑Elektrolyse, grüner Wasserstoff, Elektrokatalysator, Nickel‑Molybdän‑Grenzfläche, Anionenaustauschmembran