Clear Sky Science · fr
Altérations des gènes de réparation de l’ADN et efficacité du gemcitabine et nab-paclitaxel avec/sans durvalumab et tremelimumab dans l’adénocarcinome canalaire pancréatique métastatique
Pourquoi certains cancers du pancréas réagissent différemment
Le cancer du pancréas est l’un des cancers les plus mortels, et même les meilleurs traitements actuels ne prolongent la vie que de quelques mois en moyenne. Les immunothérapies, qui ont transformé la prise en charge de plusieurs autres cancers, ont jusqu’ici eu peu d’effet pour la plupart des personnes atteintes d’un cancer du pancréas avancé. Cette étude pose une question porteuse d’espoir : existe‑t‑il un petit sous‑groupe de patients dont les tumeurs sont configurées d’une façon particulière leur permettant de tirer beaucoup plus d’avantage de l’ajout d’une immunothérapie à la chimiothérapie standard ?
Un cancer difficile qui nécessite de meilleures options
L’adénocarcinome canalaire pancréatique métastatique est généralement diagnostiqué tardivement, lorsqu’il s’est déjà propagé et devient très difficile à traiter. Les associations de chimiothérapies ont progressivement amélioré la survie, mais de façon modeste. Les inhibiteurs de points de contrôle immunitaires, qui lèvent les freins du système immunitaire, ne sont bénéfiques dans cette maladie que lorsque la tumeur présente un défaut rare appelé déficience de réparation des mésappariements. La plupart des patients n’ont pas ce défaut, si bien que les médecins ont un besoin urgent d’autres signes fiables — des biomarqueurs — capables d’indiquer qui pourrait réellement bénéficier des traitements basés sur l’immunité.
Tester la chimiothérapie avec et sans renfort immunitaire
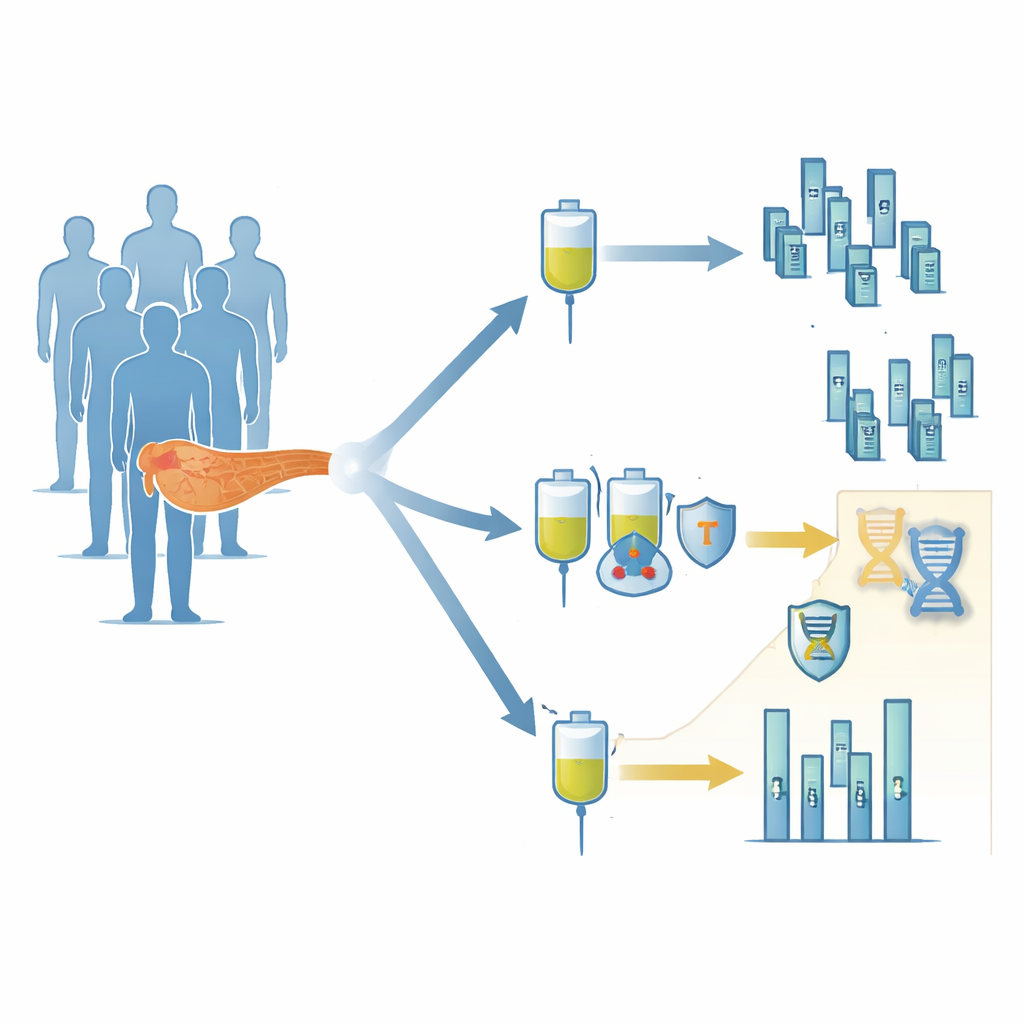
Dans l’essai clinique canadien CCTG PA.7, 180 patients récemment diagnostiqués d’un cancer du pancréas métastatique ont été répartis au hasard pour recevoir la chimiothérapie standard (gemcitabine et nab‑paclitaxel) soit seule, soit en association avec deux inhibiteurs de points de contrôle immunitaire, le durvalumab et le tremelimumab. Les chercheurs ont suivi les patients pendant plus de six ans pour savoir qui vivait plus longtemps et chez qui la maladie restait contrôlée. Globalement, l’association n’a pas aidé le patient moyen : la survie et le délai avant progression étaient pratiquement identiques dans les deux groupes. À première vue, l’ajout d’immunothérapie semblait simplement inefficace dans ce contexte.
Des indices cachés dans l’ADN tumoral circulant
L’équipe a ensuite cherché une explication plus profonde en utilisant un test sanguin appelé séquençage de l’ADN tumoral circulant, capable de détecter les altérations génétiques relâchées par les tumeurs dans la circulation. Ils se sont concentrés sur des gènes impliqués dans la réparation de l’ADN, notamment BRCA1, POLE, ATM et FANCA. À l’aide d’une approche d’apprentissage automatique, ils ont observé que lorsque les patients présentaient des mutations dans au moins deux de ces gènes de réparation de l’ADN, un schéma frappant apparaissait. Environ 10 % des patients appartenaient à ce groupe, et ceux qui ont reçu la combinaison chimiothérapie–immunothérapie ont vécu beaucoup plus longtemps que des patients comparables traités par chimiothérapie seule, la médiane de survie passant d’environ 10 mois à plus de deux ans. La plupart de ces patients présentaient également une réduction tumorale visible à l’imagerie.
Vérification du signal dans des échantillons tumoraux conservés
Pour s’assurer que le test sanguin n’induisait pas en erreur, les chercheurs ont aussi analysé des tissus tumoraux conservés d’un sous‑ensemble de patients par séquençage du génome complet. Dans la plupart des cas, les mêmes mutations des gènes de réparation de l’ADN observées dans le sang ont été confirmées dans les tissus. L’étude a également montré que ces tumeurs ne présentaient pas, au départ, une charge mutationnelle globale anormalement élevée, ce qui suggère que le motif spécifique de défauts de réparation de l’ADN — plutôt qu’un simple nombre élevé de mutations — pourrait contribuer à sensibiliser les tumeurs à la combinaison chimiothérapie plus immunothérapie. Néanmoins, les auteurs soulignent que leur analyse était exploratoire et portait sur un nombre relativement restreint de cas, de sorte que ces résultats doivent être confirmés dans des essais complémentaires.
Ce que cela pourrait signifier pour les patients
Pour la personne moyenne atteinte d’un cancer du pancréas avancé, l’ajout d’une double immunothérapie à la chimiothérapie standard n’a pas amélioré la survie. Mais cette étude met en lumière un petit sous‑groupe de patients cliniquement actionnable dont les tumeurs présentent plusieurs défauts dans des gènes clés de réparation de l’ADN et qui pourraient gagner plusieurs années de vie supplémentaire grâce à la combinaison. Comme ces altérations peuvent être détectées par un test sanguin, elles pourraient, après validation supplémentaire, aider les médecins à identifier rapidement quels patients sont les plus susceptibles de bénéficier d’une stratégie chimiothérapie–immunothérapie. Dans une maladie où le temps est compté et les options limitées, une telle stratégie guidée par des biomarqueurs pourrait faire une différence significative pour un groupe sélectionné de patients.
Citation: Renouf, D.J., Topham, J.T., Loree, J.M. et al. DNA Repair gene alterations and efficacy from gemcitabine and nab-paclitaxel with/without durvalumab and tremelimumab in metastatic pancreatic ductal adenocarcinoma. Nat Commun 17, 3631 (2026). https://doi.org/10.1038/s41467-026-70120-z
Mots-clés: cancer du pancréas, immunothérapie, gènes de réparation de l’ADN, biomarqueurs, ADN tumoral circulant