Clear Sky Science · de
Veränderungen von DNA-Reparaturgenen und Wirksamkeit von Gemcitabin und Nab-Paclitaxel mit/ohne Durvalumab und Tremelimumab beim metastasierten Pankreasduktaladenokarzinom
Warum einige Pankreaskarzinome unterschiedlich reagieren
Pankreaskrebs gehört zu den tödlichsten Krebsarten, und selbst die besten verfügbaren Medikamente verlängern das Leben meist nur um Monate. Immuntherapien, die die Behandlung mehrerer anderer Krebsarten grundlegend verändert haben, haben für die Mehrheit der Menschen mit fortgeschrittenem Pankreaskrebs bislang wenig bewirkt. Diese Studie stellt eine hoffnungsvolle Frage: Gibt es eine kleine Gruppe von Pankreaskrebspatienten, deren Tumoren auf besondere Weise beschaffen sind und die durch das Hinzufügen von Immuntherapie zur Standardchemotherapie deutlich mehr profitieren?
Ein aggressiver Krebs, der bessere Optionen braucht
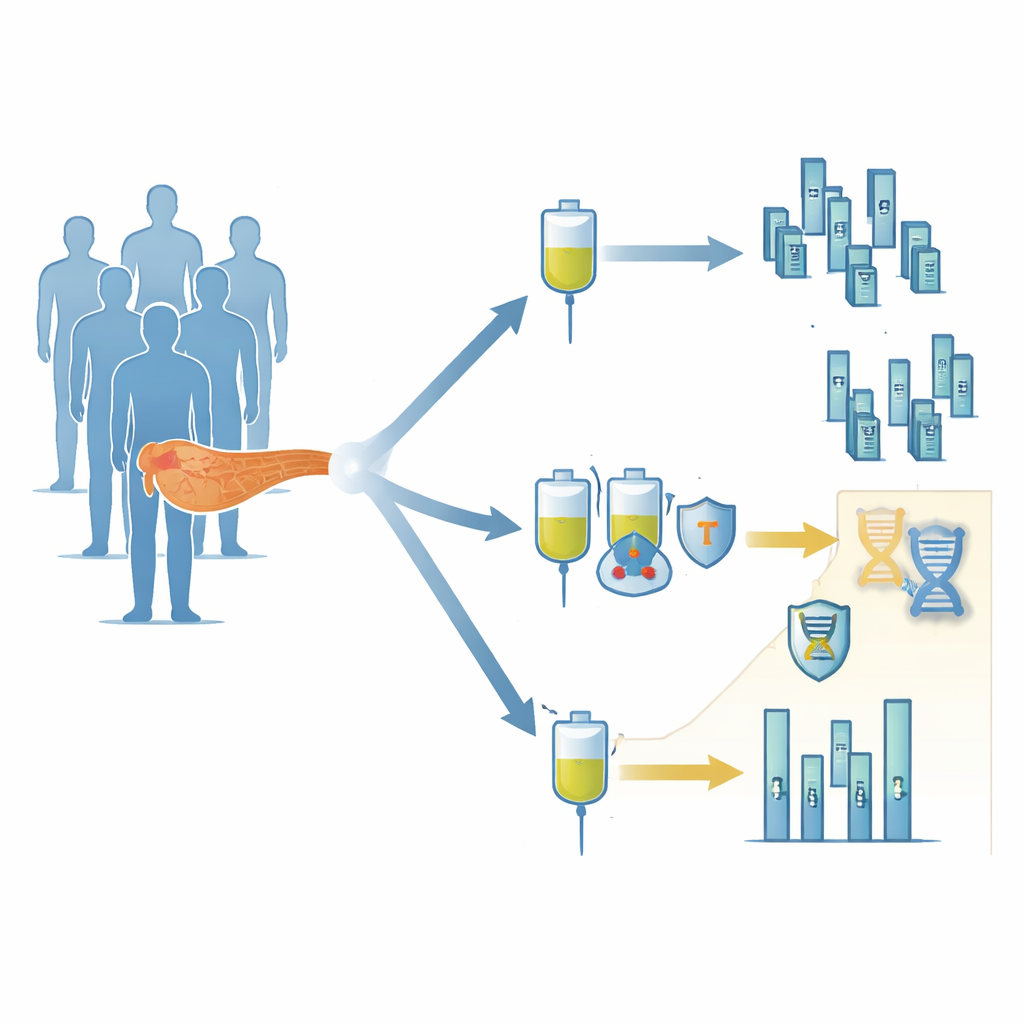
Das metastasierte Pankreasduktaladenokarzinom wird meist spät diagnostiziert, wenn es bereits gestreut hat und schwer zu behandeln ist. Standardkombinationen der Chemotherapie haben das Überleben langsam verbessert, aber nur moderat. Checkpoint-Inhibitoren, die die Bremsen des Immunsystems lösen, helfen bei dieser Erkrankung nur, wenn der Tumor einen seltenen Defekt namens Mismatch-Repair-Defizienz aufweist. Die meisten Patienten haben diesen Defekt nicht, sodass Ärzte dringend weitere verlässliche Hinweise – Biomarker – benötigen, die anzeigen können, wer tatsächlich von immunbasierten Therapien profitieren könnte.
Prüfung von Chemotherapie mit und ohne Immunverstärker
In der kanadischen CCTG PA.7-Studie wurden 180 Patienten mit neu diagnostiziertem metastasiertem Pankreaskrebs randomisiert, entweder die Standardchemotherapie (Gemcitabin und Nab-Paclitaxel) allein oder kombiniert mit zwei Checkpoint-Inhibitoren, Durvalumab und Tremelimumab, zu erhalten. Die Forschenden verfolgten die Patienten über mehr als sechs Jahre, um zu sehen, wer länger lebte und bei wem die Krankheit unter Kontrolle blieb. Insgesamt half die Kombination dem durchschnittlichen Patienten nicht: Überleben und Zeit bis zum Progress waren in beiden Behandlungsgruppen nahezu gleich. Auf den ersten Blick schien das Hinzufügen der Immuntherapie in diesem Setting einfach nicht zu wirken.
Verborgene Hinweise in Tumor-DNA aus einem Bluttest
Das Team suchte dann nach einer tieferen Erklärung mithilfe eines blutbasierten Tests namens Sequenzierung zirkulierender Tumor-DNA, der genetische Veränderungen erkennen kann, die von Tumoren ins Blut abgegeben werden. Sie konzentrierten sich auf Gene, die an der Reparatur von DNA-Schäden beteiligt sind, darunter BRCA1, POLE, ATM und FANCA. Mit einem maschinellen Lernverfahren stellten sie fest, dass, wenn Patienten Mutationen in mindestens zwei dieser DNA-Reparaturgene hatten, ein auffälliges Muster erschien. Etwa 10 Prozent der Patienten fielen in diese Gruppe, und diejenigen, die die Chemo–Immuntherapie erhielten, lebten deutlich länger als vergleichbare Patienten, die nur Chemotherapie bekamen; das mediane Überleben verlängerte sich von etwa 10 Monaten auf mehr als zwei Jahre. Die meisten dieser Patienten zeigten zudem sichtbare Tumorschrumpfungen in Bildgebungen.
Überprüfung des Signals in gelagerten Tumorproben
Um sicherzugehen, dass der Bluttest nicht irreführte, analysierten die Forschenden auch konserviertes Tumorgewebe einer Untergruppe von Patienten mittels Ganzgenomsequenzierung. In den meisten Fällen wurden die gleichen Mutationen in DNA-Reparaturgenen, die im Blut gefunden wurden, auch im Gewebe bestätigt. Die Studie zeigte zudem, dass diese Tumoren nicht von vornherein eine ungewöhnlich hohe Gesamtmutationslast aufwiesen, was darauf hindeutet, dass das spezifische Muster der DNA-Reparaturdefekte – und nicht nur eine große Anzahl von Mutationen – die Tumoren gegenüber der Kombination aus Chemotherapie und Immuntherapie empfindlicher machen könnte. Die Autoren betonen jedoch, dass ihre Analyse explorativ war und relativ kleine Fallzahlen umfasste, sodass die Ergebnisse in weiteren Studien bestätigt werden müssen.
Was das für Patienten bedeuten könnte
Für den durchschnittlichen Menschen mit fortgeschrittenem Pankreaskrebs verbesserte die Zugabe einer doppelten Immuntherapie zur Standardchemotherapie das Überleben nicht. Diese Studie hebt jedoch eine kleine, handlungsrelevante Untergruppe von Patienten hervor, deren Tumoren mehrere Defekte in wichtigen DNA-Reparaturgenen tragen und die durch die Kombination Jahre an zusätzlichem Leben gewinnen könnten. Da sich diese Veränderungen durch einen Bluttest nachweisen lassen, könnten sie – nach weiterer Validierung – Ärzten helfen, schnell zu identifizieren, welche Patienten am ehesten von Chemo–Immuntherapie profitieren. In einer Erkrankung, in der die Zeit knapp und die Optionen begrenzt sind, könnte eine biomarkergesteuerte Strategie für eine ausgewählte Patientengruppe einen spürbaren Unterschied machen.
Zitation: Renouf, D.J., Topham, J.T., Loree, J.M. et al. DNA Repair gene alterations and efficacy from gemcitabine and nab-paclitaxel with/without durvalumab and tremelimumab in metastatic pancreatic ductal adenocarcinoma. Nat Commun 17, 3631 (2026). https://doi.org/10.1038/s41467-026-70120-z
Schlüsselwörter: Pankreaskrebs, Immuntherapie, DNA-Reparaturgene, Biomarker, zirkulierende Tumor-DNA