Clear Sky Science · fr
Déconvolution double en microscopie à illumination structurée multiphotonique pour l’imagerie super‑résolutive en tissus profonds
Voir plus profondément dans les tissus vivants
La biologie moderne repose souvent sur la capacité à observer les moindres détails à l’intérieur d’échantillons épais, comme des tranches de cerveau ou des embryons en développement. Malheureusement, au fur et à mesure que la lumière traverse ces environnements denses, elle se déforme et se brouille, rendant les images floues précisément quand les chercheurs ont le plus besoin d’une grande netteté. Cet article présente une méthode pour « dé‑brouiller » numériquement ces images, permettant à un microscope avancé standard de révéler des structures extrêmement fines en profondeur dans les tissus sans ajouter de matériel coûteux et complexe.
Pourquoi l’imagerie en profondeur est si difficile
Les microscopes à fluorescence permettent d’étiqueter des molécules spécifiques et d’observer la construction et le comportement des cellules et des tissus. Au cours des dernières décennies, plusieurs méthodes de « super‑résolution » ont dépassé les limites traditionnelles de netteté, dévoilant des détails bien en dessous de 200 nanomètres. Cependant, la plupart de ces méthodes ne fonctionnent bien que près de la surface d’un échantillon. Dans des tissus épais comme le cerveau de souris, la lumière utilisée pour exciter les marqueurs fluorescents et la lumière émise vers le détecteur sont toutes deux déformées par de petites variations dans la structure du tissu. Ces déformations, appelées aberrations, floutent le foyer du microscope et effacent les informations fines, en particulier à des profondeurs supérieures à quelques dizaines de micromètres.
Des correctifs matériels à une solution logicielle
Une approche courante pour combattre les aberrations est l’optique adaptative matérielle, qui utilise des miroirs mobiles ou d’autres dispositifs pour remodeler le front d’onde et restaurer un foyer net. Bien que puissants, ces systèmes sont coûteux, techniquement exigeants et corrigent souvent les distorsions pour une seule couleur ou une seule direction de propagation à la fois. Les auteurs proposent plutôt une approche computationnelle compatible avec un type de microscope déjà répandu dans de nombreux laboratoires : le microscope multiphotonique à balayage laser. En remplaçant le détecteur unique habituel par une caméra, ils enregistrent une pile riche d’images scannées qui encode comment à la fois la lumière d’excitation entrante et la fluorescence sortante ont été déformées par le tissu.
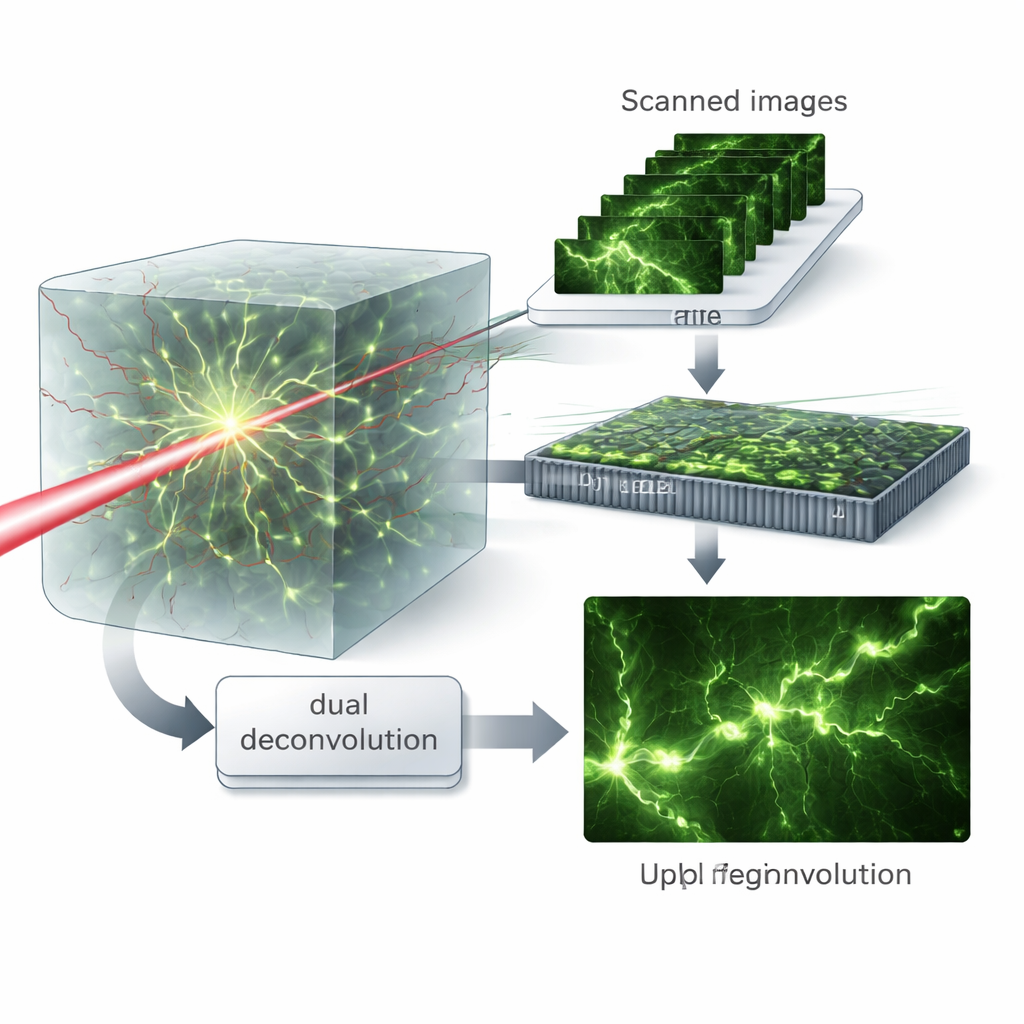
Motifs virtuels et nettoyage double
L’idée clé est de considérer les images scannées comme si l’échantillon avait été illuminé par de nombreux motifs fins de lumière différents, un concept que les auteurs appellent illumination structurée virtuelle. En recomposant mathématiquement ces données dans le domaine fréquentiel, ils séparent les rôles des processus d’excitation et d’émission. Ils introduisent ensuite un algorithme de « déconvolution double » qui estime et corrige alternativement le flou de chaque côté — la lumière entrant et la lumière sortant — plutôt que de les regrouper en un seul flou effectif. Ce traitement matriciel préserve davantage de détails en haute fréquence et permet à l’algorithme de récupérer des structures fines même lorsque les aberrations sont importantes.
Des vues plus nettes en simulations et sur des échantillons réels
Pour tester leur méthode, l’équipe a d’abord utilisé des simulations informatiques de microscopie biphotonique, une technique d’imagerie en profondeur qui utilise des paires de photons de moindre énergie pour exciter la fluorescence uniquement au point focal. Sous des distorsions simulées sévères, les reconstructions biphotoniques conventionnelles et celles d’illumination structurée standard donnaient des images visiblement floues. En revanche, la déconvolution double a restauré des motifs nets dont la résolution approchait le quart de la longueur d’onde de la fluorescence — environ 130 nanomètres — en accord avec les prévisions théoriques. Les auteurs ont ensuite construit un montage biphotonique personnalisé avec une caméra scientifique et appliqué leur algorithme à des échantillons réels, y compris des billes fluorescentes, des motifs tests cachés derrière des couches diffusantes, des cellules en culture, du tissu de cerveau de souris et des zebrafish entiers en montage. À maintes reprises, des structures qui paraissaient brouillées ou doublées dans les images conventionnelles sont apparues comme des éléments clairement séparés après traitement, et des éléments neuronaux fins comme les épines dendritiques sont restés résolvables jusqu’à 180 micromètres de profondeur dans le cerveau de souris.
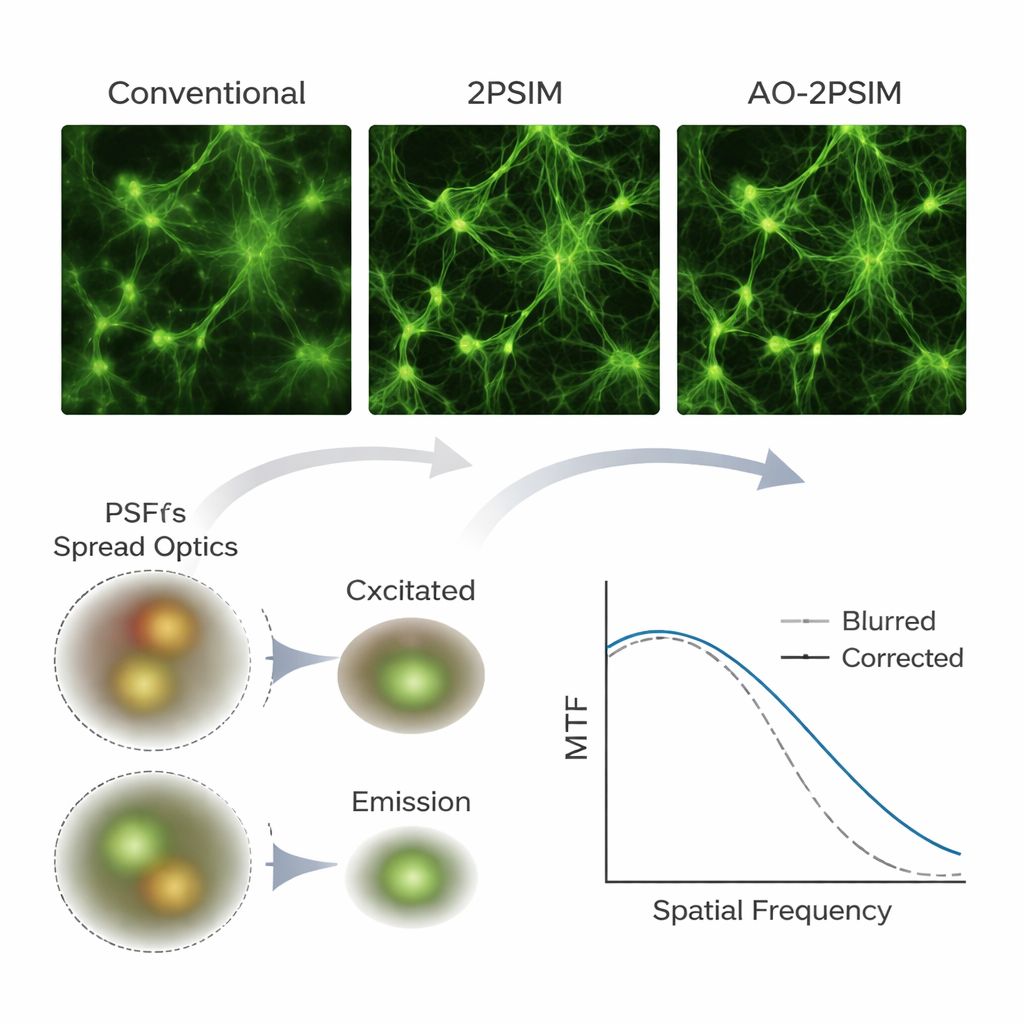
Ce que cela signifie pour l’imagerie biologique
Pour un public non spécialiste, le message principal est que les auteurs ont montré comment transformer des microscopes multiphotoniques existants en outils d’imagerie en tissus profonds beaucoup plus puissants en s’appuyant principalement sur du logiciel et une mise à niveau par caméra. En modélisant et corrigeant précisément la façon dont les tissus dévient la lumière à l’entrée comme à la sortie, leur approche de déconvolution double double la limite de résolution habituelle dans des échantillons épais et difficiles sans recourir à des miroirs adaptatifs complexes. Si la méthode dépend toujours de la collecte d’un signal suffisant et nécessite actuellement un balayage relativement lent, elle offre une voie pratique et rentable vers des vues tridimensionnelles ultra‑nettes du cerveau et d’autres organes, ouvrant la porte à des études plus détaillées de l’organisation et de l’évolution des structures biologiques dans le temps.
Citation: Lim, S., Kang, S., Hong, J.H. et al. Dual deconvolution in multiphoton structured illumination microscopy for deep-tissue super-resolution imaging. Nat Commun 17, 2123 (2026). https://doi.org/10.1038/s41467-026-69798-y
Mots-clés: microscopie super‑résolution, imagerie biphotonique, optique adaptative, imagerie en tissus profonds, imagerie computationnelle