Clear Sky Science · fr
Les récepteurs neuronaux ancestraux sont des toxines accessoires bactériennes
Des armes bactériennes à l’organisation du cerveau
Nos cerveaux dépendent de connexions d’une précision remarquable entre cellules nerveuses, guidées en partie par des protéines de surface inhabituelles appelées ténurines. Cette étude révèle que ces récepteurs neuronaux essentiels n’ont pas commencé leur existence comme de simples guides. Ils trouvent leur origine chez des bactéries, où ils faisaient partie d’armes toxiques employées dans les combats microbien. En montrant comment ces toxines anciennes ont été recyclées en outils de communication, le travail illustre de façon frappante comment l’évolution a transformé des instruments de guerre en éléments constitutifs de la vie multicellulaire complexe.
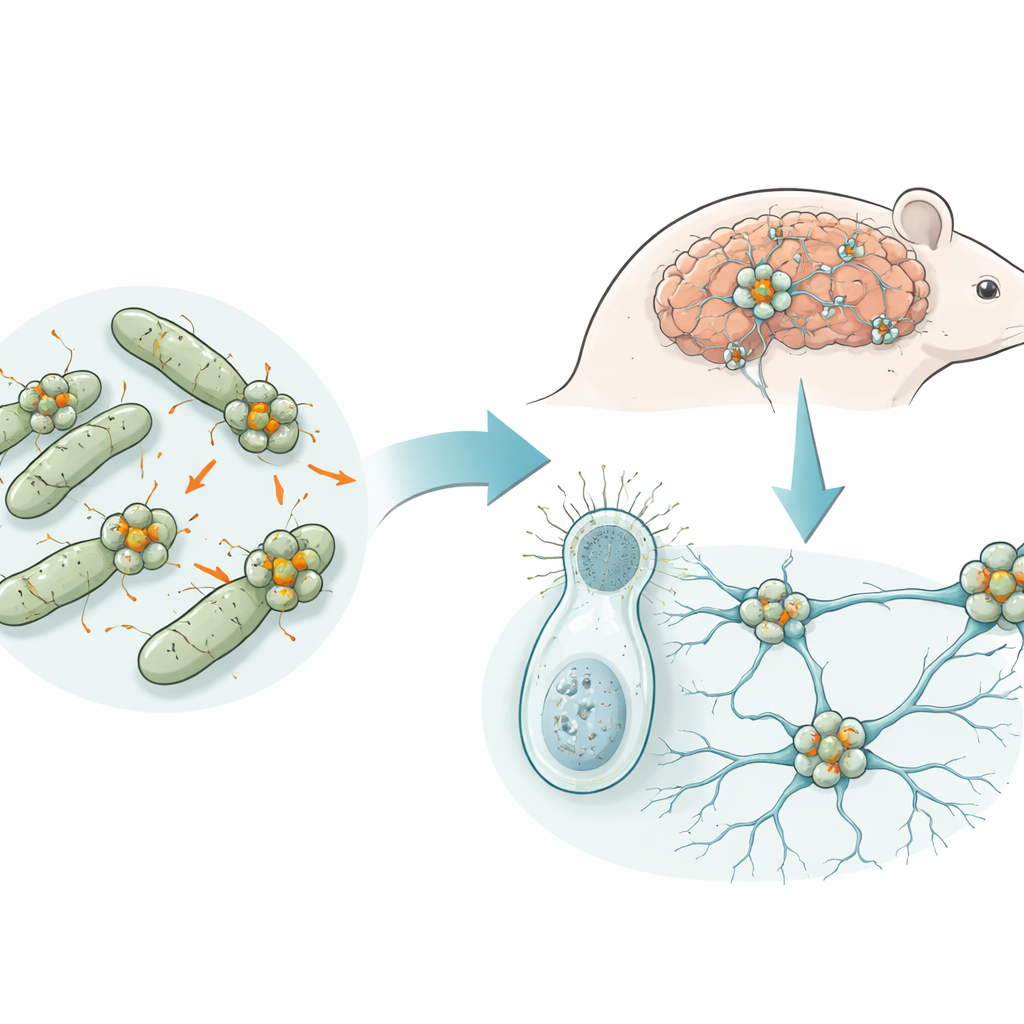
Des protéines anciennes au passé surprenant
Les ténurines sont de grandes protéines complexes qui siègent dans la membrane des cellules animales et aident les neurones à trouver et à se connecter à leurs partenaires appropriés. On les trouve chez de nombreux animaux dotés d’un système nerveux, et même chez certains de leurs proches unicellulaires, alors que les bactéries ne possèdent pas de nerfs. Des travaux antérieurs laissaient entendre que les ténurines pourraient provenir de bactéries via un transfert horizontal de gènes, c’est‑à‑dire le saut de gènes entre espèces plutôt que leur transmission héréditaire. Les auteurs ont entrepris de retracer cette origine et de comprendre quel rôle les versions bactériennes, appelées protéines de type ténurine (TLP), jouent dans la vie microbienne.
Une coquille cachée et un noyau toxique
En analysant des centaines de milliers de génomes bactériens, l’équipe a constaté que seule une petite fraction d’espèces porte des gènes TLP, mais ces espèces sont réparties à travers de nombreuses branches de l’arbre bactérien. Les TLP partagent une architecture centrale conservée : une grande « coquille » protéique construite à partir d’éléments structuraux répétés qui s’enroulent pour former une chambre fermée. À l’aide de cryo‑microscopie électronique à haute résolution sur une TLP de la bactérie Bacillus inaquosorum, les chercheurs ont montré que cette coquille ressemble étroitement à l’ossature centrale des ténurines animales. Toutefois, plutôt que de s’étendre vers l’extérieur, la queue de la TLP bactérienne se replie à l’intérieur de la coquille pour former un noyau compact entièrement enfermé.
Guerre bactérienne et protection intégrée
L’équipe s’est interrogée sur la fonction de ce noyau enfoui. Des prédictions structurales informatiques sur de nombreuses TLP ont révélé que ces domaines C‑terminaux ressemblent à un large éventail d’enzymes connues pour endommager les cellules, notamment des nucléases, des protéases, des hydrolases et des transférases ADP‑ribosyles — beaucoup d’entre elles étant des types classiques de toxines. Des expériences chez Escherichia coli ont montré que l’expression de ces noyaux pouvait arrêter la croissance, perforer les membranes ou épuiser des molécules cellulaires essentielles, confirmant leur activité toxique. Fait important, presque chaque gène TLP se trouve à côté d’un petit gène partenaire codant pour une protéine « immunitaire » correspondante. Lorsqu’elles sont co‑produites, ces protéines d’immunité se lient aux noyaux toxiques et les neutralisent, protégeant la bactérie hôte tout en lui permettant d’utiliser ces toxines contre des concurrents.
De l’attaque cellulaire à la communication cellulaire
Au‑delà d’études de cas particulières, les auteurs ont constaté que les TLP sont particulièrement enrichies dans des familles bactériennes connues pour des comportements sociaux complexes, comme la prédation et le roulement coopératif. Ce schéma, associé à la configuration modulaire toxine‑plus‑immunité, identifie les TLP comme une classe distincte de toxines polymorphes : des armes personnalisables que différentes bactéries adaptent à leurs besoins écologiques. L’ossature structurale des TLP — la coquille qui emballe leurs noyaux toxiques — est essentiellement le même « superpli » qui forme le cœur des ténurines animales. Chez les animaux, cependant, le rôle toxique a été perdu. Le squelette des ténurines est relié à une ancre membranaire et utilisé comme récepteur de surface stable qui médie l’adhésion et la signalisation entre cellules voisines, en particulier entre neurones.
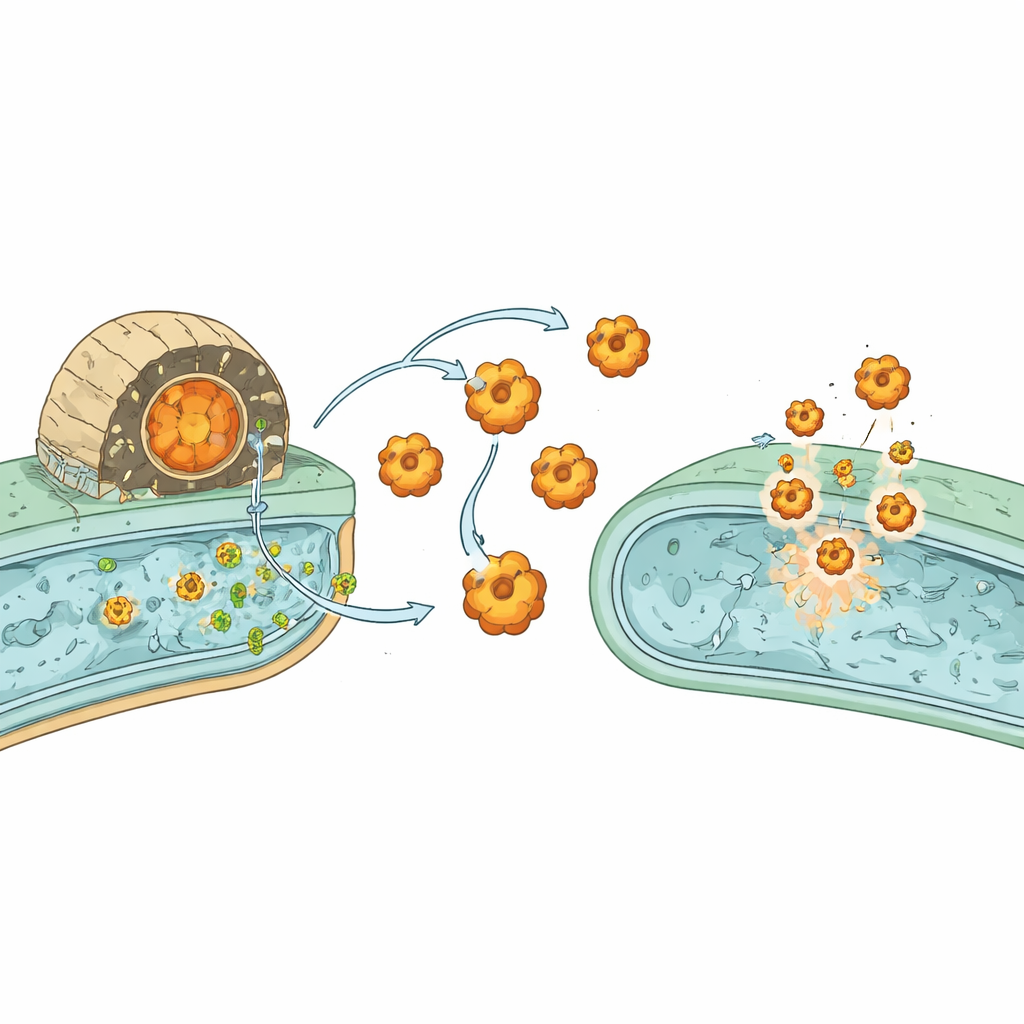
Comment une arme a contribué à construire le système nerveux
Pour le non‑spécialiste, le message central est qu’un système protéique autrefois utilisé par des bactéries pour empoisonner leurs rivaux a été capturé par les premiers proches des animaux et remodelé en un centre de communication pour les tissus nerveux. Chez les bactéries, les TLP servent de plateformes de livraison qui emballent et protègent de petites toxines fortement variables, associées à des antidotes assortis. Lorsqu’un socle structurel similaire est passé aux premiers eucaryotes — probablement via un transfert de gènes provenant de bactéries ingérées comme proies — il a été réutilisé : plutôt que de propulser des toxines, il est devenu un moyen pour les cellules de se reconnaître et de s’adhérer les unes aux autres. Au fil de l’évolution, cette transformation a contribué à l’apparition de tissus organisés et, finalement, des circuits neuronaux sophistiqués qui sous‑tendent le comportement et la cognition des animaux.
Citation: Raoelijaona, F., Szczepaniak, J., Schahl, A. et al. Ancestral neuronal receptors are bacterial accessory toxins. Nat Commun 17, 2753 (2026). https://doi.org/10.1038/s41467-026-69246-x
Mots-clés: transfert horizontal de gènes, toxines bactériennes, récepteurs ténurine, évolution du système nerveux, communication cellule‑cellule