Clear Sky Science · de
Ursprüngliche neuronale Rezeptoren sind bakterielle Zusatzgifte
Von bakteriellen Waffen zur Verdrahtung des Gehirns
Unsere Gehirne beruhen auf außerordentlich präzisen Verbindungen zwischen Nervenzellen, die unter anderem von ungewöhnlichen Oberflächenproteinen namens Teneurine geleitet werden. Diese Studie zeigt, dass diese wichtigen neuronalen Rezeptoren keineswegs ursprünglich als harmlose Lotsen entstanden sind. Stattdessen hatten sie ihren Ursprung in Bakterien als Bestandteile toxischer Waffen, die in mikrobiellen Kämpfen eingesetzt wurden. Indem die Arbeit aufdeckt, wie diese uralten Toxine zu Kommunikationswerkzeugen umfunktioniert wurden, liefert sie ein eindrückliches Beispiel dafür, wie die Evolution Instrumente des Krieges in Bausteine komplexen mehrzelligen Lebens verwandelt hat.
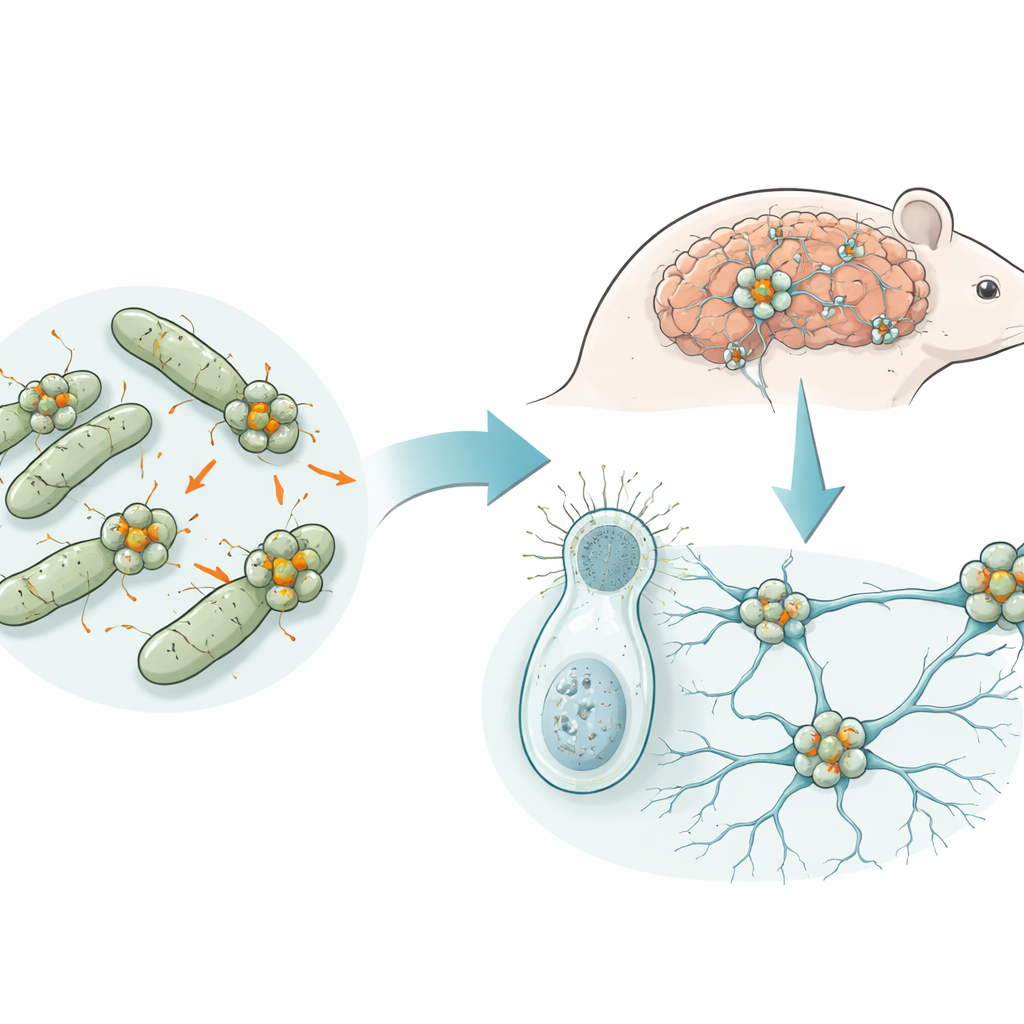
Uralte Proteine mit überraschender Vergangenheit
Teneurine sind große, komplexe Proteine, die in den Membranen tierischer Zellen sitzen und dabei helfen, dass Neuronen ihre richtigen Partner finden und verbinden. Man findet sie in Tieren mit Nervensystemen und sogar bei manchen ihrer einzelligen Verwandten, doch Bakterien besitzen überhaupt keine Nerven. Frühere Arbeiten deuteten bereits an, dass Teneurine möglicherweise durch horizontalen Gentransfer aus Bakterien stammen—ein Mechanismus, bei dem Gene zwischen Arten springen, anstatt ausschließlich entlang der Abstammungslinie vererbt zu werden. Die Autoren machten sich daran, diese Abstammung nachzuverfolgen und zu verstehen, welche Rolle die bakteriellen Versionen, sogenannte Teneurin‑ähnliche Proteine (TLPs), im mikrobiellen Leben spielen.
Eine verborgene Hülle und ein toxischer Kern
Beim Durchsuchen Hunderttausender bakterieller Genome fand das Team, dass nur ein kleiner Bruchteil der Arten TLP‑Gene trägt, diese Arten aber über viele Zweige des bakteriellen Stammbaums verstreut sind. TLPs teilen eine konservierte mittlere Architektur: eine große Protein‑„Hülle“, aufgebaut aus wiederholten Strukturelementen, die sich spiralförmig zu einer geschlossenen Kammer winden. Mithilfe hochauflösender kryogener Elektronenmikroskopie an einem TLP aus dem Bakterium Bacillus inaquosorum zeigten die Forschenden, dass diese Hülle der zentralen Gerüststruktur tierischer Teneurine sehr ähnlich ist. Anstatt sich jedoch nach außen zu verlängern, faltet sich der Schwanz des bakteriellen TLPs nach innen in die Hülle und bildet einen kompakten Kern, der vollständig eingeschlossen bleibt.
Bakterielle Kriegsführung und eingebaute Schutzmechanismen
Das Team fragte, welche Funktion dieser vergrabene Kern hat. Strukturvorhersagen per Computer über viele TLPs hinweg zeigten, dass diese C‑terminalen Kerne einer großen Bandbreite von Enzymen ähneln, die dafür bekannt sind, Zellen zu schädigen—darunter Nucleasen, Proteasen, Hydrolasen und ADP‑Ribosyl‑Transferasen, viele davon klassische Toxintypen. Experimente in Escherichia coli zeigten, dass die Expression dieser Kerne das Wachstum stoppen, Membranen durchlöchern oder entscheidende zelluläre Moleküle entziehen kann, was bestätigt, dass sie als Toxine wirken. Wichtig ist, dass fast jedes TLP‑Gen neben einem kleinen Partnergen liegt, das ein passendes „Immunitäts“-Protein kodiert. Bei gleichzeitiger Produktion binden diese Immunitätsproteine die toxischen Kerne und neutralisieren sie, wodurch das Wirtsbakterium geschützt wird, während es weiterhin Toxine gegen Konkurrenten einsetzen kann.
Vom Zellangriff zur Zellkommunikation
Über konkrete Einzelfälle hinaus fanden die Autoren, dass TLPs besonders in bakteriellen Familien angereichert sind, die für komplexes Sozialverhalten bekannt sind, etwa Prädation und kooperatives Schwärmen. Dieses Muster zusammen mit dem modularen Toxin‑plus‑Immunitäts‑Aufbau identifiziert TLPs als eigene Klasse polymorpher Toxine: anpassbare Waffen, die verschiedene Bakterien an ihre ökologischen Bedürfnisse anpassen. Das strukturelle Rückgrat der TLPs—die Hülle, die ihre toxischen Kerne verpackt—ist im Wesentlichen dasselbe „Superfold“, das das Herz tierischer Teneurine bildet. In Tieren ist die toxische Funktion jedoch verloren gegangen. Stattdessen ist das Teneurin‑Gerüst an eine Membranverankerung gekoppelt und dient als stabiler Oberflächenrezeptor, der Adhäsion und Signalübertragung zwischen benachbarten Zellen vermittelt, insbesondere zwischen Neuronen.
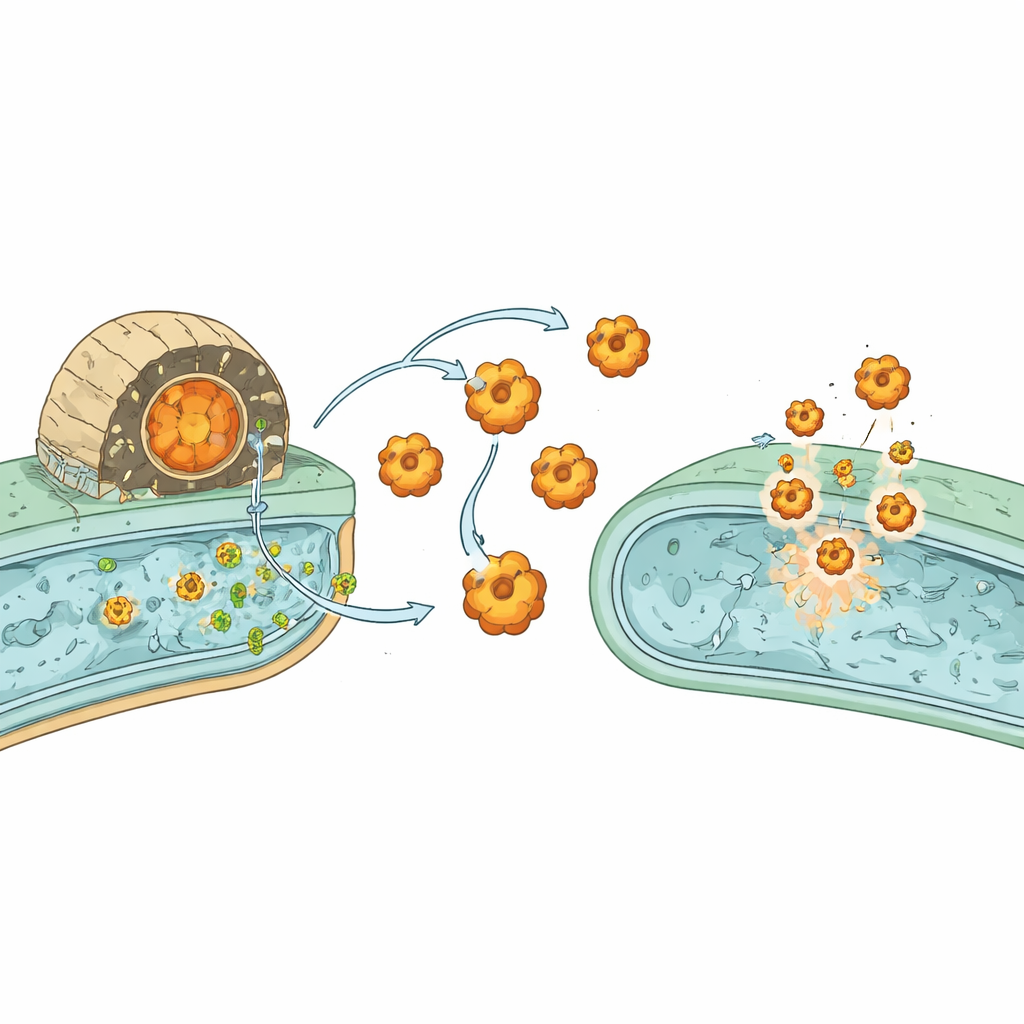
Wie eine Waffe beim Aufbau des Nervensystems half
Für Nicht‑Spezialisten lautet die zentrale Botschaft: Ein Proteinsystem, das einst von Bakterien verwendet wurde, um Rivalen zu vergiften, wurde von frühen tierischen Verwandten eingefangen und zu einem Kommunikationszentrum für Nervengewebe umgestaltet. In Bakterien fungieren TLPs als Lieferplattformen, die kleine, hochvariable Toxine verpacken und schützen, gepaart mit passenden Gegengiften. Als ein ähnliches Strukturgerüst in frühe Eukaryoten gelangte—wahrscheinlich durch Gentransfer aus von ihnen verzehrten Bakterien—wurde es umgenutzt: Anstatt Toxine abzufeuern, wurde es zu einem Mittel, mit dem Zellen einander erkennen und aneinander haften können. Im Lauf der Evolution unterstützte diese Umwandlung die Entstehung organisierter Gewebe und schließlich die komplexen neuronalen Schaltkreise, die Verhalten und Kognition von Tieren ermöglichen.
Zitation: Raoelijaona, F., Szczepaniak, J., Schahl, A. et al. Ancestral neuronal receptors are bacterial accessory toxins. Nat Commun 17, 2753 (2026). https://doi.org/10.1038/s41467-026-69246-x
Schlüsselwörter: horizontaler Gentransfer, bakterielle Toxine, Teneurin-Rezeptoren, Entwicklung des Nervensystems, Zell‑zu‑Zell‑Kommunikation