Clear Sky Science · fr
Les fontaines d’extrusion sont des signatures de l’organisation des chromosomes émergentes lors de l’activation du génome zygotique
Comment la vie précoce active son ADN
Tout embryon animal fait face au même défi : au départ, il fonctionne grâce aux molécules fournies par la mère, mais bien vite il doit réveiller son propre ADN et commencer à contrôler sa croissance. Cette étude se demande ce qui arrive au repliement physique des chromosomes à ce moment crucial, et met au jour un motif structural surprenant, surnommé « fontaines », qui semble marquer les endroits où les interrupteurs de contrôle clés du génome s’enclenchent.
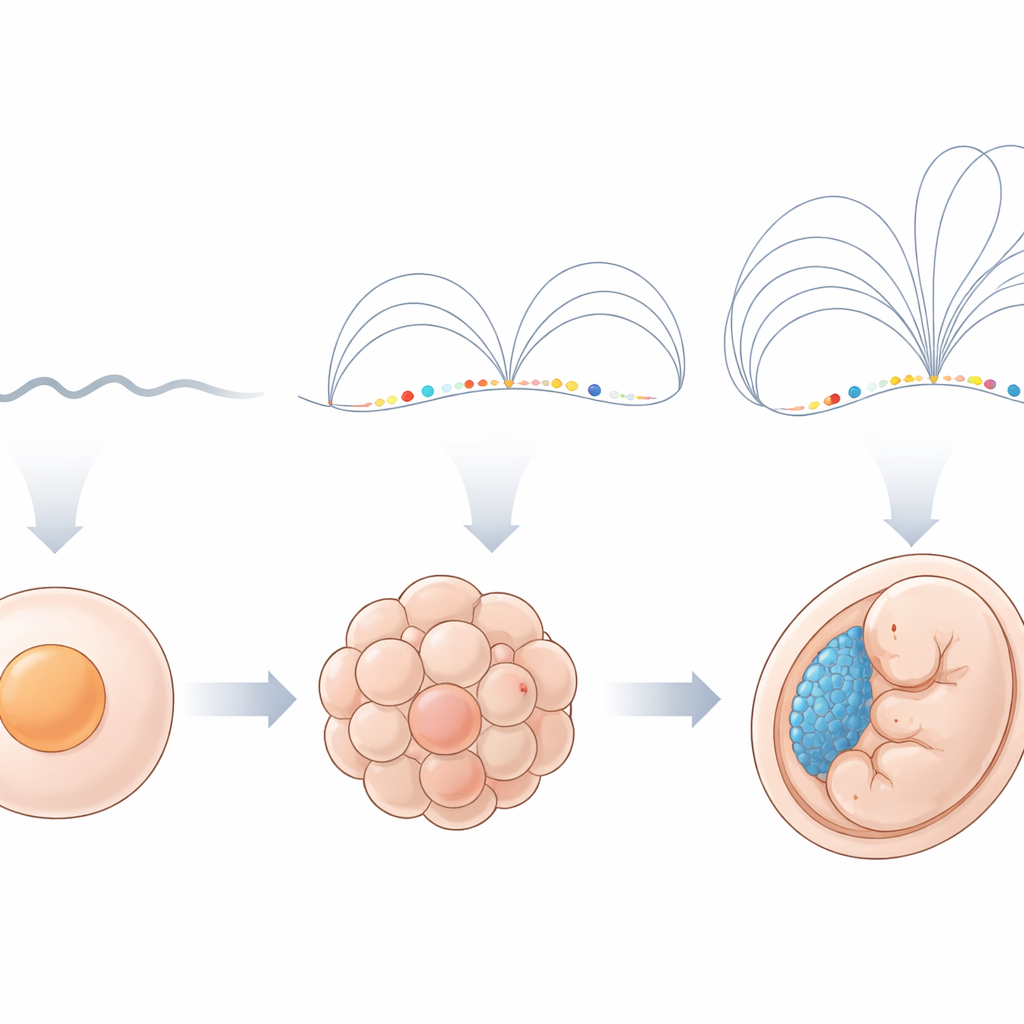
Un génome silencieux qui s’éveille soudainement
Chez le poisson zèbre et chez de nombreux autres animaux, les gènes propres de l’embryon s’activent en un sursaut appelé activation du génome zygotique. Avant cela, les chromosomes paraissent relativement uniformes lorsqu’on les observe avec le Hi-C, une technique qui mesure quelles parties de l’ADN se trouvent proches les unes des autres dans l’espace 3D. Après l’activation, les chercheurs observent généralement des motifs familiers comme des compartiments et des boucles qui reflètent l’empaquetage de l’ADN. Les auteurs ont collecté des données Hi-C à partir de spermatozoïdes et de plusieurs stades précoces d’embryons de poisson zèbre pour suivre cette transition en détail. Ils confirment qu’avant l’activation, les chromosomes présentent peu de traits reconnaissables, puis que peu après apparaissent des compartiments à grande échelle et des structures locales plus marquées.
Les motifs en « fontaine » marquent les régions de contrôle précoces
En examinant de près les premières structures locales qui surgissent, l’équipe a découvert des motifs de contacts distincts qu’elle appelle fontaines. Sur une carte Hi-C, une fontaine ressemble à une base étroite située en un point de l’ADN qui s’élargit en un éventail de contacts enrichis en s’éloignant le long du chromosome. Ces formes diffèrent des domaines en boîte et des traits en bande observés ultérieurement. À l’aide d’un outil de détection automatisé, les auteurs ont identifié plus d’un millier de fontaines peu après l’activation du génome chez le poisson zèbre, et des motifs similaires dans les premiers embryons de la grenouille et du poisson medaka. Il est intrigant de constater que les fontaines tendent à se former dans des régions d’ADN ouvertes, actives tôt dans le développement et marquées chimiquement comme des enhancers — interrupteurs régulateurs qui aident les gènes voisins à s’activer — plutôt qu’aux promoteurs, où la lecture des gènes commence réellement.
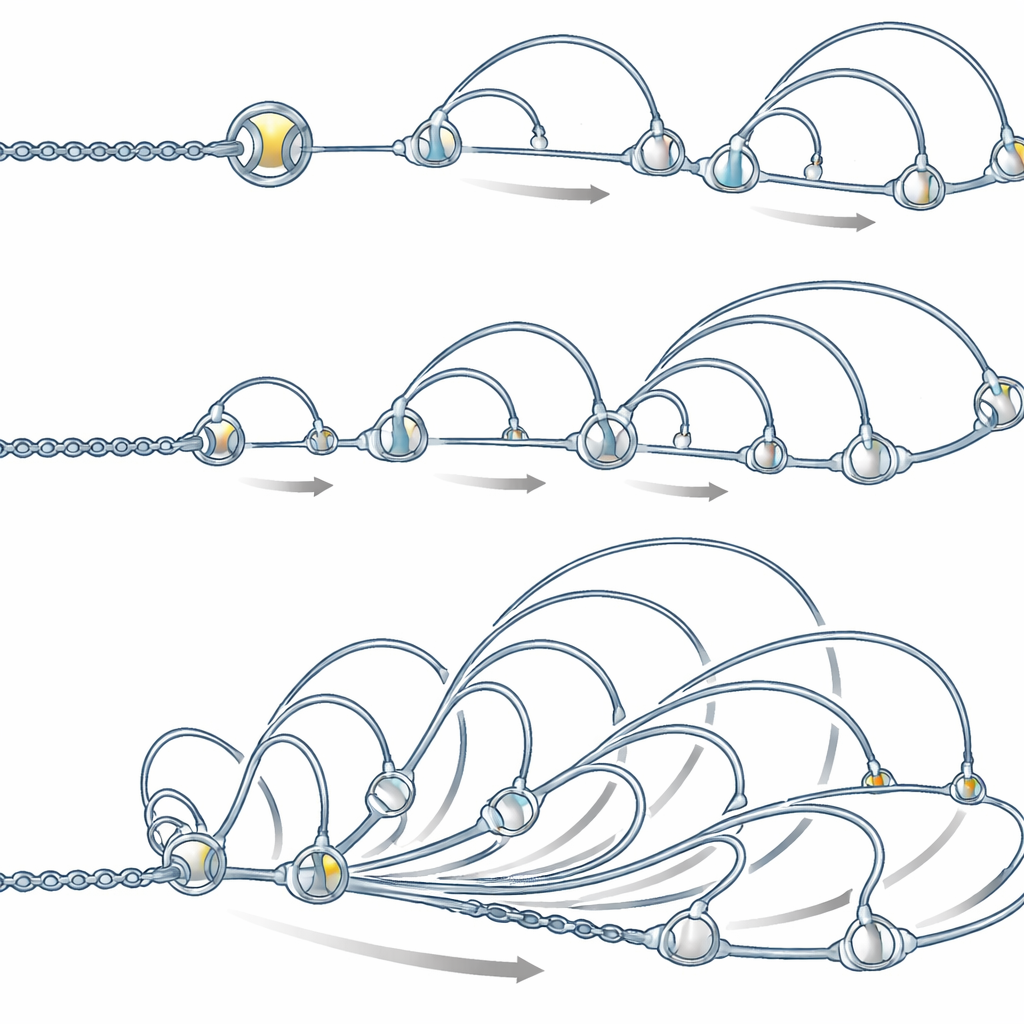
Des protéines initiatrices préparent les sites où se forment les fontaines
Pour tester si les fontaines dépendent vraiment de ces interrupteurs précoces, les chercheurs se sont concentrés sur des facteurs de transcription « pionniers » — des protéines capables d’ouvrir de l’ADN compacté. Chez le poisson zèbre, trois de ces facteurs (Pou5f3, Sox19b et Nanog) sont connus pour établir les enhancers précoces. Lorsque les embryons étaient dépourvus des trois, les motifs caractéristiques de fontaine disparaissaient en grande partie aux endroits où l’accessibilité de la chromatine et les marques d’enhancer étaient perdues. Les mutants individuels ont montré que lorsqu’un facteur pionnier ne parvenait pas à ouvrir l’ADN en un site donné, la fontaine correspondante s’affaiblissait ou disparaissait. Parallèlement, certaines fontaines restaient inchangées voire se renforçaient, et celles-ci coïncidaient souvent avec des enhancers qui s’activent plus tard dans le développement ou dans des tissus spécifiques, laissant penser que des fontaines peuvent aussi apparaître sur des éléments de contrôle « en attente » avant leur activation complète.
Des anneaux extrudeurs de boucles façonnent les fontaines
Les auteurs ont ensuite cherché ce qui pouvait créer physiquement ces motifs. Un candidat de premier plan est la cohesine, un complexe protéique en forme d’anneau connu pour saisir l’ADN et le bobiner en boucles par un processus d’extrusion de boucles. Les mesures montrent que la cohesine s’accumule à la base des fontaines, et que les régions d’enhancer contenant davantage de cohesine présentent des motifs de fontaine plus marqués. Des simulations informatiques d’une chaîne d’ADN flexible, dans lesquelles la cohesine se charge plus fréquemment à certains sites puis extrude des boucles vers l’extérieur, ont reproduit les formes observées de fontaines, à condition que le chargement aux enhancers soit plusieurs fois supérieur au reste du génome et que les deux côtés de chaque boucle se déplacent parfois de manière désynchronisée, par exemple en entrant en collision avec d’autres complexes protéiques.
Les fontaines apparaissent chez plusieurs espèces et au cours du cycle cellulaire
Pour savoir si les fontaines constituent un phénomène général, les chercheurs ont réanalysé des données de cellules souches embryonnaires de souris et d’une lignée de cellules sanguines murines. En se focalisant sur les régions enhancers de ces cellules, les cartes de type Hi-C montraient à nouveau des éventails de contacts en forme de fontaine, qui étaient fortement réduits lorsque la cohesine était épuisée expérimentalement. Lors de la division cellulaire, lorsque la cohesine quitte temporairement les chromosomes, les fontaines disparaissaient ; à mesure que les cellules entraient dans la phase de croissance suivante et que la cohesine se rechargeait, les fontaines réapparaissaient progressivement puis évoluaient en domaines et bandes plus familiers. Des fontaines liées aux enhancers ont également été rapportées chez des vers, des plantes, des champignons et des cellules immunitaires, disparaissant souvent lorsque la cohesine est retirée.
Ce que cela implique pour le développement précoce
En somme, les résultats suggèrent que, lorsqu’un embryon active ses propres gènes pour la première fois ou lorsqu’une cellule reconstruit son noyau après la division, le repliement des chromosomes commence au niveau des régions enhancers où la cohesine se charge plus facilement. Ces sites donnent naissance à des fontaines — éléments de repliement précoces centrés sur les enhancers qui, plus tard, mûrissent en structures 3D complexes observées dans les cellules pleinement développées. Pour le lecteur non spécialiste, le message clé est que les mêmes interrupteurs d’ADN qui décident quels gènes s’activent en début de vie contribuent aussi à façonner la structure même du génome, utilisant les anneaux de cohesine comme de petites machines qui bouclent et organisent les chromosomes dès leur réveil.
Citation: Galitsyna, A., Ulianov, S.V., Bazarevich, M. et al. Extrusion fountains are hallmarks of chromosome organization emerging upon zygotic genome activation. Nat Commun 17, 2787 (2026). https://doi.org/10.1038/s41467-026-69105-9
Mots-clés: activation du génome zygotique, repliement des chromosomes, extrusion de boucles par cohesine, enhancers, développement embryonnaire