Clear Sky Science · de
Extrusionsfontänen sind Kennzeichen der Chromosomenorganisation, die bei der zygotischen Genaktivierung entstehen
Wie das frühe Leben seine DNA anschaltet
Jeder tierische Embryo steht vor derselben Herausforderung: anfangs läuft alles mit Molekülen der Mutter, doch bald muss die eigene DNA erwachen und das Wachstum selbst steuern. Diese Studie fragt, was mit der physikalischen Faltung der Chromosomen in diesem entscheidenden Moment geschieht, und entdeckt ein überraschendes neues Strukturmuster, das die Forschenden „Fontänen“ tauften und das offenbar markiert, wo wichtige Schaltstellen im Genom aktiviert werden.
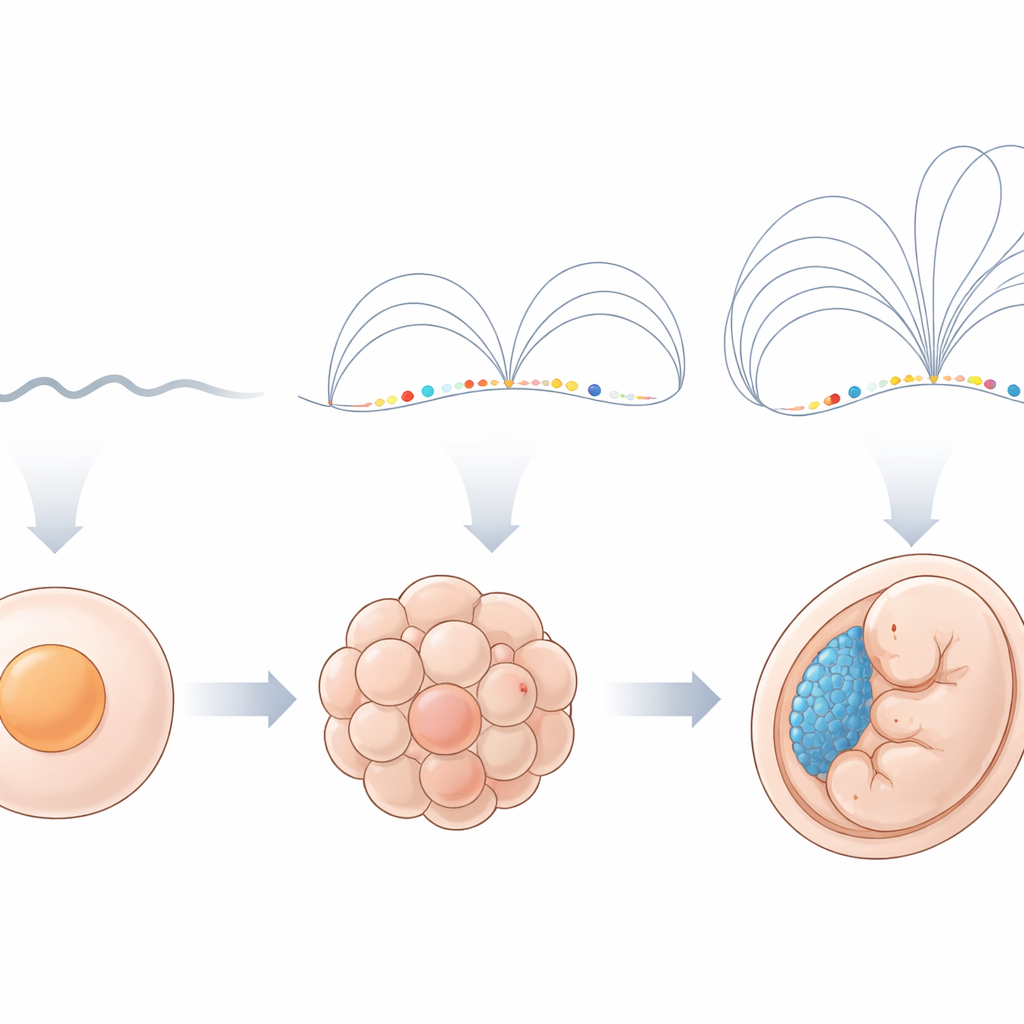
Ein ruhiges Genom erwacht plötzlich
Bei Zebrafischen und vielen anderen Tieren schalten die eigenen Gene des Embryos in einer Ausbruchswelle an, die zygotische Genaktivierung genannt wird. Davor wirken die Chromosomen in Hi‑C‑Messungen relativ unspektakulär; Hi‑C erfasst, welche DNA‑Stücke im 3D‑Raum nahe beieinander liegen. Nach der Aktivierung sieht man typischerweise vertraute Muster wie Domänen und Schleifen, die zeigen, wie die DNA verpackt ist. Die Autorinnen und Autoren sammelten Hi‑C‑Daten aus Spermium und mehreren frühen Stadien von Zebrafisch‑Embryonen, um diesen Übergang im Detail zu beobachten. Sie bestätigten, dass vor der Aktivierung wenige erkennbare Merkmale vorhanden sind, doch kurz danach größere Kompartimente und lokalere Strukturen entstehen.
Fontänenmuster markieren frühe Kontrollregionen
Bei genauer Betrachtung der ersten lokalen Strukturen entdeckte das Team ausgeprägte Kontaktmuster, die sie Fontänen nennen. In einer Hi‑C‑Karte sieht eine Fontäne wie eine schmale Basis an einer einzigen DNA‑Stelle aus, die sich zu einem Fächer aus verstärkten Kontakten aufweitet, je weiter man entlang des Chromosoms geht. Diese Formen unterscheiden sich von den später sichtbaren kastenförmigen Domänen und streifenartigen Mustern. Mit einem automatisierten Erkennungswerkzeug fanden die Autorinnen und Autoren kurz nach der Genaktivierung im Zebrafisch über tausend solcher Fontänen und ähnliche Muster in frühen Embryonen von Frosch und Medaka. Auffällig ist, dass Fontänen oft in DNA‑Regionen entstehen, die offen sind, früh in der Entwicklung aktiv werden und mit chemischen Marken verziert sind, die für Enhancer typisch sind — regulatorische Schalter, die benachbarte Gene beim Einschalten helfen — statt an Promotoren, wo Gene tatsächlich abgelesen werden.
Wichtige Starterproteine bereiten Stellen vor, an denen Fontänen entstehen
Um zu prüfen, ob Fontänen tatsächlich von diesen frühen Schaltern abhängen, konzentrierten sich die Forschenden auf „Pionier“‑Transkriptionsfaktoren — spezielle Proteine, die eng verpackte DNA öffnen können. Beim Zebrafisch sind drei solcher Faktoren (Pou5f3, Sox19b und Nanog) bekannt dafür, frühe Enhancer einzurichten. Fehlen diese drei Proteine im Embryo, verschwinden die charakteristischen Fontänen an den Regionen, in denen Chromatin‑Zugänglichkeit und Enhancer‑Markierungen verloren gehen, weitgehend. Einzelmutanten zeigten, dass, wenn ein Pionierfaktor eine Stelle nicht öffnet, die Fontänen an dieser Stelle schwächer werden oder verschwinden. Gleichzeitig blieben einige Fontänen unverändert oder wurden sogar stärker; diese lagen häufig an Enhancern, die später in der Entwicklung oder gewebespezifisch aktiv werden, was darauf hindeutet, dass Fontänen auch an „wartenden“ Kontrolllementen erscheinen können, bevor diese vollständig eingeschaltet sind.
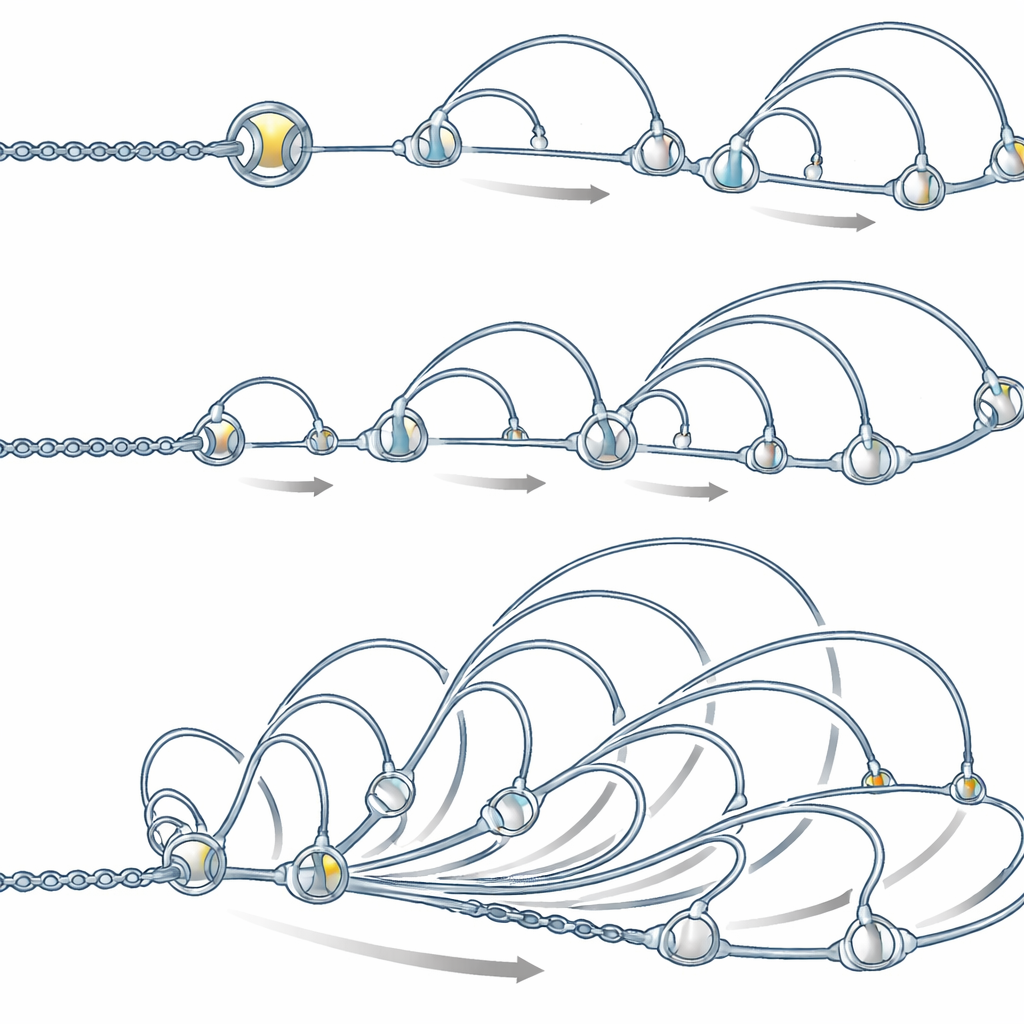
Loop‑extrudierende Ringe formen die Fontänen
Die Autorinnen und Autoren fragten dann, was diese Muster physikalisch erzeugen könnte. Ein Hauptkandidat ist Cohesin, ein ringförmiger Proteinkomplex, der DNA greifen und in einer als Loop‑Extrusion bezeichneten Bewegung zu Schleifen aufrollen kann. Messungen zeigten, dass Cohesin sich an den Fontänenbasen anreichert und dass Enhancer‑Regionen mit mehr Cohesin stärkere Fontänenmuster aufweisen. Computersimulationen einer flexiblen DNA‑Kette, bei denen Cohesin an bestimmten Stellen häufiger geladen wird und dann Schleifen nach außen extrudiert, reproduzierten die beobachteten Fontänenformen, vorausgesetzt, das Laden an Enhancern ist mehrere Male höher als im restlichen Genom und die beiden Seiten jeder Schleife bewegen sich manchmal asynchron, etwa durch Zusammenstöße mit anderen Proteinkomplexen.
Fontänen treten über Arten und Zellzyklen hinweg auf
Um zu prüfen, ob Fontänen ein allgemeines Phänomen sind, analysierten die Forschenden Daten aus Maus‑embryonalen Stammzellen und einer Maus‑Blutzelllinie neu. Fokussierten sie auf Enhancer‑Regionen in diesen Zellen, zeigten Hi‑C‑ähnliche Karten erneut fächerartige Kontaktmuster wie Fontänen, und diese gingen stark zurück, wenn Cohesin experimentell entfernt wurde. Während der Zellteilung, wenn Cohesin vorübergehend die Chromosomen verlässt, verschwanden die Fontänen; beim Übergang in die nächste Wachstumsphase und dem Wiedereinladen von Cohesin tauchten die Fontänen allmählich wieder auf und entwickelten sich später zu den vertrauteren Domänen und Streifen. Ähnliche enhancer‑verknüpfte Fontänen wurden auch in Würmern, Pflanzen, Pilzen und Immunzellen berichtet, oft mit dem Verschwinden, wenn Cohesin entfernt wird.
Was das für die frühe Entwicklung bedeutet
Insgesamt deuten die Befunde darauf hin, dass, wenn ein Embryo erstmals seine eigenen Gene anschaltet oder eine Zelle nach der Teilung ihren Zellkern wiederaufbaut, die Chromosomenfaltung in Enhancer‑Regionen beginnt, an denen Cohesin leichter geladen wird. Diese Stellen erzeugen Fontänen — frühe, enhancerzentrierte Faltungselemente, die sich später zu den komplexen 3D‑Strukturen entwickeln, die in ausgereiften Zellen sichtbar sind. Für eine allgemein verständliche Zusammenfassung lautet die Kernbotschaft: Dieselben DNA‑Schalter, die entscheiden, welche Gene im frühen Leben eingeschaltet werden, helfen auch, die Form des Genoms zu gestalten, indem Cohesinringe als winzige Maschinen Schleifen bilden und Chromosomen von dem Moment an organisieren, in dem sie erwachen.
Zitation: Galitsyna, A., Ulianov, S.V., Bazarevich, M. et al. Extrusion fountains are hallmarks of chromosome organization emerging upon zygotic genome activation. Nat Commun 17, 2787 (2026). https://doi.org/10.1038/s41467-026-69105-9
Schlüsselwörter: zygotische Genaktivierung, Chromosomenfaltung, Cohesin-Loop-Extrusion, Enhancer, Embryonalentwicklung