Clear Sky Science · fr
La dégradation déclenchée par l’acétylation de MSX1 compromet le développement du palais
Pourquoi cela compte pour les bébés et les familles
La fente palatine est l’un des défauts congénitaux les plus fréquents, affectant la respiration, l’alimentation et, plus tard, la parole des nouveau-nés. Les cliniciens savent que des facteurs génétiques et environnementaux augmentent le risque, mais la manière précise dont ces influences perturbent la formation du palais restait mystérieuse. Cette étude met au jour un « interrupteur » moléculaire caché au sein des cellules faciales qui décide si elles survivent assez longtemps pour permettre la fermeture correcte du palais, offrant de nouvelles pistes pour la prévention et le traitement précoce.
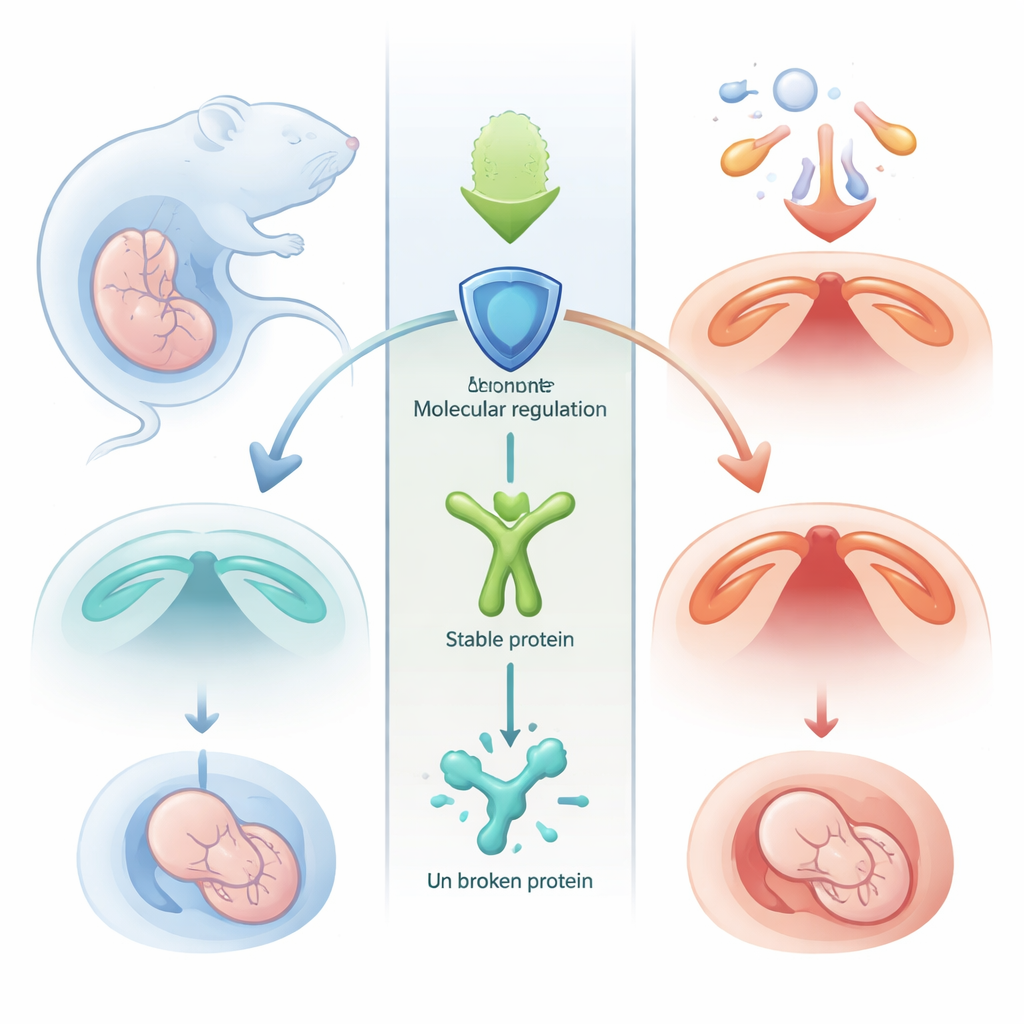
Une chorégraphie délicate dans la bouche en développement
Au cours du début de la grossesse, deux volets de tissu dans la bouche de l’embryon doivent croître l’un vers l’autre puis fusionner pour former le toit de la bouche. Ce processus exige un équilibre fin entre prolifération cellulaire et mort cellulaire. Si trop de cellules du palais meurent au mauvais moment, les volets ne se rencontrent pas, laissant une ouverture appelée fente palatine. Les auteurs se sont focalisés sur une protéine nommée MSX1, connue depuis longtemps comme un coordinateur majeur du développement facial, et ont cherché comment son niveau est régulé durant cette fenêtre critique.
Quand une protéine utile est marquée pour destruction
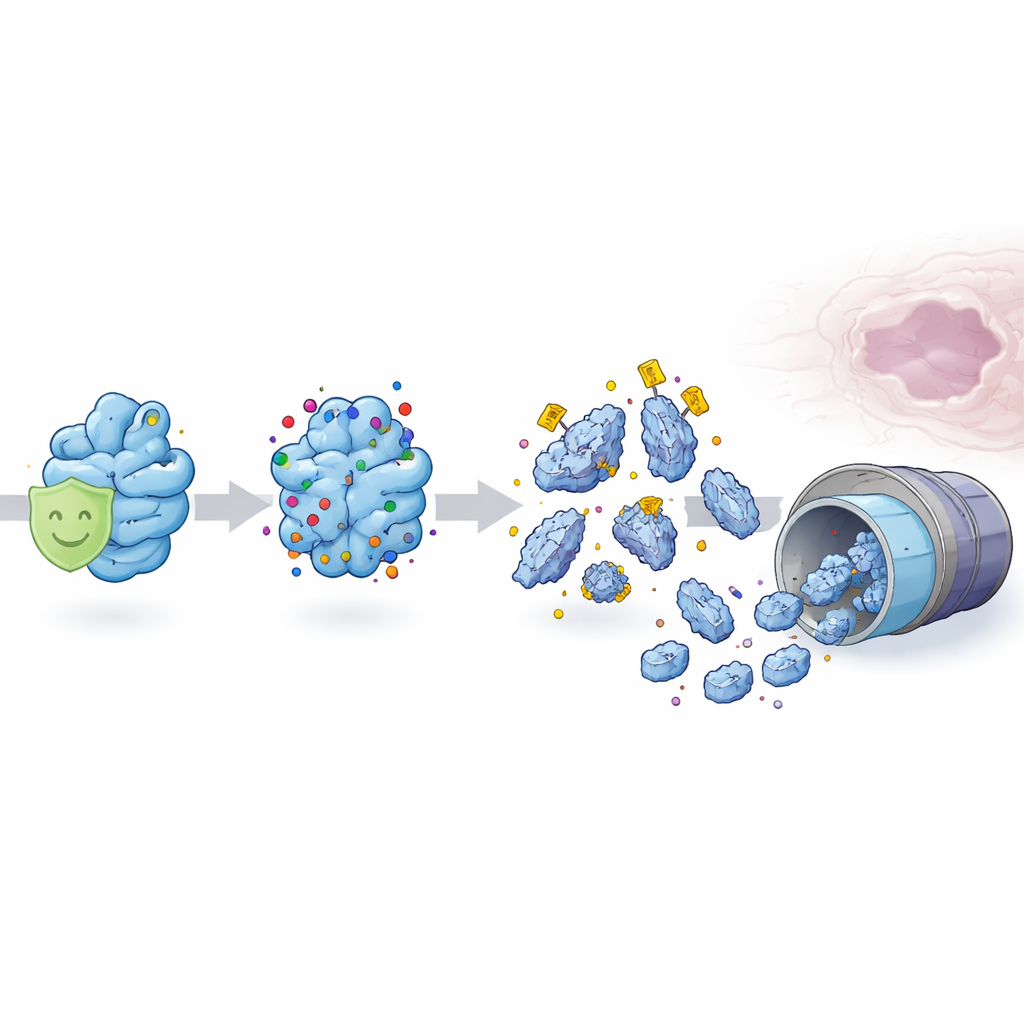
Les protéines à l’intérieur des cellules sont constamment marquées, remaniées et parfois détruites après leur synthèse. L’équipe a découvert que MSX1 porte une marque chimique spécifique — un groupe acétyle — sur un site qui agit comme un signal d’élimination. Quand ce marquage est ajouté, MSX1 devient instable et est rapidement dégradée par les mécanismes de recyclage protéique de la cellule. Dans les cellules du palais de souris, un excès de ce marquage réduit drastiquement les niveaux de protéine MSX1 alors même que le gène MSX1 reste inchangé, montrant que le problème ne vient pas du code ADN mais de la gestion de la protéine après traduction.
L’enzyme gardienne qui maintient les cellules en vie
Une autre protéine, une enzyme appelée SIRT1, enlève normalement le groupe acétyle de MSX1 et contribue à le stabiliser. Chez les embryons sains, SIRT1 et MSX1 coexistent dans le noyau cellulaire, et l’activité de SIRT1 protège MSX1 d’une destruction prématurée. En utilisant un modèle de fente palatine induite par une forte dose d’acide rétinoïque tout-trans — un dérivé de la vitamine A pouvant agir comme médicament ou polluant — les chercheurs ont constaté une chute marquée des niveaux de SIRT1. Avec cette protection affaiblie, MSX1 devient hyperacétylé, plus fortement marqué pour la dégradation, et rapidement éliminé. Le résultat est une vague de mort cellulaire excessive dans le tissu palatin et un échec de la fusion des volets.
Tester des « leurres » moléculaires pour sauver le palais
Pour savoir s’ils pouvaient contrer ce dommage, les scientifiques ont conçu deux versions de MSX1 : une qui ne peut pas être acétylée au site clé et une qui mime une acétylation permanente. En cultures cellulaires, la version non acétylable est restée stable et a fortement protégé les cellules de la mort, tandis que le mimétique d’acétylation a aggravé la situation. Lorsqu’ils ont administré un excès de SIRT1, MSX1 normal ou MSX1 résistant à l’acétylation à des souris enceintes exposées à l’acide rétinoïque, la gravité des fentes palatines a diminué et moins de cellules du palais ont subi la mort cellulaire. Ces expérimentations montrent que le contrôle d’une seule marque chimique sur MSX1 peut modifier de façon significative le cours du développement du palais.
Ce que cela pourrait signifier pour les soins futurs
Pour les non-spécialistes, le message principal est que cette recherche identifie un interrupteur moléculaire précis reliant les expositions environnementales à un défaut congénital fréquent. Plutôt que d’altérer la fonction de MSX1 au niveau du gène, l’acétylation régule la durée de vie de la protéine MSX1, supprimant silencieusement son rôle protecteur lorsque le marquage devient excessif. En renforçant l’activité de SIRT1 ou en concevant des médicaments qui empêchent la sur-marque de MSX1, il pourrait un jour être possible de réduire le risque de fente palatine dans des grossesses à haut risque connues. Ce travail suggère également que la mesure de MSX1 modifié dans des échantillons prénataux pourrait aider à identifier plus tôt les fœtus vulnérables, ouvrant la voie à une surveillance plus ciblée et, éventuellement, à des thérapies préventives.
Citation: Meng, L., You, J., Zhang, Z. et al. Acetylation-triggered degradation of MSX1 impairs palatal development. Cell Death Discov. 12, 156 (2026). https://doi.org/10.1038/s41420-026-03018-w
Mots-clés: fente palatine, développement embryonnaire, acétylation des protéines, MSX1, SIRT1