Clear Sky Science · es
Degradación de MSX1 provocada por acetilación perjudica el desarrollo palatal
Por qué importa esto para bebés y familias
El paladar hendido es uno de los defectos congénitos más comunes y afecta la respiración, la alimentación y, más adelante, el habla de los recién nacidos. Los médicos saben que tanto los genes como las exposiciones ambientales pueden aumentar el riesgo, pero cómo exactamente estas influencias dañan el paladar en desarrollo ha sido un enigma. Este estudio descubre un “interruptor” molecular oculto dentro de las células faciales que decide si sobreviven el tiempo suficiente para que el paladar cierre correctamente, ofreciendo ideas nuevas para la prevención y el tratamiento precoz.
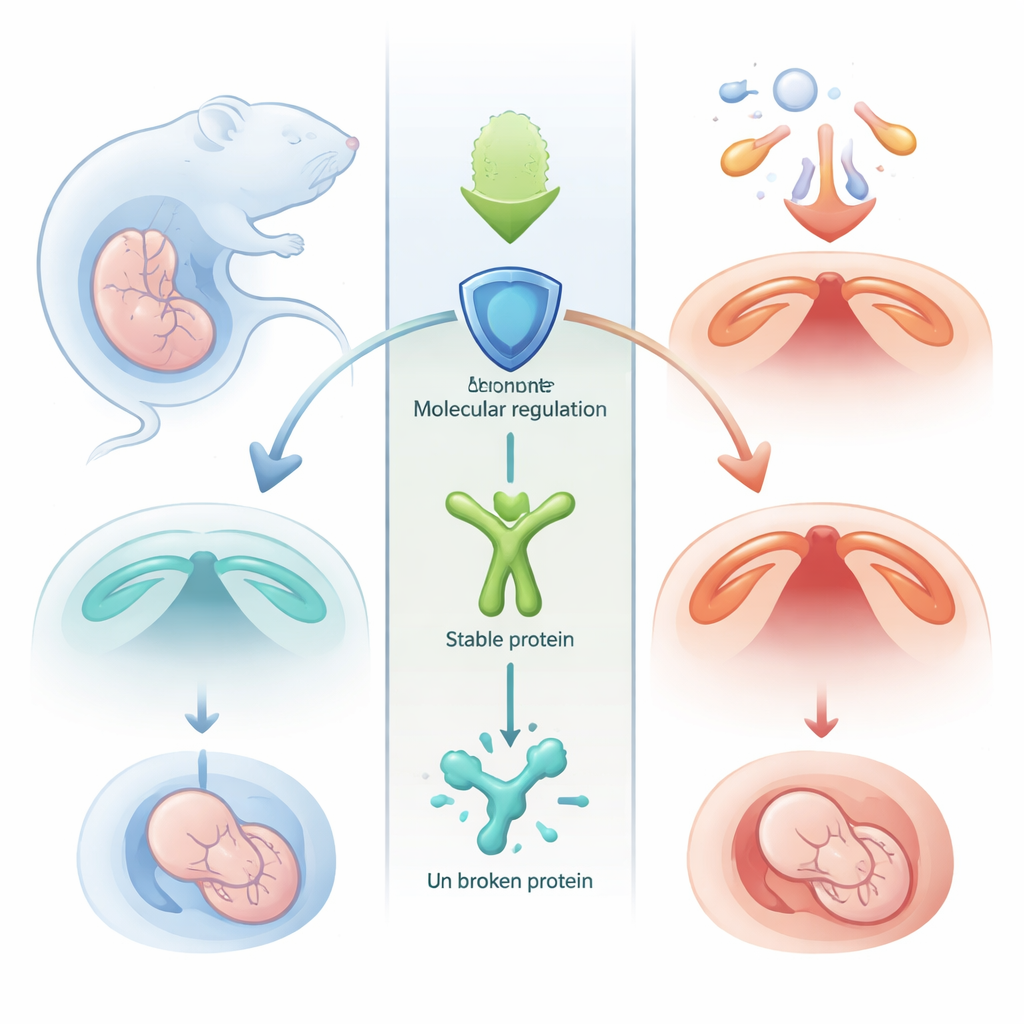
Una danza delicada en la boca en desarrollo
Durante el inicio del embarazo, dos repisas de tejido en la boca del embrión deben crecer una hacia la otra y fusionarse para formar el techo de la boca. Este proceso exige un equilibrio cuidadoso entre el crecimiento celular y la muerte celular. Si demasiadas células del paladar mueren en el momento equivocado, las repisas no llegan a juntarse, dejando una abertura conocida como paladar hendido. Los autores se centraron en una proteína llamada MSX1, conocida desde hace tiempo como coordinadora clave del desarrollo facial, y preguntaron cómo se regulan sus niveles durante esta ventana crítica.
Cuando una proteína útil recibe la marca de destrucción
Las proteínas dentro de las células están siendo etiquetadas, remodeladas y a veces degradadas constantemente tras su síntesis. El equipo descubrió que MSX1 porta una etiqueta química específica—un grupo acetilo—en un sitio que actúa como marca de desecho. Cuando se añade esta etiqueta, MSX1 se vuelve inestable y es degradada rápidamente por la maquinaria recicladora de proteínas de la célula. En células del paladar de ratón, el exceso de esta acetilación reduce drásticamente los niveles de la proteína MSX1 aunque el gen MSX1 subyacente permanezca sin cambios, lo que revela que el problema no está en el código del ADN sino en cómo se gestiona la proteína después de sintetizarse.
La enzima guardiana que mantiene vivas a las células
Otra proteína, una enzima llamada SIRT1, normalmente elimina la etiqueta acetilo de MSX1 y ayuda a mantenerla estable. En embriones sanos, SIRT1 y MSX1 coexisten en el núcleo celular, y la actividad de SIRT1 protege a MSX1 de una destrucción prematura. Usando un modelo de paladar hendido inducido por una dosis alta de ácido retinoico todo-trans—un derivado de la vitamina A que puede comportarse como fármaco o contaminante—los investigadores observaron que los niveles de SIRT1 caen bruscamente. Con este guardián debilitado, MSX1 queda sobreacetilada, más fuertemente marcada para su degradación y es rápidamente eliminada. El resultado es una oleada de muerte celular excesiva en el tejido palatal y el fracaso de las repisas para fusionarse.
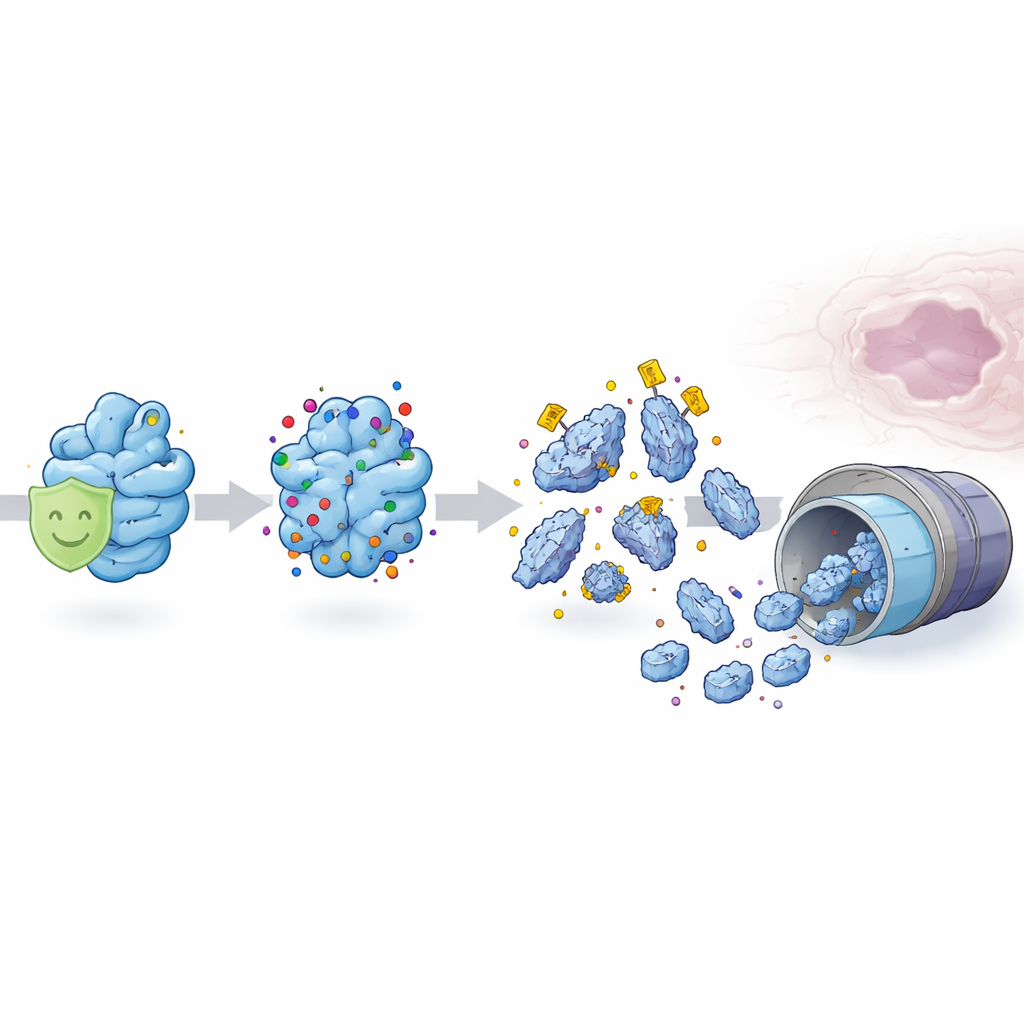
Probando “señuelos” moleculares para rescatar el paladar
Para ver si podían contrarrestar este daño, los científicos diseñaron dos versiones de MSX1: una que no podía ser acetilada en el sitio clave y otra que imitaba la acetilación constante. En experimentos celulares, la versión no acetilable se mantuvo estable y protegió con fuerza a las células de la muerte, mientras que el mimético de acetilación empeoró la situación. Cuando administraron SIRT1 adicional, MSX1 normal o MSX1 resistente a la acetilación a hembras embarazadas de ratón expuestas al ácido retinoico, la gravedad del paladar hendido se redujo y menos células del paladar sufrieron muerte celular. Estas pruebas demostraron que controlar esta única marca química en MSX1 puede influir de manera significativa en el desarrollo del paladar.
Qué podría significar esto para la atención futura
Para los no especialistas, el mensaje clave es que esta investigación identifica un interruptor molecular preciso que vincula las exposiciones ambientales con un defecto congénito común. En lugar de cambiar lo que hace MSX1 como gen, la acetilación controla cuánto tiempo sobrevive la proteína MSX1, eliminando silenciosamente su función protectora cuando el etiquetado es excesivo. Al incrementar la actividad de SIRT1 o diseñar fármacos que impidan que MSX1 se sobreetiquete, quizá algún día sea posible reducir el riesgo de paladar hendido en embarazos conocidos como de alto riesgo. El trabajo también sugiere que medir MSX1 modificado en muestras prenatales podría ayudar a identificar fetos vulnerables antes, abriendo la puerta a una supervisión más dirigida y, eventualmente, a terapias preventivas.
Cita: Meng, L., You, J., Zhang, Z. et al. Acetylation-triggered degradation of MSX1 impairs palatal development. Cell Death Discov. 12, 156 (2026). https://doi.org/10.1038/s41420-026-03018-w
Palabras clave: labio leporino, desarrollo embrionario, acetilación de proteínas, MSX1, SIRT1