Clear Sky Science · fr
CHK1 est un régulateur essentiel de la réplication de l’ADN dans les cellules humaines
Pourquoi il est crucial que la copie de l’ADN reste sur la bonne voie
Chaque fois qu’une cellule de notre organisme se divise, elle doit copier l’intégralité de son ADN—des milliards de « lettres » chimiques—sans introduire d’erreurs dangereuses. Si ce processus de copie déraille, il peut en résulter des chromosomes brisés, des mutations et, in fine, des maladies comme le cancer. Cette étude porte sur une protéine nommée CHK1, un chef d’orchestre moléculaire qui aide à maintenir l’ordre lors de la réplication de l’ADN. En désactivant CHK1 avec une précision inhabituelle, les chercheurs montrent à quel point ce gardien est central pour la vie et la santé des cellules humaines.
Un contrôleur moléculaire du trafic pour la copie de l’ADN
La réplication de l’ADN débute à de nombreux points le long des chromosomes et progresse via des structures appelées fourches de réplication, où la double hélice est ouverte et dupliquée. CHK1 fait partie d’une voie de signalisation qui veille sur ces fourches, les ralentissant ou arrêtant le cycle cellulaire lorsque des problèmes surviennent. Les travaux précédents étudiaient surtout CHK1 en situation de stress extrême, par exemple après chimiothérapie ou irradiation, souvent à l’aide de médicaments qui touchent aussi d’autres cibles. Il restait donc difficile de savoir quel rôle joue CHK1 lors de la réplication « normale » de l’ADN dans des cellules non stressées.
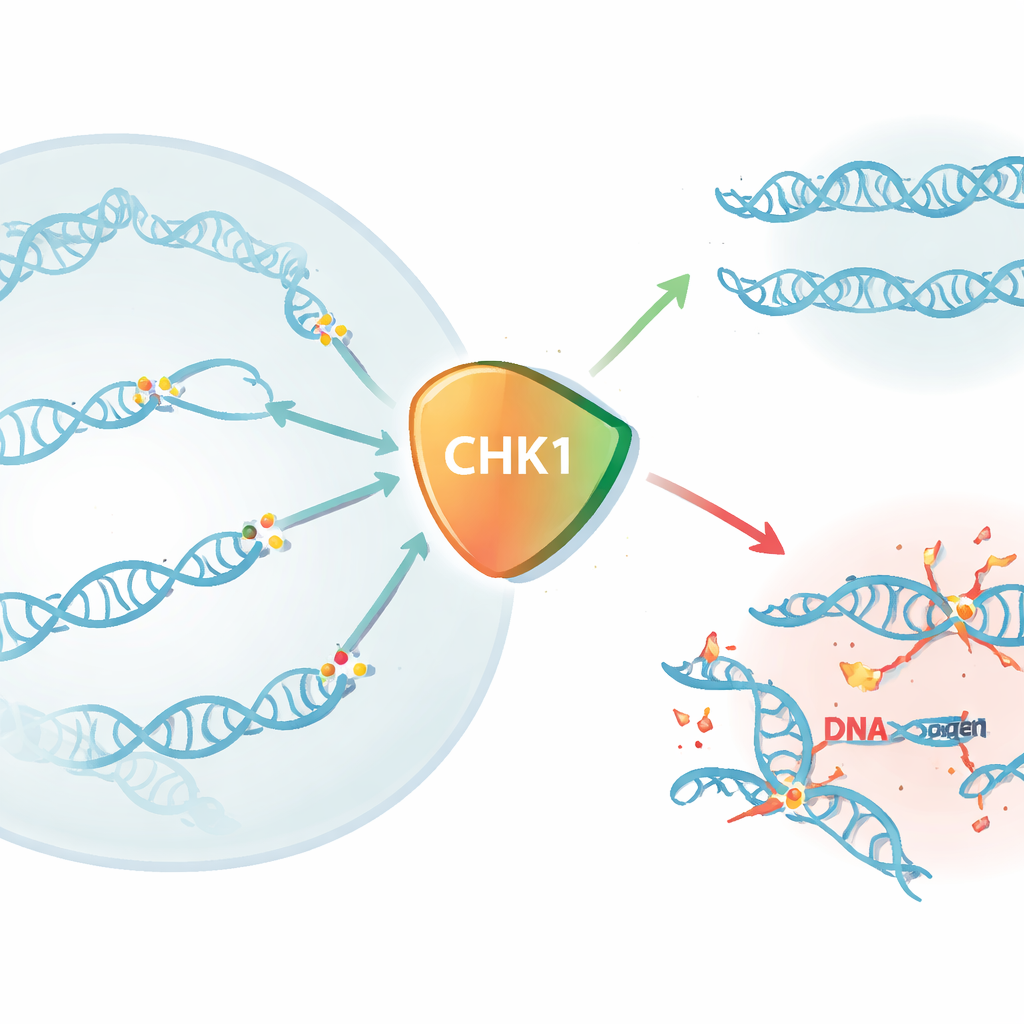
Une élimination rapide de CHK1 montre son importance
Pour répondre à cette question, les auteurs ont utilisé le système dTAG, un artifice génétique qui leur permet de marquer la protéine CHK1 pour qu’elle soit détruite en quelques minutes après l’ajout d’une petite molécule au milieu de culture. Dans des lignées cellulaires humaines, plus des trois quarts de CHK1 avaient disparu en 15 minutes, et presque toute la protéine était éliminée en une demi-heure. Lorsque CHK1 était supprimé de manière aiguë, les cellules perdaient rapidement la capacité de former des colonies et manifestaient une chute marquée de viabilité en 16 heures, avec une mortalité quasi complète à 48 heures—souvent en l’espace d’un seul cycle cellulaire. Seule la réintroduction d’une CHK1 pleinement fonctionnelle, conservant son activité enzymatique et ses régions régulatrices clés, permettait de sauver les cellules, prouvant que l’activité de kinase de CHK1 et son activation par une protéine en amont nommée ATR sont toutes deux essentielles à la survie.
Quand CHK1 disparaît, les fourches de réplication s’effondrent
Après l’épuisement de CHK1, les marqueurs de dommages à l’ADN et de stress de réplication ont rapidement augmenté. Les chercheurs ont observé davantage de ruptures de brins d’ADN avec des essais de type « comet » et une activation accrue de protéines qui s’associent à l’ADN simple brin exposé. Parallèlement, les cellules se retrouvaient bloquées en phase S (réplication) : elles pouvaient initier la réplication, mais leurs fourches ralentissaient, s’effondraient et ne parvenaient pas à terminer le travail. Ces cellules ne pouvaient alors pas entrer en mitose, la phase où les chromosomes sont séparés entre les cellules filles. Des inhibiteurs pharmacologiques de CHK1 produisaient des effets très similaires, et ces phénomènes apparaissaient tant dans des cellules d’origine tumorale que dans des cellules humaines non transformées, ce qui souligne que CHK1 n’est pas seulement un système de secours pour les cellules stressées mais une exigence fondamentale de la réplication normale de l’ADN.
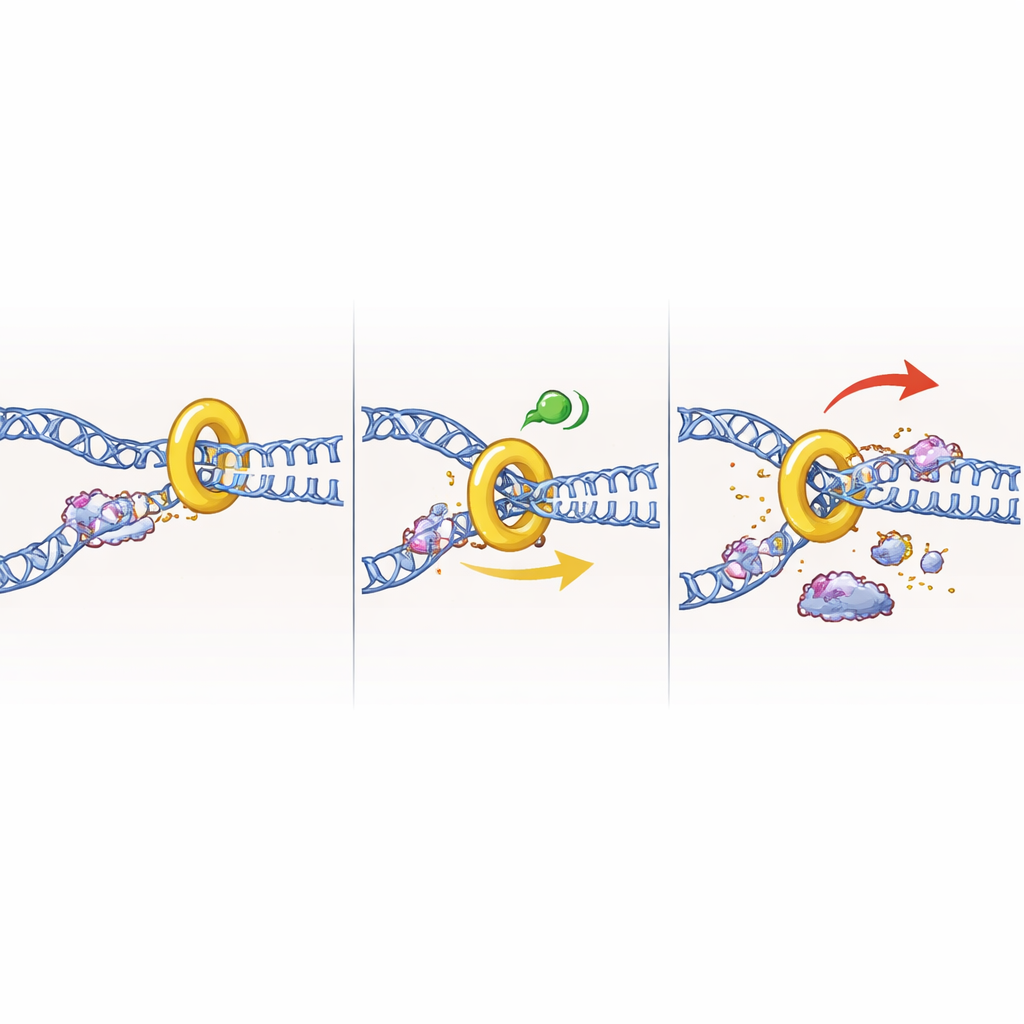
Un rôle inattendu avant même le début de la copie de l’ADN
Le résultat peut-être le plus surprenant est venu quand l’équipe a bloqué les cellules à la frontière entre la phase pré-réplicative (G1) et la phase S, un moment où la synthèse massive d’ADN n’a pas encore commencé. Intuitivement, on pourrait s’attendre à ce que la perte de CHK1 à ce stade soit sans conséquence, puisque les fourches de réplication ne se sont pas encore formées. Au contraire, supprimer CHK1 dans ces cellules arrêtées en G1/S déclenchait tout de même de puissants signaux de dommages à l’ADN et une perte de viabilité, alors même que les cellules étaient empêchées d’entrer en phase S. Des expériences complémentaires suggèrent que CHK1 bride normalement l’activation prématurée des origines de réplication et le déroulement de l’ADN par les hélicases. En l’absence de CHK1, ce mécanisme semblait initier un déroulement inapproprié, créant des segments d’ADN exposé et fragilisés qui aboutissaient à des cassures. Inhiber d’autres enzymes qui déclenchent l’allumage des origines apportait un secours partiel contre ces dommages, ce qui soutient ce modèle.
Ce que cela signifie pour la santé et la thérapie
Dans l’ensemble, ce travail présente CHK1 comme un gestionnaire constant et essentiel de la réplication de l’ADN, plutôt que comme une protéine qui n’intervient qu’en cas de problème. CHK1 agit avant le démarrage de la copie de l’ADN pour empêcher une activation inconsidérée des origines, et continue de fonctionner pendant la phase S en adaptant la vitesse de l’hélicase déroulant l’ADN à celle des enzymes de copie, afin que les fourches progressent en sécurité. Lorsque CHK1 est éliminé, cette coordination échoue, les fourches s’effondrent, les cassures d’ADN s’accumulent et les cellules meurent rapidement. Pour un lecteur non spécialiste, le message clé est que CHK1 veille à ce que chaque nouvelle copie du génome soit produite soigneusement et complètement. Ce rôle central explique pourquoi CHK1 est devenu une cible prometteuse en thérapie anticancéreuse—le bloquer peut pousser des cellules tumorales déjà stressées au-delà du point de rupture—mais aussi pourquoi de tels traitements doivent être employés avec prudence, compte tenu de l’importance fondamentale de CHK1 pour la survie des cellules normales en division.
Citation: Li, S., Zhu, D., Tang, M. et al. CHK1 is an integral regulator of DNA replication in human cells. Cell Death Dis 17, 375 (2026). https://doi.org/10.1038/s41419-026-08624-1
Mots-clés: Réplication de l’ADN, cycle cellulaire, stabilité du génome, kinase de point de contrôle, stress de réplication