Clear Sky Science · de
CHK1 ist ein integraler Regulator der DNA-Replikation in menschlichen Zellen
Warum es wichtig ist, das DNA-Kopieren auf Kurs zu halten
Jedes Mal, wenn sich eine Zelle in unserem Körper teilt, muss sie ihre gesamte DNA — Milliarden chemischer „Buchstaben“ — fehlerfrei kopieren. Wenn dieser Kopiervorgang schiefgeht, können Chromosomen beschädigt, Mutationen erzeugt und letztlich Krankheiten wie Krebs ausgelöst werden. In dieser Studie steht ein Protein namens CHK1 im Mittelpunkt, ein molekularer Verkehrsleiter, der das geordnete Kopieren der DNA unterstützt. Indem die Forschenden CHK1 mit ungewöhnlicher Präzision ausschalten, zeigen sie, wie zentral dieser Wächter für Leben und Gesundheit menschlicher Zellen ist.
Ein molekularer Verkehrsleiter für das DNA-Kopieren
Die DNA-Replikation beginnt an vielen Startpunkten entlang der Chromosomen und läuft an Strukturen ab, den Replikationsgabeln, wo die Doppelhelix geöffnet und verdoppelt wird. CHK1 gehört zu einem Signalweg, der diese Gabeln überwacht und sie bei Problemen verlangsamt oder den Zellzyklus anhält. Frühere Arbeiten untersuchten CHK1 meist unter extremem Stress, etwa nach Chemotherapie oder Bestrahlung, oft mithilfe von Wirkstoffen, die auch andere Ziele beeinflussen. Daher blieb unklar, welche Rolle CHK1 während des alltäglichen, „normalen“ DNA-Kopierens in unverstörten Zellen spielt.
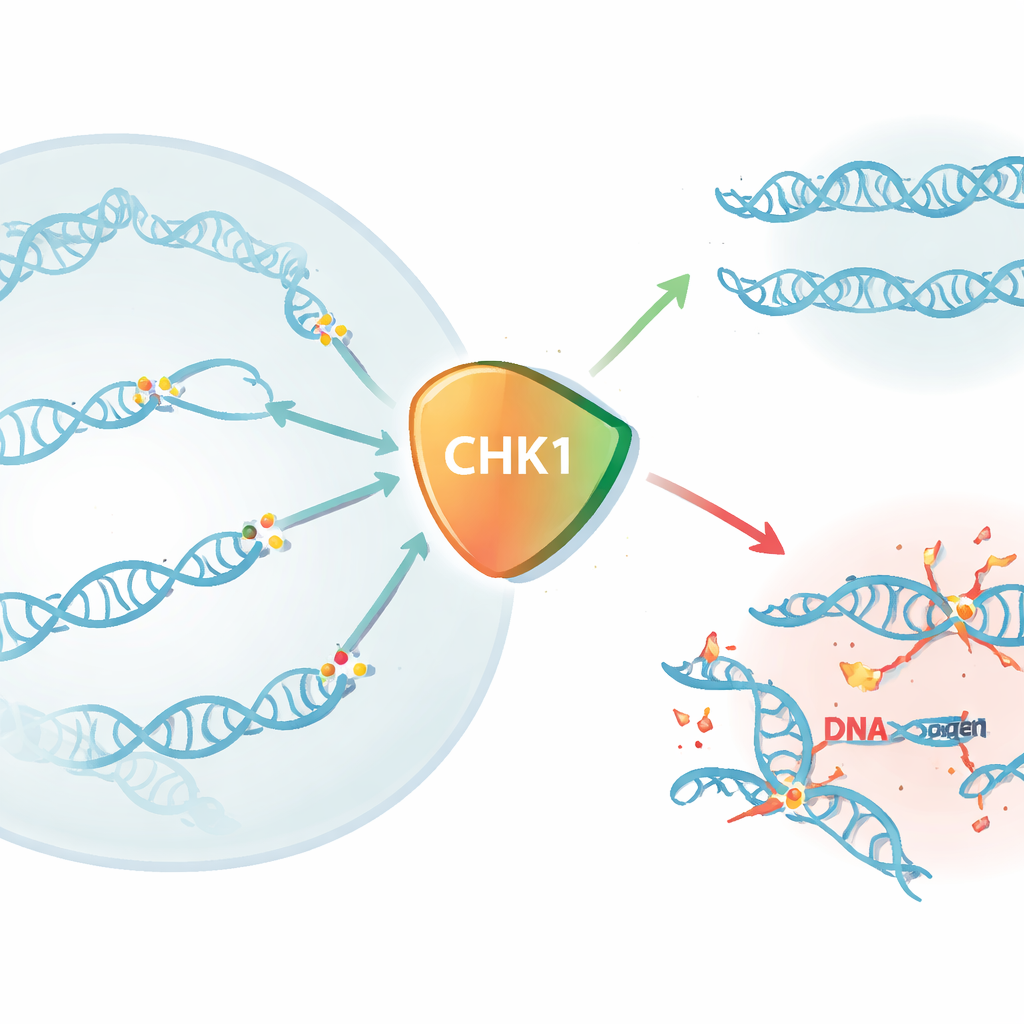
Schnelles Entfernen von CHK1 zeigt seine Bedeutung
Um das zu klären, verwendeten die Autorinnen und Autoren das dTAG-System, einen genetischen Trick, mit dem sie das CHK1-Protein so markieren können, dass es innerhalb von Minuten durch Zugabe eines kleinen Moleküls zur Zellkultur zerstört wird. In humanen Zelllinien war mehr als drei Viertel von CHK1 innerhalb von 15 Minuten verschwunden, und nahezu alles war nach einer halben Stunde abgebaut. Wurde CHK1 auf diese Weise akut entfernt, verloren die Zellen schnell die Fähigkeit, Kolonien zu bilden, und zeigten innerhalb von 16 Stunden einen starken Abfall der Lebensfähigkeit, mit nahezu kompletter Zellsterblichkeit nach 48 Stunden — oft bereits innerhalb eines einzigen Zellzyklus. Nur die Wiedereinführung einer voll funktionsfähigen CHK1-Variante, mit intakter enzymatischer Aktivität und den wichtigen regulatorischen Bereichen, konnte die Zellen retten. Das beweist, dass die Kinase-Aktivität von CHK1 und seine Aktivierung durch ein vorgelagertes Protein namens ATR beide für das Überleben essenziell sind.
Wenn CHK1 fehlt, brechen Replikationsgabeln zusammen
Nachdem CHK1 erschöpft war, stiegen Marker für DNA-Schäden und Replikationsstress stark an. Die Forschenden beobachteten mehr DNA-Strangbrüche in Comet-Assays und eine verstärkte Aktivierung von Proteinen, die Einzelstrang-DNA bedecken. Gleichzeitig blieben die Zellen in der DNA-Kopierphase (S-Phase) stecken: Sie konnten die Replikation starten, doch ihre Replikationsgabeln verlangsamten sich, kollabierten und konnten die Replikation nicht abschließen. Diese Zellen konnten anschließend nicht in die Mitose eintreten, die Phase, in der Chromosomen auf Tochterzellen verteilt werden. Pharmakologische CHK1-Inhibitoren erzeugten sehr ähnliche Muster, und die Effekte traten sowohl in krebsabgeleiteten als auch in nicht transformierten humanen Zellen auf. Das unterstreicht, dass CHK1 nicht nur ein Reservemechanismus für gestresste Zellen ist, sondern eine Kernanforderung für die normale DNA-Replikation.
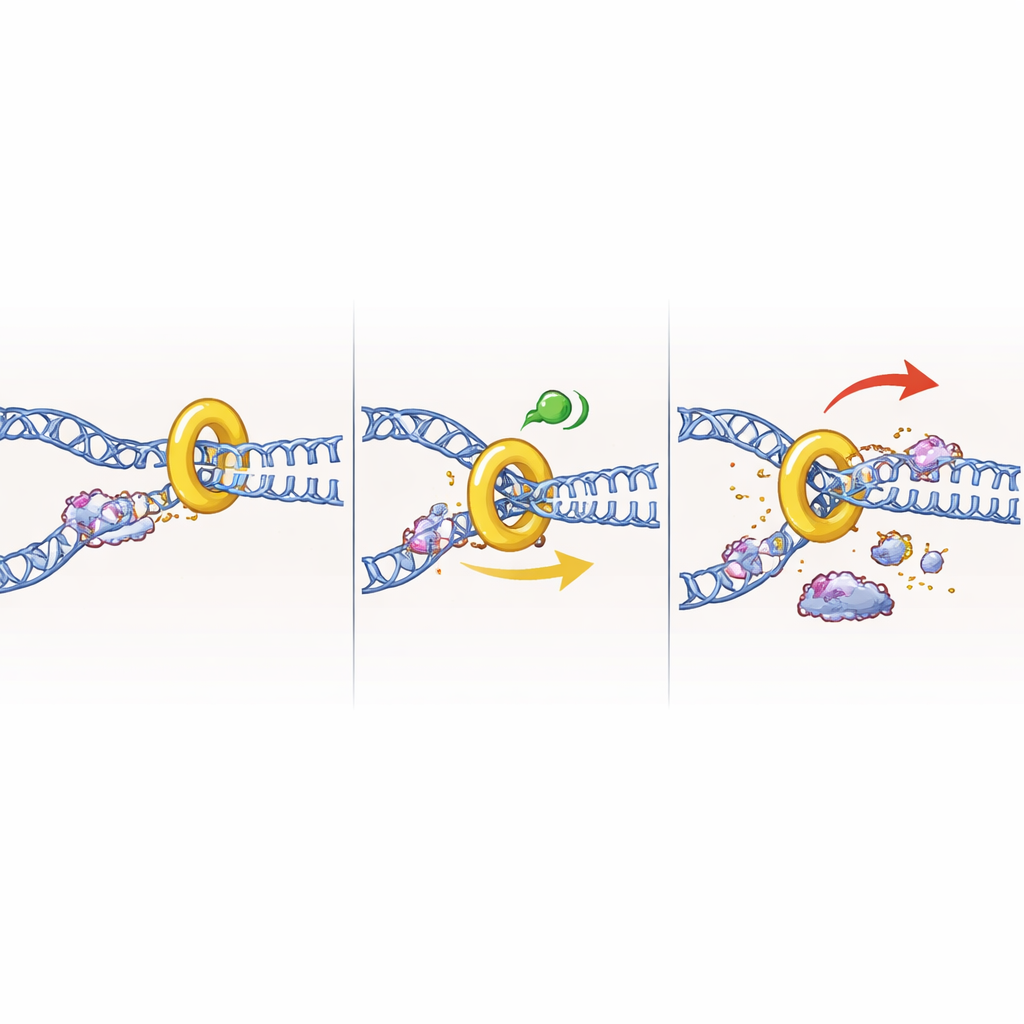
Eine unerwartete Rolle noch bevor das DNA-Kopieren beginnt
Die vielleicht überraschendste Beobachtung ergab sich, als das Team Zellen an der Grenze zwischen der Vorreplikationsphase (G1) und der S-Phase blockierte, einem Punkt, an dem die Großzahl der DNA-Synthese noch nicht begonnen hat. Intuitiv könnte man erwarten, dass das Fehlen von CHK1 hier harmlos ist, da Replikationsgabeln noch nicht gebildet wurden. Stattdessen löste das Entfernen von CHK1 in diesen G1/S-arrestierten Zellen dennoch starke DNA-Schadenssignale und einen Verlust der Lebensfähigkeit aus, obwohl die Zellen daran gehindert wurden, in die S-Phase einzutreten. Folgeexperimente deuteten darauf hin, dass CHK1 normalerweise die vorzeitige Aktivierung von Replikationsursprüngen und das Aufdröseln der DNA durch die Helikasemaschinerie zurückhält. Ohne CHK1 schien diese Maschinerie unangemessenes Aufdröseln zu initiieren, wodurch lange Strecken exponierter, fragiler DNA entstanden, die zu Brüchen führten. Die Hemmung anderer Enzyme, die das Anlaufen von Ursprüngen anstoßen, rettete die Schäden teilweise und stützt dieses Modell.
Was das für Gesundheit und Therapie bedeutet
Insgesamt zeichnen die Ergebnisse CHK1 als einen integralen, dauerhaften Manager der DNA-Replikation und nicht als ein Protein, das nur bei Problemen eingreift. CHK1 wirkt bereits bevor das DNA-Kopieren beginnt, um rücksichtslose Ursprungaktivierung zu verhindern, und arbeitet während der S-Phase weiter, indem es die Geschwindigkeit der DNA-aufspülenden Helikase an die Kopierenzymatik anpasst, sodass die Gabeln sicher voranschreiten. Wenn CHK1 entfernt wird, geht diese Koordination verloren, Replikationsgabeln brechen zusammen, DNA-Brüche häufen sich und Zellen sterben schnell. Für den Laien lautet die Kernbotschaft: CHK1 hilft sicherzustellen, dass jede neue Kopie des Genoms sorgfältig und vollständig hergestellt wird. Diese zentrale Rolle erklärt, warum CHK1 ein vielversprechendes Ziel in der Krebstherapie geworden ist — seine Blockade kann bereits gestresste Tumorzellen über die Grenze treiben — aber auch, warum solche Behandlungen mit Bedacht eingesetzt werden müssen, angesichts der grundlegenden Bedeutung von CHK1 für das Überleben normal teilender Zellen.
Zitation: Li, S., Zhu, D., Tang, M. et al. CHK1 is an integral regulator of DNA replication in human cells. Cell Death Dis 17, 375 (2026). https://doi.org/10.1038/s41419-026-08624-1
Schlüsselwörter: DNA-Replikation, Zellzyklus, Genomstabilität, Checkpoint-Kinase, Replikationsstress