Clear Sky Science · fr
La phagocytose par l’épithélium pigmentaire rétinien et la microglie n’altère pas la restauration de la vision par des nanoparticules P3HT dans la rétinite pigmentaire
Un nouvel espoir pour la cécité héréditaire
La rétinite pigmentaire est une cause majeure de cécité héréditaire ; pourtant, la plupart des personnes touchées se voient dire qu’il n’y a plus rien à faire une fois que les cellules photoréceptrices de l’œil ont disparu. Cette étude examine une alternative émergente : de minuscules particules injectables qui fonctionnent comme une « prothèse rétinienne liquide ». Le travail évalue si ces nanoparticules peuvent restaurer la vision même lorsque les cellules de nettoyage de l’œil sont saines et activement engagées dans l’élimination des débris — une étape importante pour rendre la technologie pertinente pour des patients réels.
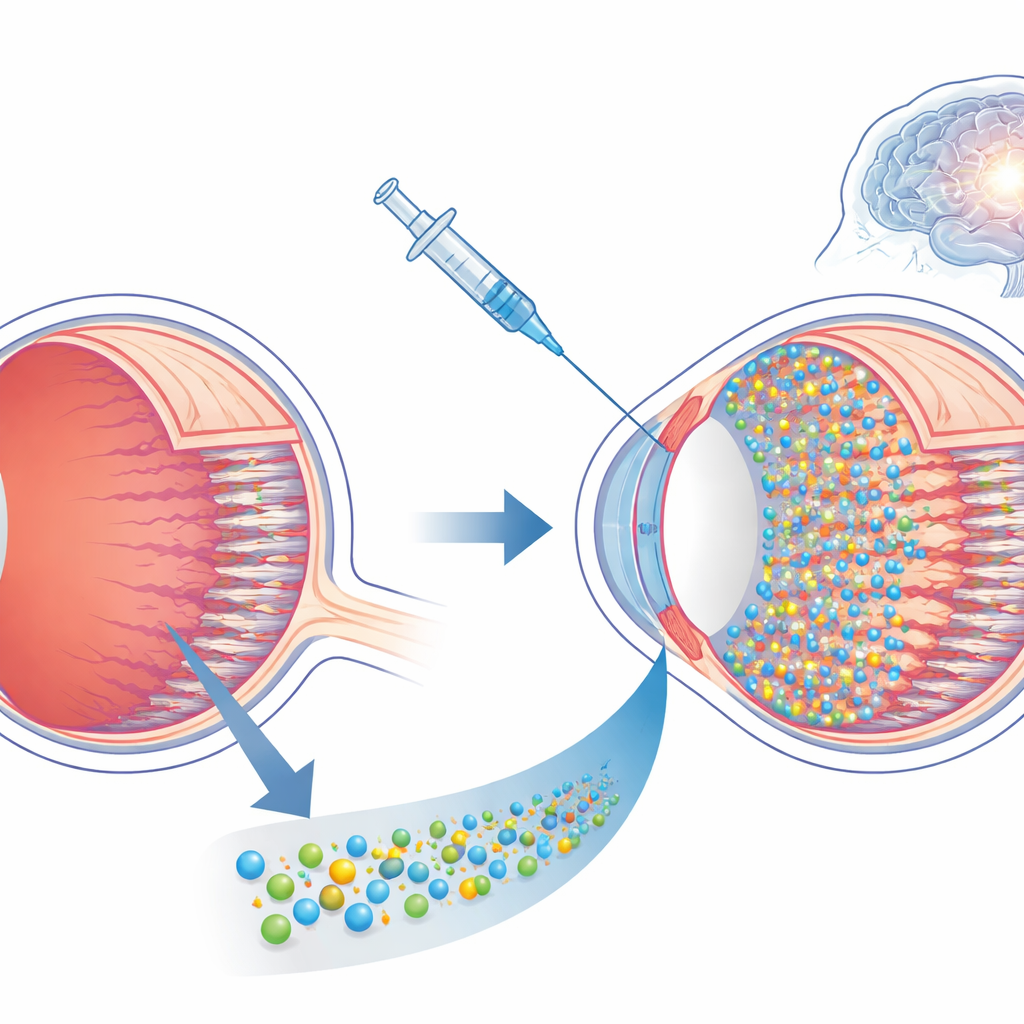
Lorsque l’appareil photo de l’œil tombe en panne
Dans un œil sain, les cellules bâtonnets et cônes au fond de la rétine convertissent la lumière en signaux électriques qui circulent via les circuits rétiniens internes vers le cerveau. Dans la rétinite pigmentaire, des défauts génétiques héréditaires tuent progressivement ces photorécepteurs, laissant d’abord les personnes nyctalopes, puis avec un champ de vision en tunnel, et enfin totalement aveugles. De nombreux traitements expérimentaux tentent de réparer ou de remplacer les cellules mourantes, mais ils reposent souvent sur l’identification précise du gène défectueux et une intervention très précoce. Une fois les bâtonnets et les cônes disparus, la plupart de ces options ne fonctionnent plus, et l’attention se tourne vers des dispositifs prothétiques qui contournent les cellules manquantes et stimulent directement le réseau rétinien restant.
Une prothèse rétinienne liquide
Les chercheurs se concentrent sur des nanoparticules fabriquées à partir d’un plastique photosensible appelé P3HT. Lorsque ces particules se trouvent à proximité des cellules nerveuses, des éclairs de lumière provoquent de minuscules changements électriques à leur surface qui peuvent pousser les neurones voisins à s’activer. Des travaux antérieurs ont montré que l’injection de nanoparticules de P3HT sous la rétine d’une souche de rat particulière, présentant des défauts dans ses cellules de nettoyage, pouvait restaurer des réponses proches de la vision pendant de nombreux mois. Mais comme ces rats ne peuvent pas éliminer efficacement les débris, il restait incertain si ce succès apparent dépendait de ce défaut : des cellules de nettoyage normales dans des formes plus typiques de la maladie avaleraient‑elles simplement et élimineraient les particules ?
Mettre les nanoparticules à l’épreuve
Pour répondre à cette question, l’équipe a utilisé des souris rd10, un modèle largement employé de rétinite pigmentaire où les bâtonnets meurent tôt en raison d’une mutation affectant une enzyme spécifique aux bâtonnets, tandis que l’épithélium pigmentaire rétinien (une couche de soutien) et la microglie (cellules de type immunitaire) restent fonctionnels. Les scientifiques ont attendu que la maladie atteigne son stade final — disparition complète des bâtonnets, cônes réduits à des moignons dispersés et circuits rétiniens internes largement réorganisés — afin que toute récupération puisse être attribuée aux nanoparticules plutôt qu’à des photorécepteurs survivants. Ils ont injecté un tout petit volume de suspension de nanoparticules de P3HT sous la rétine et suivi les animaux pendant jusqu’à quatre mois, en les comparant à des souris non traitées et à des animaux ayant reçu des particules de verre inertes de taille similaire.
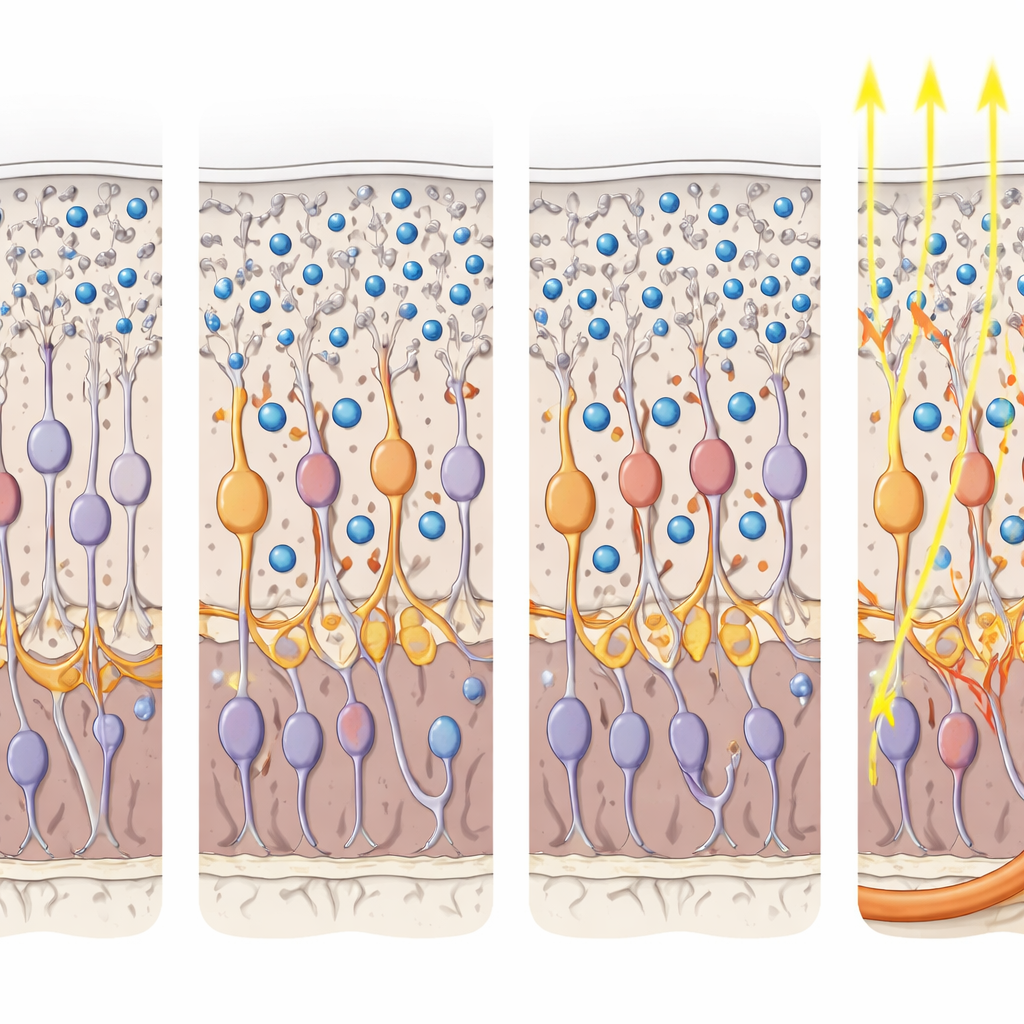
Survivre à l’équipe de nettoyage de l’œil
Des images à haute résolution ont montré qu’une seule injection répartissait les nanoparticules de P3HT sur environ 80 % de la surface rétinienne. La plupart des particules restaient dans la rétine externe, nichées parmi les prolongements des neurones de second ordre, tandis qu’environ 30 % seulement étaient internalisées par l’épithélium pigmentaire et moins de 5 % par la microglie. Fait important, cette phagocytose partielle n’endommageait pas ces cellules de soutien et immunitaires ni ne provoquait d’inflammation supplémentaire ; leur morphologie et leur densité étaient similaires en présence ou en l’absence des nanoparticules. En bref, même dans un œil doté d’un « aspirateur » cellulaire actif, une population importante et stable de particules persistait au bon endroit pour influencer le circuit rétinien survivant.
De la lumière au comportement et à l’activité cérébrale
La question essentielle était de savoir si ces particules résidentes rétablissaient réellement une vision utile. Plusieurs tests convergent vers un oui. Dans un test optomoteur, où les souris suivent de manière réflexe des bandes en mouvement, les souris rd10 traitées avec le P3HT ont retrouvé des réponses à des niveaux de détail spatial que les souris aveugles non traitées ou sham‑traitées ne pouvaient pas détecter, approchant la performance d’animaux sains. Dans une tâche de conditionnement classique, les souris ont appris à associer de brefs flashs lumineux à un léger choc au pied. Seules les souris saines et les souris rd10 traitées au P3HT se sont ensuite figées par anticipation lorsqu’elles ont vu la lumière seule, indiquant que les signaux induits par la lumière atteignaient et étaient traités par des centres cérébraux supérieurs pour former des mémoires visuelles implicites. Des enregistrements électriques du cortex visuel primaire ont confirmé ce tableau : après traitement, des souris auparavant aveugles montraient des réponses robustes et verrouillées dans le temps aux flashs lumineux et aux réseaux de franges, avec une acuité visuelle comparable à celle de souris normales d’un âge similaire, bien que l’amplitude des signaux fût quelque peu réduite.
Ce que cela signifie pour les thérapies futures
Pris ensemble, les résultats montrent que des nanoparticules de P3HT injectables peuvent restaurer des fonctions visuelles complexes — même à des stades tardifs et fortement dégénératifs de la rétinite pigmentaire — dans un œil à activité de nettoyage normale. Les particules ne sont pas rapidement éliminées ni manifestement toxiques, et elles peuvent générer des réponses comportementales et cérébrales semblables à celles d’animaux voyants. Pour les personnes vivant avec une cécité héréditaire avancée, cela suggère qu’une « prothèse liquide » agnostique au gène et peu invasive pourrait un jour compléter ou remplacer les approches actuelles, offrant un moyen de réveiller des circuits visuels dormants longtemps après la disparition des cellules photoréceptrices d’origine.
Citation: Mantero, G., Francia, S., Galluzzi, F. et al. Phagocytosis by retinal pigment epithelium and microglia does not affect vision restoration by P3HT nanoparticles in Retinitis pigmentosa. Cell Death Dis 17, 295 (2026). https://doi.org/10.1038/s41419-026-08510-w
Mots-clés: rétinite pigmentaire, prothèse rétinienne, nanoparticules, restauration de la vision, dégénérescence rétinienne