Clear Sky Science · ar
البلع الخلوي بواسطة ظهارة صبغة الشبكية والميكروغليا لا يؤثر على استعادة البصر بواسطة جُسيمات P3HT في التهاب الشبكية الصباغي
أمل جديد في عمى وراثي
التهاب الشبكية الصباغي هو سبب رئيسي للعمى الوراثي، ومع ذلك يُقال لمعظم المصابين إنه لا يمكن فعل شيء بمجرد فقدان خلايا استقبال الضوء في العين. تستكشف هذه الدراسة بديلًا ناشئًا: جُسيمات حقنية صغيرة تعمل مثل «شبكية صناعية سائلة». تختبر الدراسة ما إذا كانت هذه الجسيمات النانوية لا تزال قادرة على استعادة البصر حتى عندما تكون خلايا التنظيف في العين صحية وتنخرط بفاعلية في ابتلاع الحطام—وهو خطوة مهمة لجعل هذه التقنية ذات صلة بالمرضى الحقيقيين.
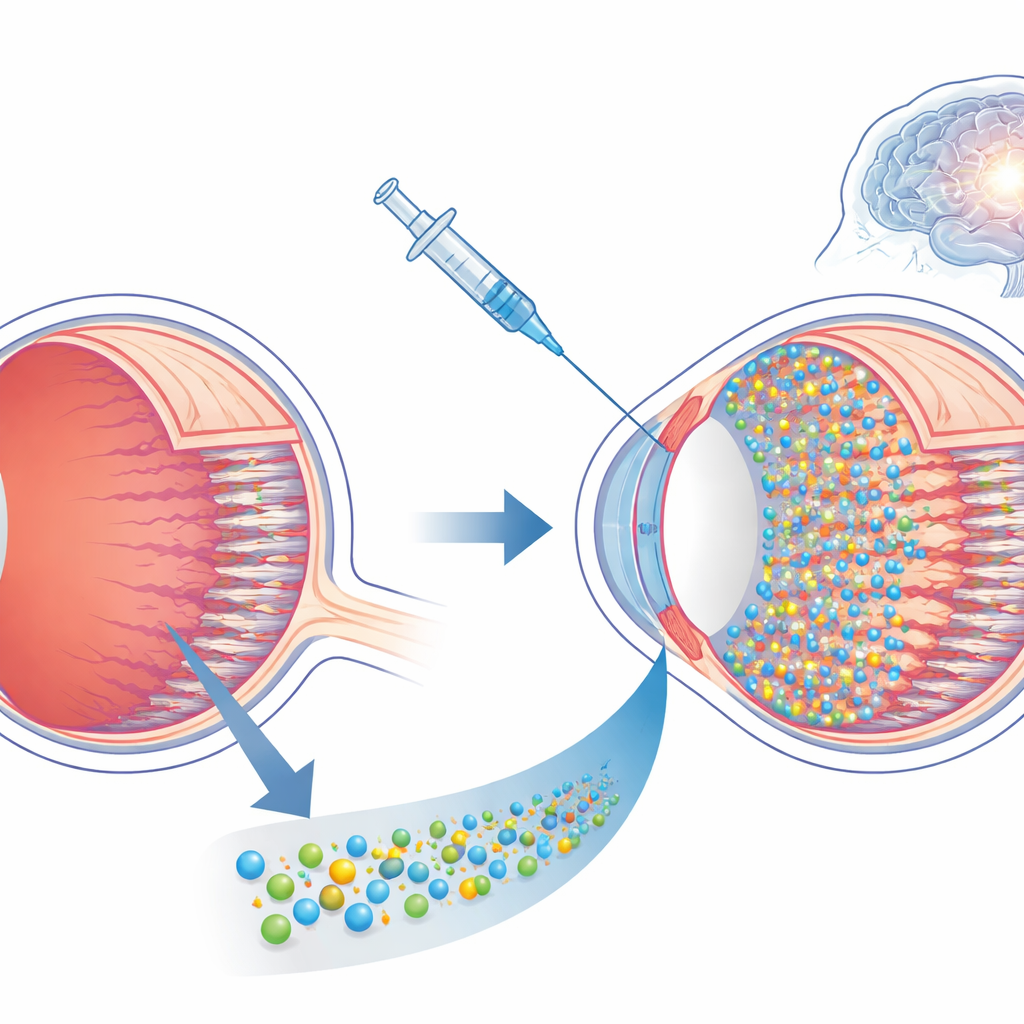
عندما يتعطل جهاز الكاميرا في العين
في عين سليمة، تحوّل خلايا القضبان والمخاريط في مؤخرة الشبكية الضوء إلى إشارات كهربائية تنتقل عبر دوائر الشبكية الداخلية إلى الدماغ. في التهاب الشبكية الصباغي، تقضي عيوب جينية وراثية تدريجيًا على هذه الخلايا الحساسة للضوء، مما يترك المصابين أولًا عميانًا ليلاً، ثم يعانون من رؤية نفقية، وفي النهاية يفقدون البصر تمامًا. تحاول العديد من العلاجات التجريبية إصلاح أو استبدال الخلايا المحتضرة، لكنها غالبًا ما تعتمد على معرفة العيب الجيني المحدد والتدخل في وقت مبكر جدًا من الحياة. وبمجرد اختفاء القضبان والمخاريط، تتوقف معظم هذه الخيارات عن العمل، ويتجه الاهتمام إلى الأجهزة التعويضية التي تتجاوز الخلايا المفقودة وت刺激 الشبكة الشبكية المتبقية مباشرة.
طرف شبكي سائل
يركز الباحثون على جُسيمات نانوية مصنوعة من بلاستيك حساس للضوء يُدعى P3HT. عندما تجلس هذه الجسيمات بالقرب من الخلايا العصبية، تتسبب ومضات الضوء في تغيّرات كهربائية طفيفة على سطحها يمكن أن تدفع الخلايا العصبية المجاورة نحو الانطلاق في إطلاق الشحنات. أظهرت أعمال سابقة أن حقن جُسيمات P3HT تحت الشبكية في نوع معين من الجرذان التي تعاني عجزًا في خلايا التنظيف قد أعاد ردودًا شبيهة بالبصر لعدة أشهر. لكن لأن تلك الجرذان غير قادرة على إزالة الحطام بكفاءة، لم يكن واضحًا ما إذا كان النجاح الظاهر يعتمد على هذا العيب: هل ستبتلع خلايا التنظيف الطبيعية في العين الجسيمات ببساطة وتزيلها في أشكال أكثر شيوعًا من المرض؟
اختبار الجسيمات النانوية
للإجابة عن ذلك، استخدم الفريق فئران rd10، نموذج واسع الاستخدام لالتهاب الشبكية الصباغي حيث تموت خلايا القضيب مبكرًا بسبب طفرة في إنزيم خاص بالقضيب، بينما تظل ظهارة صبغة الشبكية (طبقة داعمة) والميكروغليا (خلايا شبيهة بالمناعة) وظيفية. انتظر العلماء حتى بلغت المرض مرحلته النهائية—اختفاء القضبان تمامًا، تقلص المخاريط إلى بقايا متناثرة، وإعادة توصيل واسعة لدوائر الشبكية الداخلية—حتى يمكن عزو أي تعافٍ إلى الجسيمات النانوية وليس إلى خلايا ضوئية باقية. حقنوا حجمًا طفيفًا من معلق جُسيمات P3HT تحت الشبكية وتابعوا الحيوانات لمدة تصل إلى أربعة أشهر، مقارنين إياها بفئران غير معالجة وبحيوانات أعطيت جُسيمات زجاجية غير فعالة مشابهة في الحجم.
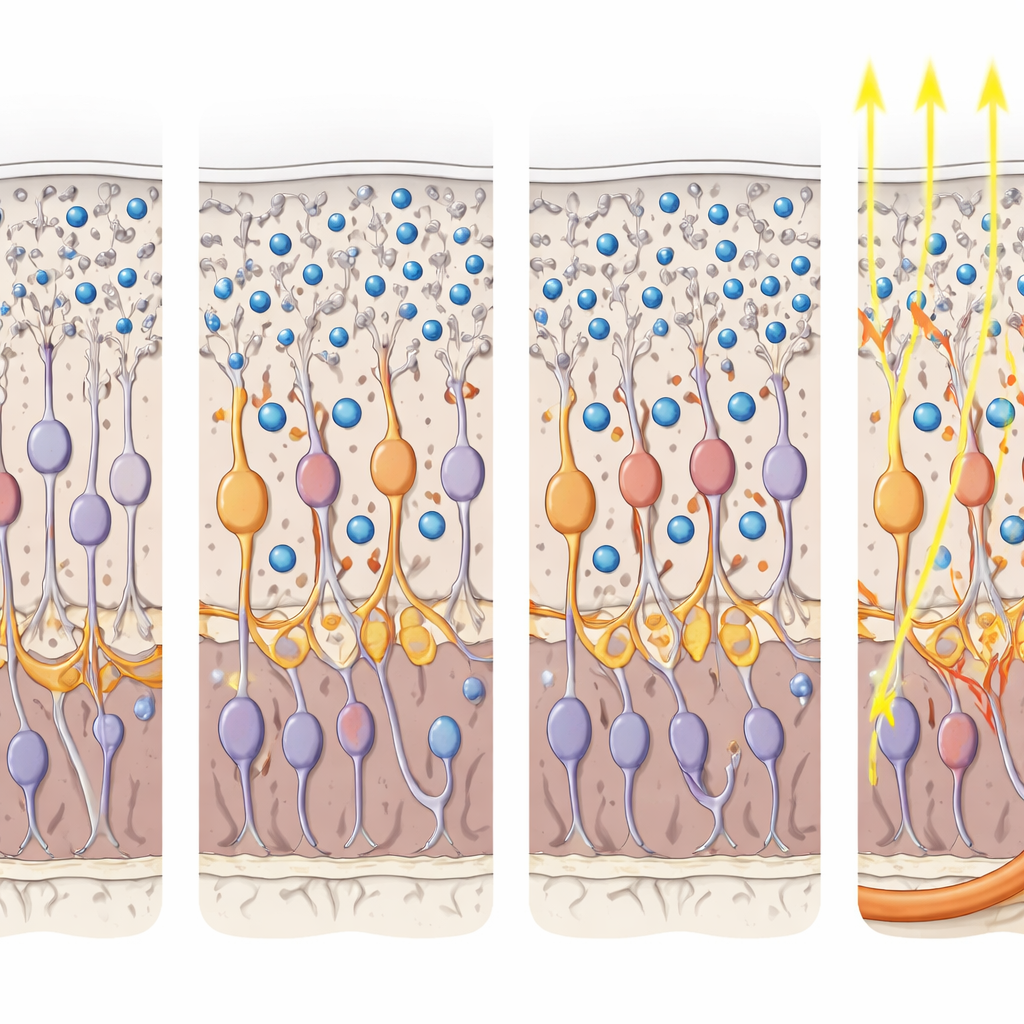
البقاء أمام طاقم التنظيف في العين
أظهرت التصويرات عالية الدقة أن حقنة واحدة وزعت جُسيمات P3HT عبر نحو 80 بالمئة من سطح الشبكية. بقيت معظم الجسيمات في الشبكية الخارجية، متوضعة بين تفرعات الخلايا العصبية من الدرجة الثانية، بينما تم ابتلاع نحو 30 بالمئة فقط منها بواسطة ظهارة الصبغة وأقل من 5 بالمئة بواسطة الميكروغليا. ومن المهم أن هذا الالتقاط الجزئي لم يضر بتلك الخلايا الداعمة والمناعية ولم يثير التهابات إضافية؛ فقد كانت شكلها وكثافتها مشابهين مع وبدون الجسيمات. باختصار، حتى في عين ذات «مكنسات خلايا» نشطة، استمرت مجموعة كبيرة وثابتة من الجسيمات في المكان المناسب للتأثير على دوائر الشبكية الباقية.
من الضوء إلى السلوك ونشاط الدماغ
السؤال الحاسم كان ما إذا كانت هذه الجسيمات المقيمة فعلاً تستعيد بصرًا وظيفيًا. أعطت اختبارات متعددة إجابة متقاربة بنعم. في اختبار تتبع بصري انعكاسي حيث تتبع الفئران الشريط المتحرك، استعادت فئران rd10 المعالجة بـP3HT استجابات عند مستويات تفصيل مكاني لا تستطيع الفئران العمياء غير المعالجة أو المعالجة الوهمية اكتشافها، مقتربة من أداء الحيوانات السليمة. في مهمة تكييف كلاسيكي، تعلمت الفئران ربط ومضات ضوئية قصيرة بصدمة خفيفة في القدم. تجمدت لاحقًا فقط الفئران السليمة وفئران rd10 المعالجة بـP3HT ترقبًا عندما رأت الضوء وحده، مما يدل على أن الإشارات المدفوعة بالضوء وصلت إلى المراكز الدماغية العليا وتمت معالجتها لتشكيل ذكريات بصرية ضمنية. أكدت التسجيلات الكهربائية من القشرة البصرية الأولية هذه الصورة: بعد المعالجة، أظهرت الفئران العمياء سابقًا استجابات قوية ومتزامنة زمنياً للومضات الضوئية والشرائط النمطية، بدقة بصرية مطابقة للفئران الطبيعية من نفس العمر، وإن كانت بقوة إشارة أقل بعض الشيء.
ماذا يعني هذا للعلاجات المستقبلية
تظهر النتائج مجتمعة أن جُسيمات P3HT القابلة للحقن يمكنها استعادة وظائف بصرية معقدة—حتى في مراحل متأخرة وشديدة التحلل من التهاب الشبكية الصباغي—في عين ذات نشاط تنظيف طبيعي. لا تُزال الجسيمات بسرعة ولا تبدو سامة بوضوح، ويمكنها دفع سلوكيات واستجابات دماغية تشبه تلك لدى الحيوانات المبصرة. بالنسبة للأشخاص الذين يعيشون مع عمى وراثي متقدم، يشير ذلك إلى أن «طرف سائل» خالٍ من الاعتماد على الطفرة ومُتدخل بأقل قدر من الغازية قد يكمل أو يحل محل النهج الحالية يومًا ما، ويقدّم طريقة لإعادة إيقاظ دوائر بصرية خامدة بعد مدة طويلة من اختفاء الخلايا الحساسة للضوء الأصلية.
الاستشهاد: Mantero, G., Francia, S., Galluzzi, F. et al. Phagocytosis by retinal pigment epithelium and microglia does not affect vision restoration by P3HT nanoparticles in Retinitis pigmentosa. Cell Death Dis 17, 295 (2026). https://doi.org/10.1038/s41419-026-08510-w
الكلمات المفتاحية: التهاب الشبكية الصباغي, طرف صناعي شبكي, جسيمات نانوية, استعادة البصر, انحلال الشبكية