Clear Sky Science · fr
Del[20q] dérivé du donneur après transplantation allogénique de cellules hématopoïétiques : un cas avec suivi sur 26 ans et revue de la littérature
Particularités cachées dans la moelle osseuse donnée
Les transplantations de moelle osseuse peuvent sauver la vie des personnes atteintes de cancers du sang, mais que se passe-t-il lorsque les cellules du donneur portent discrètement leurs propres anomalies génétiques ? Cet article explore une situation rare dans laquelle une modification subtile de l’ADN dans les cellules hématopoïétiques d’une donneuse a été transmise à une receveuse et suivie pendant plus d’un quart de siècle. L’histoire illustre comment certaines altérations génétiques peuvent rester inoffensives des décennies durant, alors que d’autres peuvent favoriser l’apparition de maladies graves.
Un récit de longue durée sur du sang partagé
Le point central de l’étude est une femme ayant reçu une greffe de moelle osseuse de sa sœur pour traiter un lymphome réfractaire. La moelle de la sœur contenait, à son insu, une petite population de cellules dépourvues d’un segment d’ADN sur un bras du chromosome 20, une anomalie appelée délétion 20q. Après la transplantation, ces cellules d’origine donneuse ont colonisé l’appareil sanguin de la receveuse. Au fil du temps, les analyses ont montré que les cellules portant cette délétion sont devenues dominantes dans le sang de la receveuse, en particulier dans les globules blancs impliqués dans la défense contre les infections. Pourtant, de façon remarquable, la receveuse est restée en bonne santé, avec des numérations sanguines normales et sans signe de cancer hématologique pendant 26 ans.
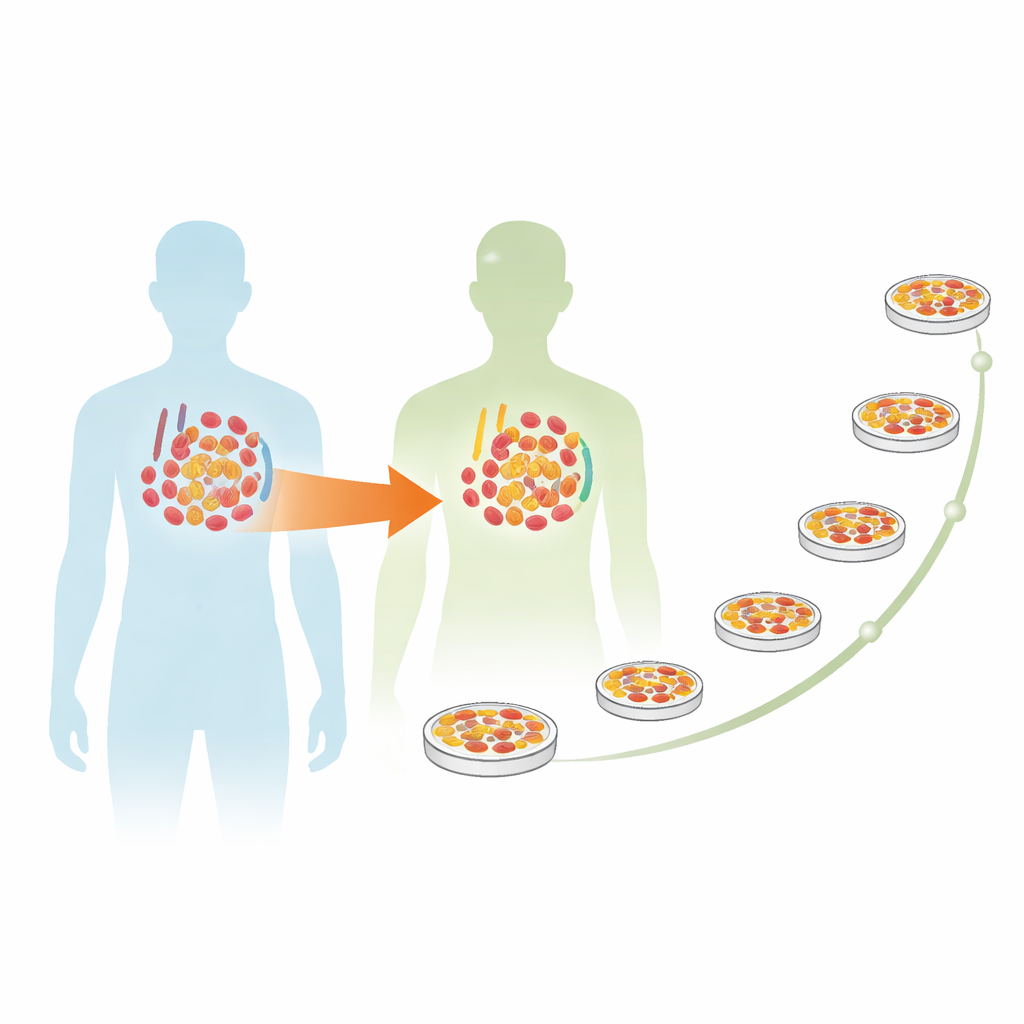
Suivre une empreinte génétique sur des décennies
Pour comprendre ce cas inhabituel, les chercheurs ont utilisé des outils de laboratoire détaillés pour suivre les cellules d’origine donneuse. Une technique appelée hybridation fluorescente in situ leur a permis de compter combien de cellules sanguines portaient le segment manquant du chromosome 20 dans différents types cellulaires, comme les cellules combattant les infections et les cellules productrices d’anticorps. Plus tard, ils ont appliqué le séquençage génétique moderne à la moelle conservée du donneur et au sang de la receveuse prélevé 20 et 26 ans après la transplantation. Ces tests ont révélé des variants de très faible abondance dans deux gènes connus pour être liés au cancer, DNMT3A et TP53, à la fois dans les échantillons du donneur et de la receveuse, confirmant que le même clone anormal avait été transmis de sœur à sœur au moment de la greffe.
Quand les cellules du donneur deviennent dangereuses
Les chercheurs se sont ensuite posé une question plus large : à quelle fréquence ce type de délétion 20q d’origine donneur mène-t-il à des complications ? Ils ont passé en revue la littérature médicale et identifié 20 receveurs de greffe connus dont les cellules donneuses portaient la même anomalie chromosomique. La plupart avaient reçu une greffe d’un frère ou d’une sœur compatible, souvent pour une leucémie. Dans ce groupe combiné, la délétion 20q a été généralement détectée environ un an et demi après la transplantation, et le suivi durait en moyenne trois ans. Environ un tiers de ces receveurs ont finalement développé des troubles sanguins sévères d’origine donneur, tels que des syndromes myélodysplasiques ou des leucémies aiguës, le plus souvent autour du moment où l’anomalie chromosomique était observée.
Pourquoi les évolutions divergent
Cette comparaison côte à côte des patients a révélé une variation frappante. Certaines personnes, comme le cas principal de ce rapport, ont vécu des décennies avec une population dominante de cellules donneuses génétiquement altérées sans jamais développer de maladie. D’autres, présentant des anomalies chromosomiques apparemment similaires, ont évolué vers des cancers du sang agressifs. Dans quelques cas où des tests génétiques complémentaires ont été réalisés, certains patients portaient des mutations supplémentaires délétères dans des gènes impliqués dans la prolifération et le contrôle des cellules sanguines, tandis que d’autres n’en présentaient aucune. Les auteurs suggèrent que les expositions environnementales, les réponses immunitaires, le microenvironnement médullaire et le mélange spécifique d’altérations génétiques influencent probablement si un clone d’origine donneur reste silencieux ou devient menaçant.
Repenser le dépistage des donneurs et le suivi
Ces constatations soulèvent des questions pratiques pour les programmes de transplantation. Aujourd’hui, la plupart des donneurs sont évalués par l’anamnèse et des examens sanguins de routine, et non par une analyse chromosomique détaillée ou un séquençage profond. Pourtant, des études montrent maintenant que des mutations subtiles liées à l’âge dans les cellules sanguines des donneurs sont courantes, en particulier chez les adultes plus âgés. Certaines de ces altérations peuvent être inoffensives ou même neutres, tandis que d’autres peuvent comporter un risque plus élevé. Les auteurs soutiennent que plutôt que d’exclure automatiquement tous les donneurs ayant des clones détectables, les médecins devraient mettre en balance l’urgence de la maladie du receveur, la disponibilité d’autres donneurs et la nature précise des altérations génétiques présentes. Tout aussi important, les receveurs de tels greffons pourraient bénéficier d’un suivi structuré à long terme pour détecter tôt tout signe avant-coureur.
Ce que cela signifie pour les patients et les donneurs
En termes simples, ce travail montre que des cellules sanguines légèrement anormales du donneur peuvent coloniser la moelle d’un receveur et rester silencieuses pendant des décennies, même lorsqu’elles portent des altérations d’ADN souvent associées au cancer. Dans le même temps, environ un cas sur trois similaire dans la littérature médicale a évolué vers une maladie grave. La leçon n’est pas de craindre la transplantation de moelle, qui reste une thérapie essentielle et souvent curative, mais d’apprécier la complexité génétique qui la sous-tend. Avec un meilleur profilage génétique des donneurs et un suivi à long terme des receveurs, les médecins espèrent distinguer les particularités génétiques inoffensives des altérations réellement à risque et adapter en conséquence la surveillance et le traitement.
Citation: Bouley, C., Fang, M., Radich, J. et al. Donor-derived del[20q] following allogeneic-hematopoietic cell transplantation: a case with 26-year follow-up and literature review. Bone Marrow Transplant 61, 445–451 (2026). https://doi.org/10.1038/s41409-026-02801-8
Mots-clés: transplantation de moelle osseuse, hématopoïèse clonale, délétion du chromosome 20q, leucémie d’origine donneur, syndrome myélodysplasique