Clear Sky Science · de
Vom Spender stammende del[20q] nach allogener hämatopoetischer Zelltransplantation: ein Fall mit 26-jähriger Nachbeobachtung und Literaturübersicht
Verborgene Eigenheiten im gespendeten Knochenmark
Knochenmarktransplantationen können für Menschen mit Blutkrebs lebensrettend sein. Doch was passiert, wenn die Zellen des Spenders stillschweigend eigene genetische Besonderheiten tragen? Dieser Artikel beschreibt eine seltene Situation, in der eine subtile DNA-Veränderung in den blutbildenden Zellen einer Spenderin auf eine Empfängerin übertragen wurde und über mehr als ein Vierteljahrhundert verfolgt werden konnte. Die Geschichte zeigt, wie einige genetische Veränderungen über Jahrzehnte harmlos bleiben können, während andere den Weg für schwere Erkrankungen ebnen können.
Eine Langzeitgeschichte gemeinsamen Bluts
Im Mittelpunkt der Studie steht eine Frau, die zur Behandlung einer schwer zu behandelnden Lymphomform eine Knochenmarktransplantation von ihrer Schwester erhielt. Das Knochenmark der Schwester enthielt unwissentlich eine kleine Zellpopulation, der ein Stück DNA am einen Arm von Chromosom 20 fehlte — eine Fehlstellung, bezeichnet als 20q-Deletion. Nach der Transplantation übernahmen diese Spenderzellen das Blutbild der Empfängerin. Im Laufe der Zeit zeigten Tests, dass Zellen mit dieser Deletion in der Empfängerin zunehmend dominant wurden, insbesondere in den weißen Blutkörperchen, die Infektionen bekämpfen. Bemerkenswerterweise blieb die Empfängerin jedoch gesund, mit normalen Blutwerten und ohne Hinweise auf Blutkrebs über 26 Jahre hinweg.
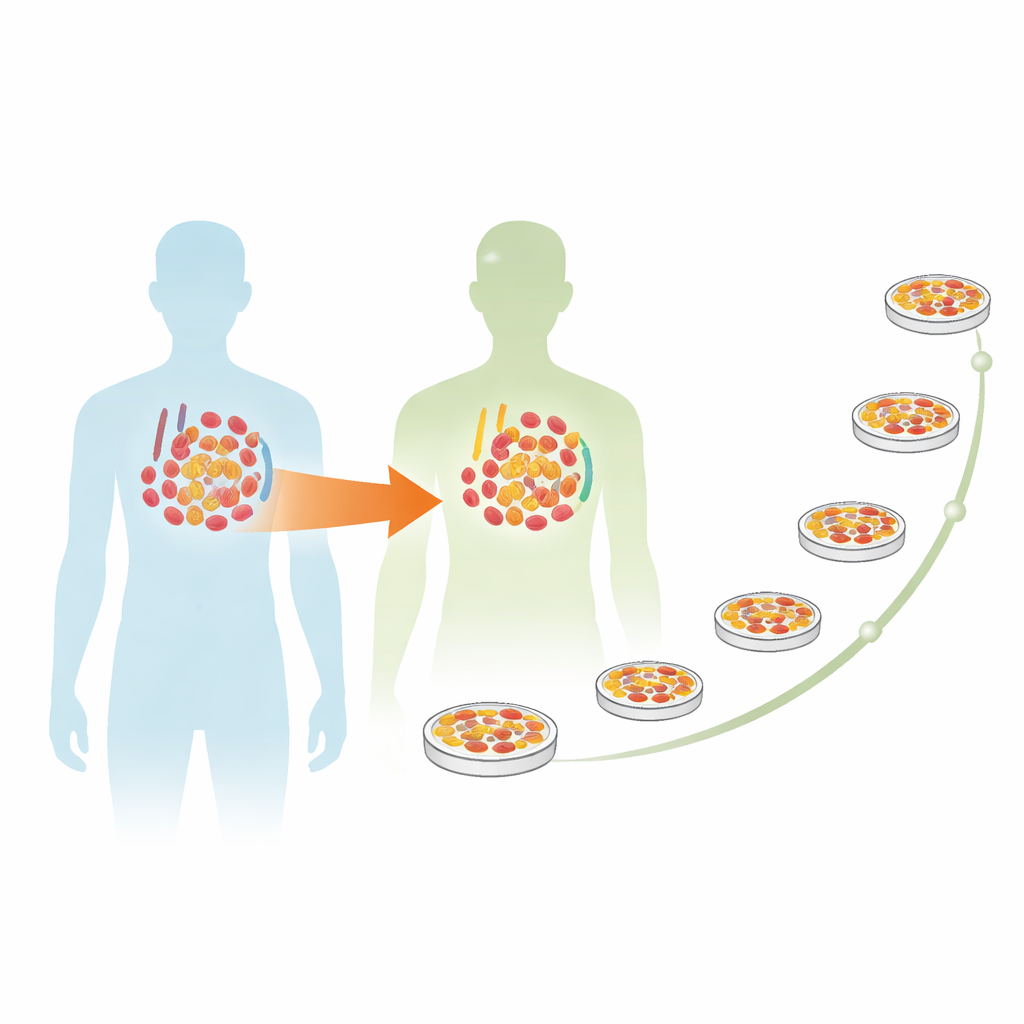
Ein genetischen Fußabdruck über Jahrzehnte verfolgen
Um diesen ungewöhnlichen Fall zu verstehen, nutzten die Forschenden detaillierte Labormethoden, um die vom Spender stammenden Zellen nachzuverfolgen. Eine Methode namens Fluoreszenz-in-situ-Hybridisierung ermöglichte es ihnen zu zählen, wie viele Blutzellen das fehlende Stück von Chromosom 20 in verschiedenen Zelltypen trugen, etwa in infekti-onsbekämpfenden Zellen und in antikörperproduzierenden Zellen. Später wandten sie moderne Gen-Sequenzierung auf konserviertes Spendermark und auf das Blut der Empfängerin an, das 20 und 26 Jahre nach der Transplantation entnommen worden war. Diese Tests enthüllten sehr niedriggradige Veränderungen in zwei gut bekannten krebsassoziierten Genen, DNMT3A und TP53, in Proben von Spenderin und Empfängerin und bestätigten, dass derselbe abnorme Klon zur Zeit der Transplantation von Schwester zu Schwester übertragen worden war.
Wenn Spenderzellen gefährlich werden
Die Forschenden stellten danach eine größere Frage: Wie oft führt eine solche vom Spender stammende 20q-Deletion zu Problemen? Sie durchforsteten die medizinische Fachliteratur und identifizierten 20 bekannte Transplantationsempfänger, deren Spenderzellen dieselbe chromosomale Veränderung aufwiesen. Die meisten hatten Transplantationen von passenden Geschwisterspendern erhalten, häufig wegen Leukämie. In dieser zusammengefassten Gruppe wurde die 20q-Deletion meist etwa anderthalb Jahre nach der Transplantation entdeckt, und die Nachbeobachtung dauerte typischerweise drei Jahre. Etwa ein Drittel dieser Empfänger entwickelte schließlich ernsthafte vom Spender stammende Bluterkrankungen, wie myelodysplastisches Syndrom oder akute Leukämie, oft in zeitlicher Nähe zur Entdeckung der Chromosomenveränderung.
Warum die Verläufe auseinandergehen
Der direkte Vergleich der Patientinnen und Patienten zeigte deutliche Unterschiede. Manche, wie der zentrale Fall in diesem Bericht, lebten Jahrzehnte mit einer dominanten Population genetisch veränderter Spenderzellen, ohne jemals eine Krankheit zu entwickeln. Andere mit scheinbar ähnlichen chromosomalen Veränderungen entwickelten aggressive Bluttumore. In einigen Fällen, in denen zusätzliche genetische Untersuchungen durchgeführt wurden, trugen einige Patientinnen und Patienten zusätzliche schädliche Mutationen in Genen, die am Wachstum und an der Regulation von Blutzellen beteiligt sind; andere zeigten keine solchen Veränderungen. Die Autorinnen und Autoren vermuten, dass Umweltfaktoren, Immunantworten, das Knochenmarkmilieu und die spezifische Kombination genetischer Veränderungen vermutlich alle beeinflussen, ob ein vom Spender stammender Klon stumm bleibt oder gefährlich wird.
Neues Nachdenken über Spender-Screening und Nachsorge
Die Befunde werfen praktische Fragen für Transplantationsprogramme auf. Heute werden die meisten Spender anhand von Anamnese und Routine-Bluttests überprüft, nicht durch detaillierte Chromosomenanalyse oder umfassende Gensequenzierung. Studien zeigen jedoch, dass subtile altersbedingte Mutationen in Blutstammzellen von Spendern, insbesondere bei älteren Erwachsenen, verbreitet sind. Einige dieser Veränderungen können harmlos oder sogar nützlich sein, andere hingegen mit einem höheren Risiko verbunden sein. Die Autorinnen und Autoren plädieren dafür, nicht automatisch alle Spender mit nachweisbaren Klonen auszuschließen, sondern die Dringlichkeit der Erkrankung des Empfängers, die Verfügbarkeit alternativer Spender und die spezifischen genetischen Veränderungen gegeneinander abzuwägen. Ebenso wichtig ist, dass Empfänger solcher Transplantate von einer langfristigen, strukturierten Überwachung profitieren könnten, um mögliche Warnsignale früh zu erkennen.
Was das für Patientinnen, Patienten und Spender bedeutet
Kurz gesagt zeigt diese Arbeit, dass leicht abnorme Blutzellen eines Spenders das Knochenmark einer Empfängerin übernehmen und über Jahrzehnte ruhig bleiben können, selbst wenn sie DNA-Veränderungen tragen, die oft mit Krebs in Verbindung gebracht werden. Gleichzeitig entwickelten etwa ein Drittel ähnlicher Fälle in der Fachliteratur doch eine schwere Erkrankung. Die Lehre ist nicht, Knochenmarktransplantationen zu fürchten — sie bleiben eine wichtige und oft kurative Therapie — sondern die genetische Komplexität dahinter zu erkennen. Mit besserer genetischer Profilerstellung von Spendern und langfristiger Nachbeobachtung der Empfänger hoffen Ärztinnen und Ärzte, harmlose genetische Besonderheiten von tatsächlich riskanten Veränderungen zu unterscheiden und die Überwachung sowie Behandlung entsprechend anzupassen.
Zitation: Bouley, C., Fang, M., Radich, J. et al. Donor-derived del[20q] following allogeneic-hematopoietic cell transplantation: a case with 26-year follow-up and literature review. Bone Marrow Transplant 61, 445–451 (2026). https://doi.org/10.1038/s41409-026-02801-8
Schlüsselwörter: Knochenmarkstransplantation, klonale Hämatopoese, Deletion von Chromosom 20q, vom Spender stammende Leukämie, myelodysplastisches Syndrom