Clear Sky Science · es
Disfunción de fibroblastos impulsada por ubiquitinación: un plan multi-ómico para el diagnóstico y la terapia de precisión en la úlcera del pie diabético
Por qué importan las heridas persistentes en el pie
Para muchas personas con diabetes, una pequeña llaga en el pie puede convertirse en una úlcera persistente que se niega a cicatrizar. Estas úlceras del pie diabético con frecuencia conducen a estancias hospitalarias prolongadas e incluso a amputación, y los médicos todavía tienen dificultades para predecir qué heridas empeorarán y qué tratamientos funcionarán mejor. Este estudio profundiza en las células dentro de estas heridas crónicas y descubre un sistema de control oculto que podría explicar por qué falla la cicatrización —y cómo podríamos diagnosticar y tratar estas úlceras con mayor precisión en el futuro. 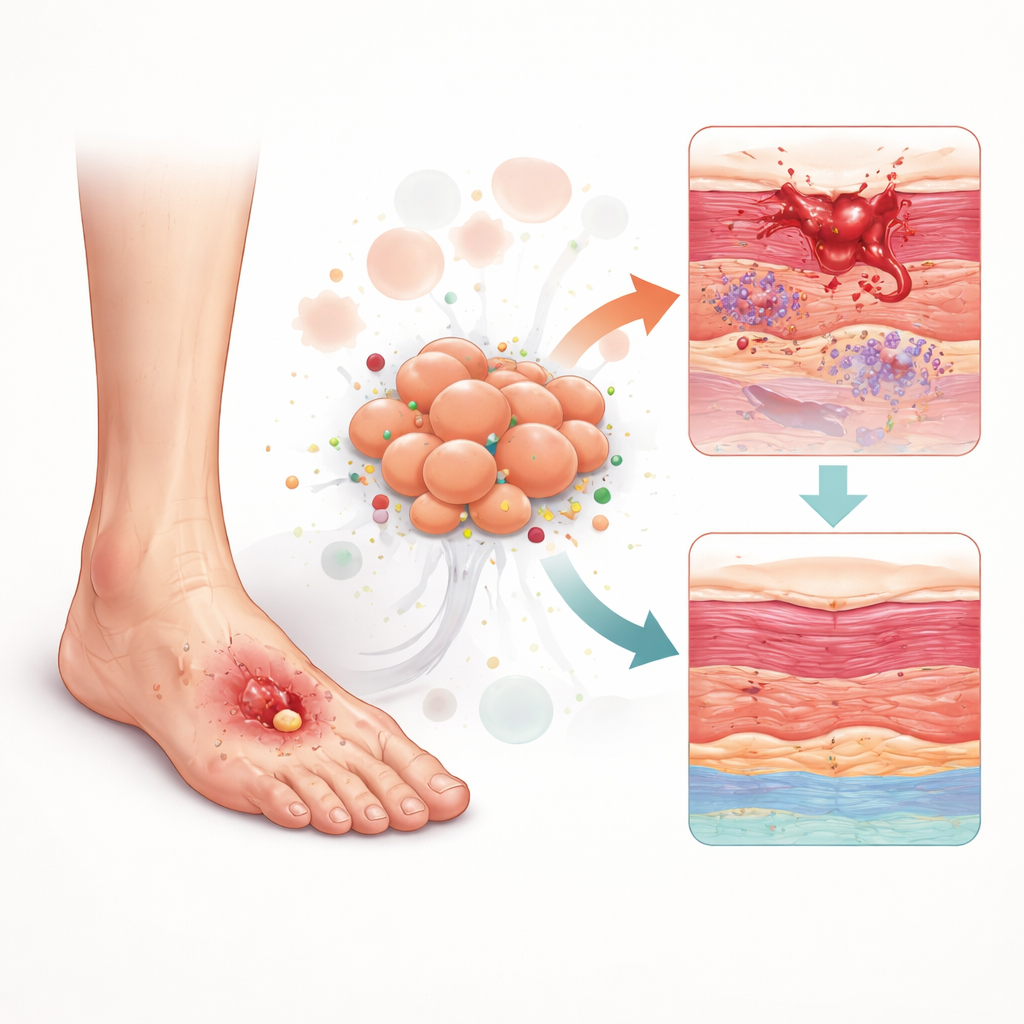
Una mirada más estrecha al equipo reparador de la piel
La piel sana depende de un conjunto de células que reparan el daño tras una lesión. Entre las más importantes están los fibroblastos, los “manitas” estructurales que construyen y remodelan el andamiaje tisular durante la reparación de la herida. Los investigadores usaron secuenciación de ARN de célula única de vanguardia para analizar más de 23.000 células individuales de piel del pie normal y de úlceras del pie diabético. Esto les permitió ver qué genes estaban activados en cada tipo celular, desde células inmunitarias y de los vasos sanguíneos hasta fibroblastos. Se centraron en un grupo de genes implicados en la ubiquitinación, un sistema químico de etiquetado que marca proteínas para reciclaje o reubicación y ayuda a mantener el equilibrio de la maquinaria celular.
Descubrimiento de un grupo problemático de fibroblastos
Al comparar tejidos sanos y enfermos, los fibroblastos surgieron como el tipo celular más alterado en las úlceras diabéticas. Un subgrupo distinto de fibroblastos apareció casi exclusivamente en el tejido ulcerado. Estos fibroblastos “patogénicos” mostraron indicios de mayor potencial semejante al de células madre, metabolismo alterado y comunicación reconfigurada con las células vecinas. Empleando herramientas computacionales que trazan cómo cambian las células con el tiempo, el estudio sugirió que los fibroblastos ordinarios se transforman gradualmente en este estado dañino en el duro entorno de la herida diabética. Una vez transformados, emiten y reciben señales excesivas relacionadas con la inflamación, la formación de nuevos vasos y la remodelación tisular —señales que, en lugar de promover la reparación, podrían encerrar la herida en un estado crónico e inflamado. 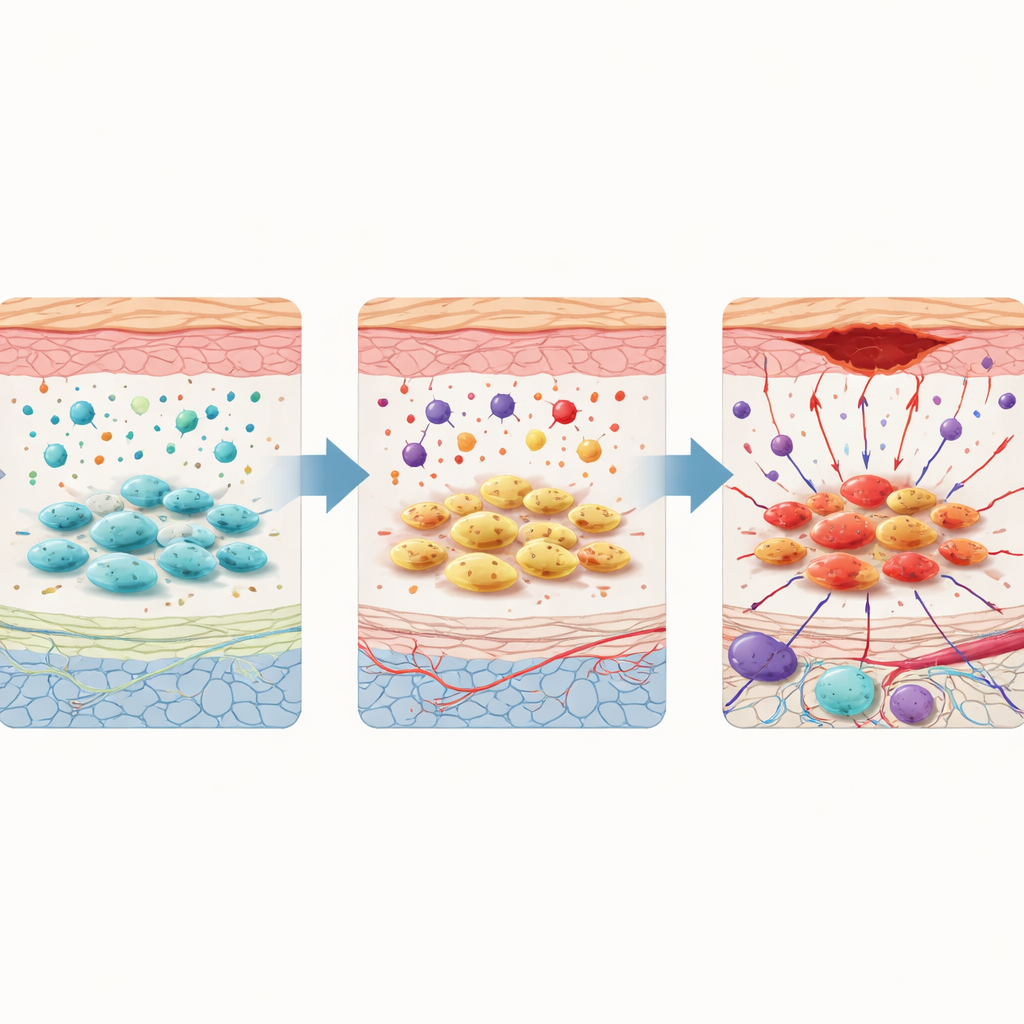
Interruptores moleculares ocultos y una huella diagnóstica
Para convertir miles de mediciones génicas en algo clínicamente útil, los investigadores combinaron varios métodos de aprendizaje automático para cribar grandes conjuntos de datos públicos de tejidos del pie diabético y sanos. Identificaron cuatro genes clave —MEF2A, SKIL, MAF y KRT5— que en conjunto formaron una potente “huella” capaz de distinguir las úlceras diabéticas de la piel normal, con alta precisión en datos de prueba. Entre ellos, SKIL destacó como el más influyente. Se sabe por otras investigaciones que interfiere con una vía de reparación mayor (a menudo controlada por TGF-β) que guía a los fibroblastos en la construcción de tejido nuevo. En las úlceras diabéticas, SKIL se mostró consistentemente hiperactivo y estrechamente vinculado a cambios en el uso de energía por parte de los fibroblastos, en particular una mayor dependencia de vías de quema de azúcar como la glucólisis.
Defensas inflamadas y subtipos de enfermedad a medida
El estudio también examinó las células inmunitarias que infiltran las úlceras del pie diabético. En comparación con la piel normal, las úlceras diabéticas contenían más células inflamatorias —como ciertos macrófagos y neutrófilos— y menos células reguladoras que normalmente ayudan a atenuar la respuesta. Al agrupar las muestras de úlceras según la actividad de genes relacionados con la ubiquitinación, los investigadores descubrieron dos subtipos moleculares distintos: uno dominado por cambios relacionados con la inflamación y el metabolismo, y otro enriquecido en señales implicadas en la formación de vasos y la cicatrización fibrótica. Estos patrones sugieren que no todas las úlceras son iguales a nivel molecular, lo que puede explicar por qué los pacientes responden de forma diferente a los mismos tratamientos y subraya la necesidad de cuidados personalizados.
Nuevas posibilidades terapéuticas a la vista
Debido a que SKIL parecía central en la disfunción de los fibroblastos, los investigadores buscaron en bases de datos fármaco‑gen y usaron simulaciones de acoplamiento molecular para predecir medicamentos que podrían unirse e influir en SKIL. Identificaron dos candidatos: lumicolchicina y ramipril. Ramipril resulta especialmente intrigante porque es un fármaco antihipertensivo ya existente, recetado comúnmente a personas con diabetes. Las simulaciones sugieren que ramipril podría interactuar con SKIL mientras mejora la función vascular, lo que insinúa que esta clase de fármacos familiar podría algún día reutilizarse para ayudar a que las heridas diabéticas cicatricen con mayor eficacia. Estas predicciones aún requieren pruebas de laboratorio y ensayos clínicos, pero abren un camino práctico para traducir los hallazgos moleculares en terapia.
Qué significa esto para pacientes y atención
En conjunto, este trabajo mapea cómo un sistema de etiquetado proteico dentro de los fibroblastos puede desviar su conducta, alimentando la inflamación crónica y la mala reparación en las úlceras del pie diabético. Al identificar un subtipo específico de fibroblasto dañino, definir una firma diagnóstica de cuatro genes y señalar a SKIL como posible diana terapéutica, el estudio ofrece un plano para un diagnóstico más preciso y un tratamiento individualizado. A largo plazo, estrategias informadas molecularmente como estas podrían ayudar a los clínicos a identificar úlceras de alto riesgo antes, adaptar terapias a la biología de cada herida y quizá usar fármacos existentes de nuevas formas para prevenir complicaciones que amenacen las extremidades.
Cita: Wang, W., Peng, X., Hua, Q. et al. Ubiquitination-driven fibroblast dysfunction: a multi-omics blueprint for precision diagnosis and therapy in diabetic foot ulcer. Sci Rep 16, 14669 (2026). https://doi.org/10.1038/s41598-026-45436-x
Palabras clave: úlcera del pie diabético, fibroblastos, ubiquitinación, cicatrización de heridas, medicina de precisión