Clear Sky Science · es
Productos avanzados de glicación dietética combinados con estrés por restricción crónica inducen comportamientos similares a la ansiedad y la depresión en ratones macho
Por qué la comida cotidiana y el estrés influyen en el estado de ánimo
Hoy muchas personas combinan altos niveles de estrés con comidas rápidas llenas de productos procesados, alimentos quemados o fritos. Este estudio plantea una pregunta simple pero importante: cuando una dieta poco saludable y el estrés crónico coinciden, ¿pueden actuar en conjunto para empeorar la ansiedad y la depresión? Usando ratones macho, los investigadores siguieron cómo interactúan ciertos compuestos procedentes de alimentos cocinados, las bacterias intestinales y las células cerebrales, revelando una cadena de eventos que vincula lo que comemos y el estrés con cambios cerebrales que recuerdan a trastornos del ánimo.
Partículas quemadas en la comida y un cuerpo estresado
El trabajo se centra en compuestos llamados productos finales de glicación avanzada, o AGE, que se forman cuando los alimentos se cocinan a altas temperaturas, como al asar o freír. Estos compuestos están presentes en muchos alimentos ultraprocesados. El equipo expuso a los ratones a una dieta rica en AGE durante 12 semanas y añadió estrés por restricción diario durante el último mes, imitando un estilo de vida de tensión crónica y comidas muy procesadas. En comparación con los animales de control, los ratones estresados ya mostraban signos de conductas similares a la ansiedad y la depresión, como menor placer por soluciones dulces y más inmovilidad en pruebas estándar. Añadir AGE además del estrés empeoró notablemente estos comportamientos, y el tejido cerebral de áreas clave del estado de ánimo mostraba más daño y niveles reducidos de proteínas que sostienen conexiones nerviosas saludables.
El papel oculto del intestino en el estado de ánimo
Para entender cómo la comida y el estrés se comunican con el cerebro, los investigadores se centraron en el intestino. Hallaron que el estrés y los AGE juntos alteraron la comunidad microbiana intestinal, reduciendo la diversidad general y aumentando cepas previamente asociadas con inflamación y desequilibrio químico. Al mismo tiempo, la barrera intestinal—normalmente una muralla estrecha que controla lo que pasa al torrente sanguíneo—se volvió permeable. La microscopía reveló tejido inflamado y pérdida de células secretoras de moco protectoras, mientras que proteínas clave de sellado en el intestino y en la barrera sangre–cerebro se vieron reducidas. Estos cambios permitieron que señales inflamatorias y ciertas pequeñas moléculas circularan más libremente e influyeran en el cerebro, preparando el terreno para cambios químicos más profundos. 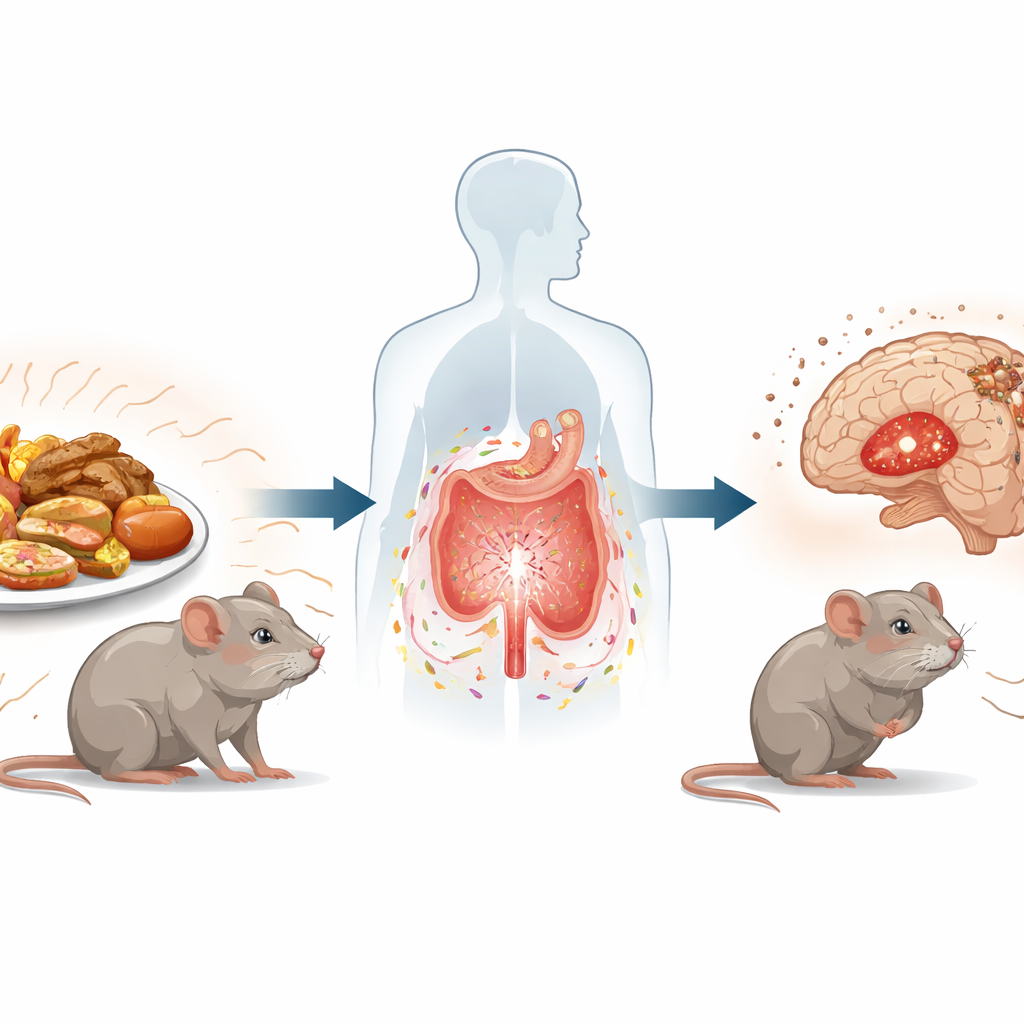
Un atasco en la química del triptófano
El estudio se centró en el triptófano, un aminoácido conocido principalmente como precursor de la serotonina, un mensajero relacionado con el estado de ánimo. En condiciones saludables, el triptófano alimenta tanto la producción de serotonina como otra vía llamada ruta de la quinurenina. Bajo la combinación de AGE y estrés, ese equilibrio se inclinó drásticamente. Se encontraron menos triptófano y serotonina en el cerebro y en el cuerpo, mientras que más se desvió hacia la quinurenina y productos posteriores como la 3-hidroxiquinurenina. Estos metabolitos pueden cruzar al cerebro y se sabe que favorecen el estrés oxidativo, básicamente una corrosión química dentro de las células. Cuando los investigadores bloquearon la enzima clave que impulsa este cambio usando un fármaco llamado 1-metiltriptófano, los niveles de estos subproductos tóxicos bajaron, la química cerebral mejoró y los ratones mostraron menos conductas similares a la ansiedad y la depresión.
Cuando las células cerebrales se oxidan desde dentro
Más a fondo, el equipo descubrió un tipo específico de muerte celular en el hipocampo, una región cerebral vinculada a la memoria y la emoción. Este proceso, llamado ferroptosis, está impulsado por la acumulación de hierro y la oxidación lipídica descontrolada. Los ratones expuestos tanto a AGE como al estrés mostraron niveles más altos de hierro, defensas antioxidantes más débiles y mitocondrias—las centrales energéticas de la célula—con estructuras encogidas y dañadas, características de la ferroptosis. Inhibir esta vía de muerte celular con un compuesto llamado ferrostatina-1 protegió a las neuronas y alivió los síntomas conductuales, aunque no corrigió el desequilibrio del triptófano aguas arriba. En células nerviosas en cultivo, añadir quinurenina o 3-hidroxiquinurenina por sí solos fue suficiente para desencadenar ferroptosis, vinculando de forma sólida estos metabolitos relacionados con la dieta y el estrés con la pérdida de células cerebrales impulsada por el hierro. 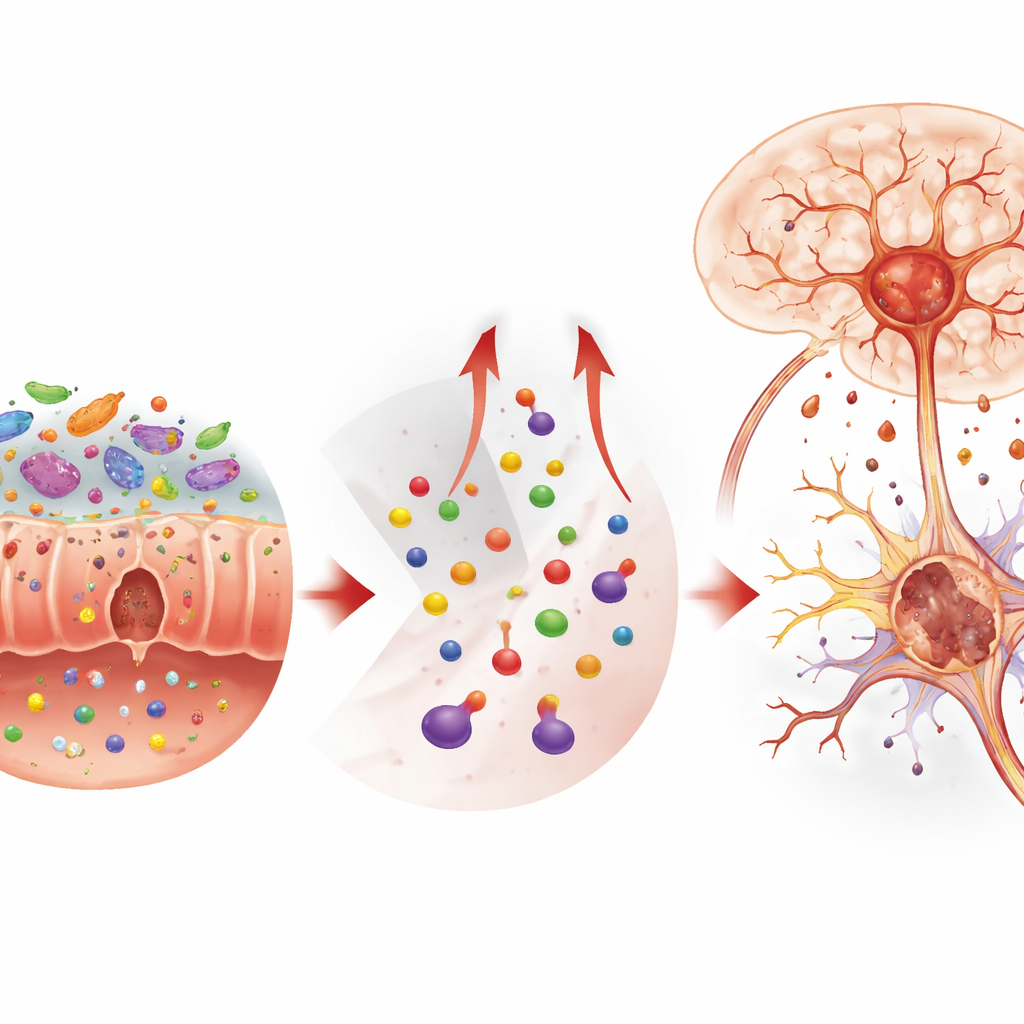
Qué significa esto para la vida cotidiana
En conjunto, los hallazgos dibujan una historia por pasos: la ingesta frecuente de alimentos muy cocinados y ricos en AGE combinada con estrés persistente primero desestabiliza el microbioma intestinal y debilita las barreras intestinal y cerebral. Este entorno empuja el metabolismo del triptófano lejos de la serotonina y hacia productos quinurenínicos tóxicos, que luego se acumulan en las neuronas y desencadenan muerte celular dependiente del hierro. En ratones, esta cadena termina en conductas similares a la ansiedad y la depresión. Aunque se necesita más trabajo en humanos, el estudio sugiere que manejar el estrés, limitar los alimentos ultraprocesados y muy dorados, y orientar este eje intestino–triptófano–cerebro podrían convertirse en estrategias potentes para prevenir o tratar los trastornos del ánimo.
Cita: Zhang, Y., Gu, K., Xin, L. et al. Dietary advanced glycation products combined with chronic restraint stress induced anxiety-like and depression-like behaviors in male mice. npj Sci Food 10, 135 (2026). https://doi.org/10.1038/s41538-026-00789-5
Palabras clave: eje intestino–cerebro, alimentos procesados, metabolismo del triptófano, ferroptosis, ansiedad y depresión