Clear Sky Science · es
La estructura del filamento flagelar de Vibrio alginolyticus sugiere un mecanismo molecular para la rotación de flagelos envueltos
Propulsores ocultos de microbios dañinos
Muchas bacterias causantes de enfermedades dependen de pequeños propulsores giratorios, llamados flagelos, para nadar a través de líquidos y alcanzar nuestras células. En algunas especies, entre ellas Vibrio alginolyticus, estos propulsores están envueltos en una cubierta externa blanda formada por la membrana de la propia célula. Este estudio revela cómo se ensamblan estos propulsores «envueltos» y cómo pueden girar a gran velocidad sin rozar contra su vaina, una cuestión relevante para entender tanto el movimiento bacteriano como la manera en que estos microbios eluden nuestro sistema inmunitario. 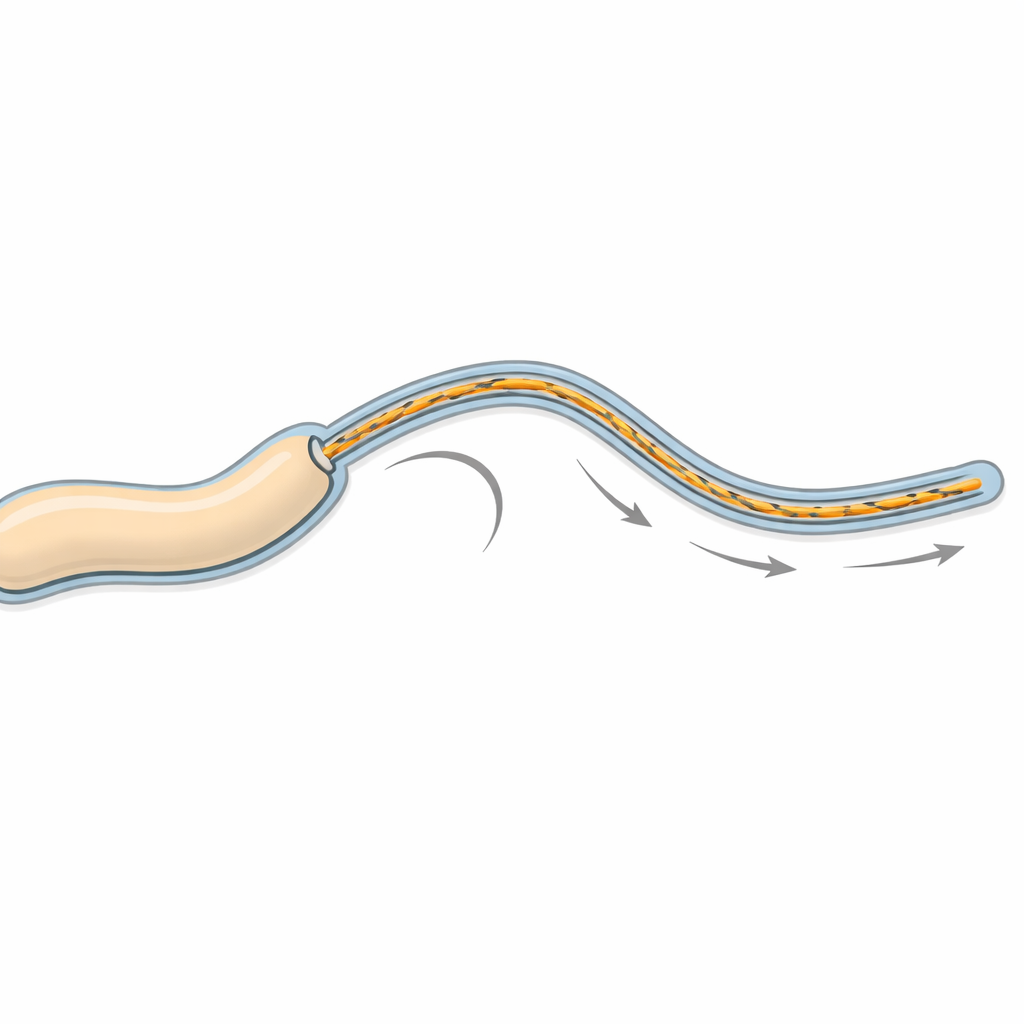
Un propulsor envuelto en su propio abrigo
Los investigadores se centraron en Vibrio alginolyticus, una bacteria marina que puede infectar peces, mariscos y humanos. Como su pariente Vibrio cholerae, posee un único flagelo potente en un polo celular que está envuelto por una vaina formada a partir de la membrana externa, la misma envoltura que mira al exterior. Empleando microscopía electrónica avanzada captaron imágenes tridimensionales de alta resolución de estos filamentos envueltos. Las imágenes muestran que el núcleo del flagelo forma un familiar haz helicoidal de 11 hebras, muy parecido a los flagelos sin envoltura de otras bacterias, pero aquí ese haz está rodeado ordenadamente por un tubo membranoso de doble capa que continúa sin interrupción desde la superficie celular.
El bloque constructivo principal del propulsor
Vibrio alginolyticus tiene seis genes estrechamente relacionados que, en principio, podrían aportar los bloques constructivos de su flagelo polar. Para averiguar cuál es el esencial, el equipo combinó pistas estructurales de sus imágenes con pruebas genéticas. Al eliminar estos genes uno por uno y medir la capacidad de natación de las bacterias, descubrieron que una proteína, llamada FlaD2, es fundamental: las células sin FlaD2 quedaban casi completamente inmóviles, mientras que la pérdida de las demás tenía poco efecto. Las estructuras detalladas de filamentos envueltos y no envueltos coinciden con la forma de FlaD2, lo que confirma que esta única proteína forma el eje principal del propulsor, apilada decenas de miles de veces para crear un largo filamento superenrollado.
Cómo girar rápido sin raspar la vaina
Un rompecabezas clave era cómo el filamento interior puede rotar rápidamente dentro de su cubierta membranosa sin desgarrarla ni frenarla. Al calcular la carga eléctrica en la superficie del filamento FlaD2, los científicos hallaron algo llamativo: a diferencia de la mayoría de flagelos bacterianos, que son bastante neutros, el filamento de Vibrio es fuertemente negativo en toda su superficie. Se espera que la superficie interna de la vaina membranosa circundante también sea negativa debido a los grupos polares de sus lípidos. Como dos imanes con el mismo polo enfrentado, estas superficies se repelen. El equipo propone que esta repulsión electrostática impide el contacto entre filamento y vaina, creando una fina separación lubricante que permite que el núcleo gire libremente a gran velocidad con muy poca fricción, incluso mientras la vaina flexible puede doblarse y deformarse mientras la bacteria nada. 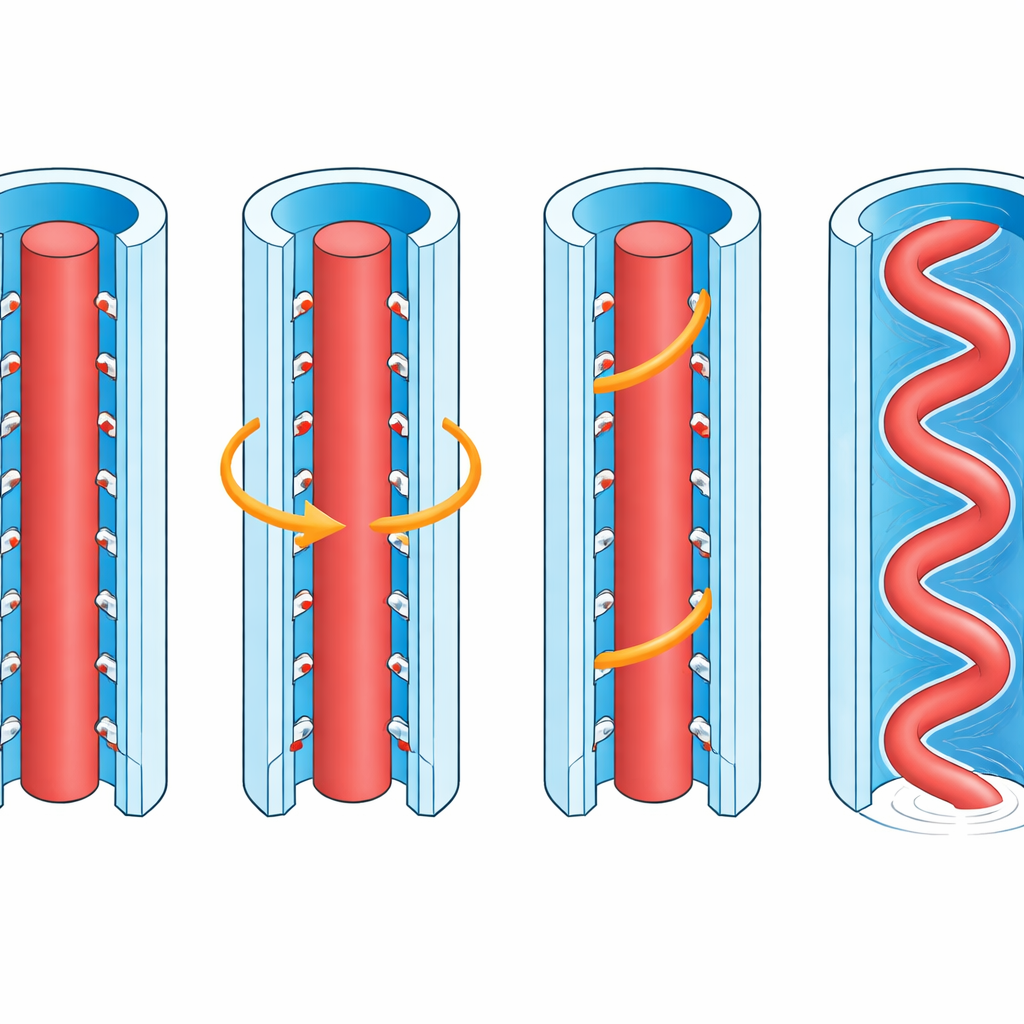
Una punta especial que mantiene el crecimiento coordinado
En el extremo distal de cada flagelo hay una tapa compuesta por una proteína llamada FliD, que ayuda a que nuevos bloques constructivos se añadan al filamento en crecimiento. En Vibrio y en algunas otras bacterias envueltas, esta tapa posee un dominio adicional ausente en la mayoría de las especies. Los modelos estructurales sugieren que esta pieza extra, denominada D4, se sitúa como una amplia falda en la parte superior del filamento y tiene casi el mismo ancho que la capa interna de la vaina. Cuando los investigadores eliminaron este dominio de la tapa, las bacterias aún podían fabricar flagelos funcionales y nadar, pero la microscopía electrónica a veces mostró tubos de vaina vacíos que se prolongaban más allá de la punta del filamento. Esto sugiere que el dominio D4 normalmente ayuda a mantener sincronizado el crecimiento del filamento sólido y de la vaina circundante, evitando que la vaina crezca más rápido que su núcleo giratorio.
Qué significa esto para la infección y estudios futuros
En conjunto, estos hallazgos respaldan una imagen física sencilla: en los flagelos envueltos, la cubierta de membrana no rota como una unidad rígida con el filamento. En cambio, el filamento gira libremente dentro de un tubo flexible, mantenido alejado de las paredes por repulsión de cargas, mientras una punta especializada ayuda a que la vaina y el filamento crezcan juntos. Esta disposición puede permitir que las bacterias Vibrio se desplacen rápidamente, desprendan pequeñas burbujas de membrana que pueden transportar factores de virulencia y oculten partes clave del flagelo a los sensores inmunitarios. Al revelar cómo la naturaleza construye un motor de alta velocidad y baja fricción en una funda blanda, el estudio proporciona un marco para entender estructuras similares en otros patógenos y puede inspirar nuevas estrategias para interrumpir el movimiento bacteriano durante la infección.
Cita: Qin, K., Einenkel, R., Zhao, W. et al. The structure of the Vibrio alginolyticus flagellar filament suggests molecular mechanism for the rotation of sheathed flagella. Nat Commun 17, 3532 (2026). https://doi.org/10.1038/s41467-026-71203-7
Palabras clave: motilidad bacteriana, flagelos envueltos, Vibrio alginolyticus, crio-microscopía electrónica, repulsión electrostática