Clear Sky Science · de
Die Struktur des Flagellenfilaments von Vibrio alginolyticus deutet auf einen molekularen Mechanismus für die Rotation umhüllter Flagellen hin
Verborgene Propeller schädlicher Mikroben
Viele krankheitserregende Bakterien verlassen sich auf winzige drehende Propeller, sogenannte Flagellen, um sich durch Flüssigkeit zu bewegen und unsere Zellen zu erreichen. Bei einigen Arten, darunter Vibrio alginolyticus, sind diese Propeller in eine weiche Außenhülle aus der eigenen Membran des Zellkörpers eingebettet. Diese Studie zeigt, wie diese umhüllten "sheathed" Propeller aufgebaut sind und wie sie sich mit hoher Geschwindigkeit drehen können, ohne an ihrer Hülle zu scheuern — eine Frage, die sowohl für das Verständnis bakterieller Bewegung als auch dafür relevant ist, wie diese Mikroben dem Immunsystem entgehen. 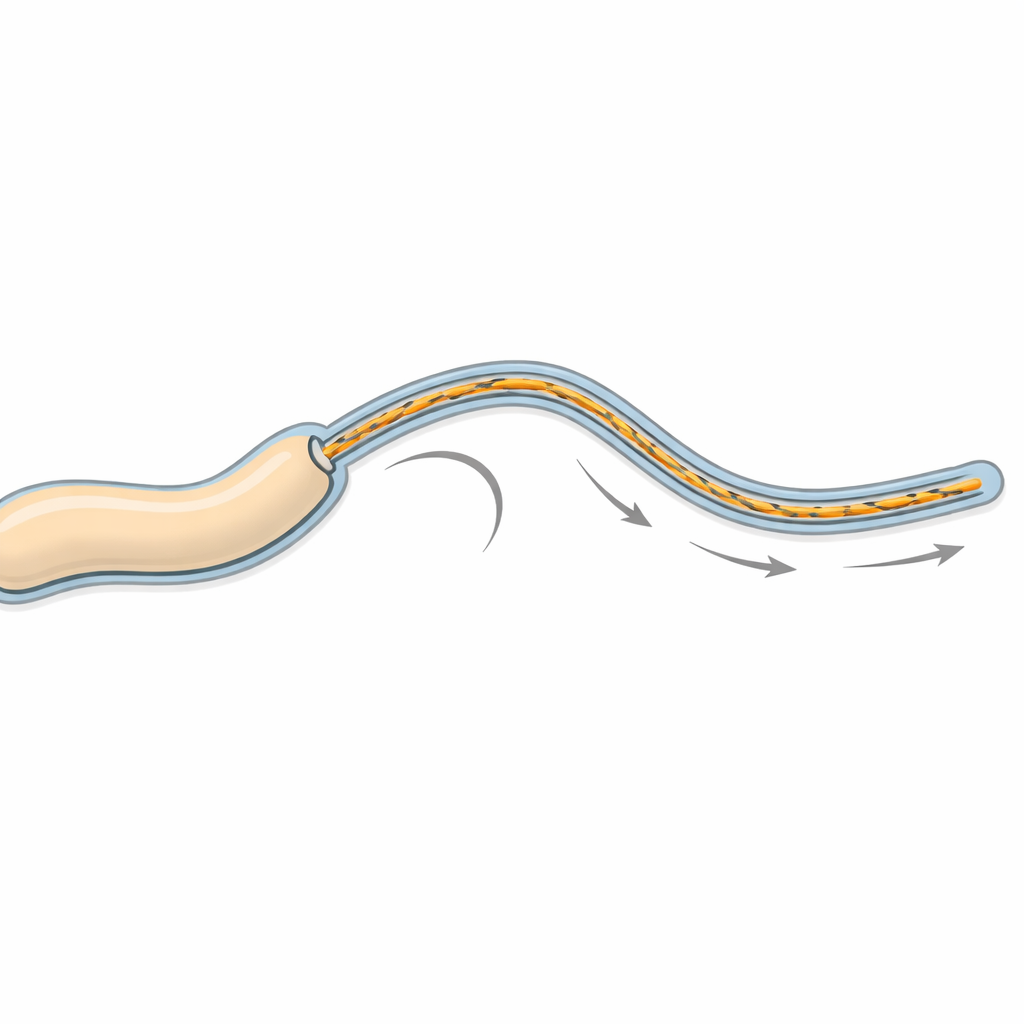
Ein Propeller in seinem eigenen Mantel
Die Forschenden konzentrierten sich auf Vibrio alginolyticus, ein Meeresbakterium, das Fische, Schalentieren und Menschen infizieren kann. Wie sein Verwandter Vibrio cholerae besitzt es an einem Zellpol eine einzelne leistungsstarke Flagelle, die in einer Hülle aus der äußeren Membran liegt — derselben Membranschicht, die nach außen zeigt. Mit fortschrittlicher Elektronenmikroskopie erzeugten sie hochauflösende Dreidimensionalbilder dieser umhüllten Filamente. Die Aufnahmen zeigen, dass der Kern der Flagelle ein vertrautes spiraliges Bündel aus 11 Strängen bildet, ähnlich wie unbehüllte Flagellen anderer Bakterien, aber hier ist dieses Bündel ordentlich von einer doppelschichtigen Membrantube umgeben, die nahtlos von der Zelloberfläche fortgesetzt wird.
Der Hauptbaustein des Propellers
Vibrio alginolyticus trägt sechs eng verwandte Gene, die prinzipiell die Bausteine seiner polaren Flagelle liefern könnten. Um herauszufinden, welches davon wirklich entscheidend ist, kombinierten die Forschenden strukturelle Hinweise aus ihren Bildern mit genetischen Tests. Durch das gezielte Entfernen dieser Gene einzeln und die Messung der Schwimmfähigkeit der Zellen stellten sie fest, dass ein Protein, genannt FlaD2, essentiell ist: Zellen ohne FlaD2 wurden nahezu vollständig unbeweglich, während der Verlust der anderen Gene wenig Wirkung zeigte. Die detaillierten Strukturen sowohl der umhüllten als auch der unbehüllten Filamente entsprechen der Form von FlaD2 und bestätigen, dass dieses einzelne Protein die Hauptachse des Propellers bildet und zehntausendfach aufgestapelt einen langen supergewickelten Filamentstrang ergibt.
Wie man schnell dreht, ohne die Hülle zu zerkratzen
Ein zentrales Rätsel war, wie das innere Filament sich schnell in seiner Membranhülle drehen kann, ohne sie zu zerreißen oder zu bremsen. Durch Berechnung der elektrischen Ladung auf der Oberfläche des FlaD2-Filaments fanden die Wissenschaftler etwas Auffälliges: Im Gegensatz zu den meisten bakteriellen Flagellen, die relativ neutral sind, ist das Vibrio-Filament überall stark negativ geladen. Auch die Innenseite der umgebenden Membranhülle wird aufgrund der polaren Kopfgruppen der Lipide voraussichtlich negativ geladen sein. Wie zwei Magnete mit gleichnamigen Polen stoßen sich diese Oberflächen ab. Das Team schlägt vor, dass diese elektrostatische Abstoßung das Filament von der Hülle fernhält und einen dünnen, schmierenden Spalt erzeugt, der dem Kern erlaubt, sich mit sehr wenig Reibung frei und schnell zu drehen, während die flexible Hülle sich beim Schwimmen biegen und verformen kann. 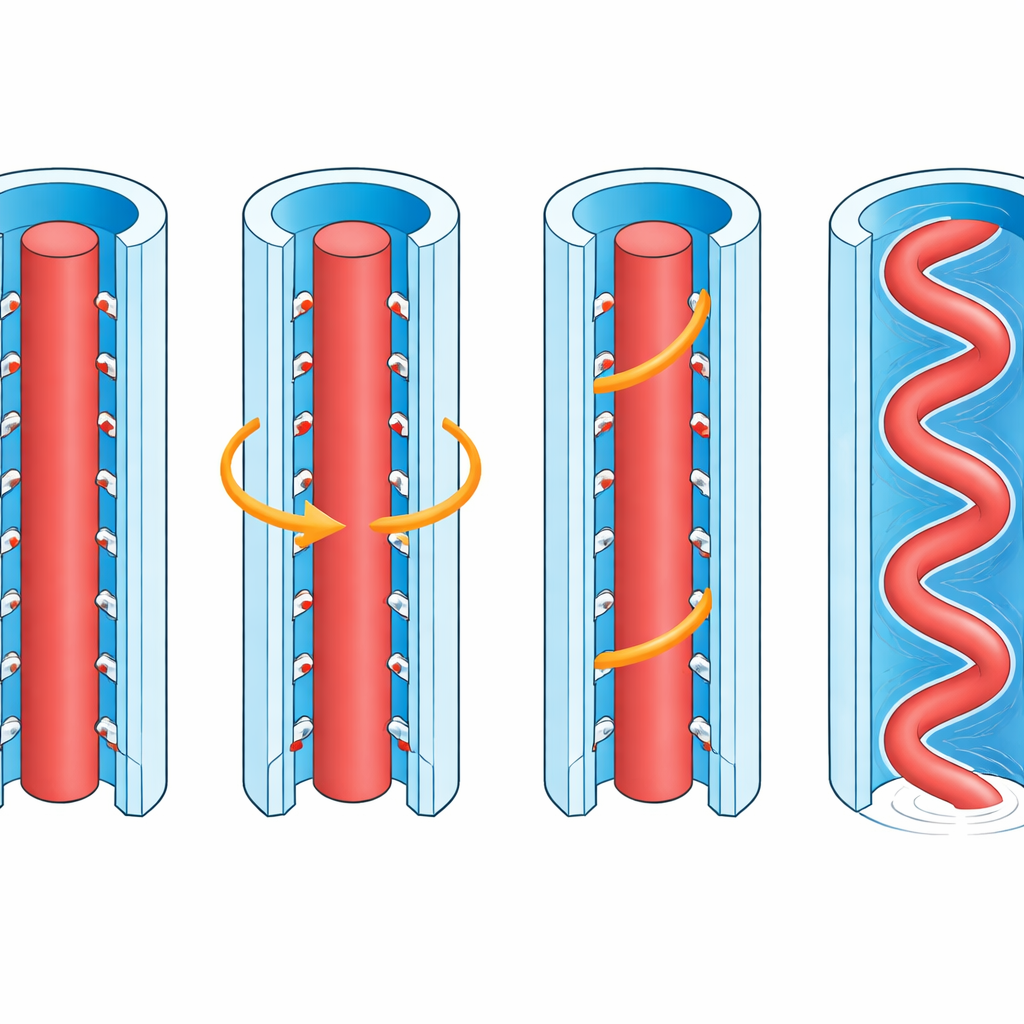
Eine besondere Spitze, die das Wachstum synchronisiert
Am Ende jeder Flagelle sitzt eine Kappe aus einem Protein namens FliD, das neue Bausteine beim Aufbau des Filaments anlagert. Bei Vibrio und einigen anderen umhüllten Bakterien trägt diese Kappe eine zusätzliche Domäne, die bei den meisten Arten nicht vorkommt. Strukturelle Modelle legen nahe, dass dieses zusätzliche Stück, D4 genannt, wie ein weiter Rock oben am Filament sitzt und etwa die gleiche Breite wie die innere Schicht der Hülle besitzt. Entfernten die Forschenden diese Domäne aus der Kappe, konnten die Bakterien weiterhin funktionelle Flagellen bauen und schwimmen, doch die Elektronenmikroskopie zeigte gelegentlich leere Hüllröhren, die über die Filamentspitze hinausragten. Das deutet darauf hin, dass die D4-Domäne normalerweise hilft, das Wachstum des festen Filaments und der äußerlichen Hülle zu synchronisieren und so verhindert, dass die Hülle ihren rotierenden Kern überholt.
Was das für Infektionen und künftige Studien bedeutet
Zusammen stützen diese Befunde ein einfaches physikalisches Bild: Bei umhüllten Flagellen dreht sich die Membranhülle nicht starr mit dem Filament mit. Stattdessen rotiert das Filament frei in einer flexiblen Röhre, die durch ladungsbedingte Abstoßung von den Wänden ferngehalten wird, während eine spezialisierte Spitze das gleichzeitige Wachstum von Hülle und Filament fördert. Diese Anordnung könnte es Vibrio-Bakterien ermöglichen, sich schnell zu bewegen, kleine Membranbläschen abzusondern, die Virulenzfaktoren transportieren, und zentrale Bestandteile der Flagelle vor Immunrezeptoren zu verbergen. Indem die Studie zeigt, wie die Natur einen hochdrehenden, reibungsarmen Motor in einer weichen Hülle konstruiert, liefert sie einen Rahmen zum Verständnis ähnlicher Strukturen anderer Krankheitserreger und könnte neue Ansätze inspirieren, bakterielle Bewegung während Infektionen zu stören.
Zitation: Qin, K., Einenkel, R., Zhao, W. et al. The structure of the Vibrio alginolyticus flagellar filament suggests molecular mechanism for the rotation of sheathed flagella. Nat Commun 17, 3532 (2026). https://doi.org/10.1038/s41467-026-71203-7
Schlüsselwörter: bakterielle Motilität, umhüllte Flagellen, Vibrio alginolyticus, Cryo-Elektronenmikroskopie, elektrostatische Abstoßung