Clear Sky Science · es
La bioconjugación electroquímica dirigida a tirosina habilita la detección multiplexada de citocinas y el inmunoperfilado en suero nativo
Por qué importan las señales diminutas en la sangre
Médicos y científicos a menudo quieren leer las señales inmunitarias del cuerpo con sólo unas gotas de sangre, para seguir infecciones, cáncer o los efectos de la contaminación en tiempo real. Estas señales son transportadas por pequeñas proteínas llamadas citocinas, pero medir varias de ellas a la vez en sangre sin tratar es difícil. Los sensores usados hoy en día con frecuencia pierden actividad, ofrecen lecturas inestables o requieren horas de preparación. Este estudio introduce un truco rápido de química de superficie que ayuda a construir mejores sensores electroquímicos, facilitando el perfilado de respuestas inmunitarias directamente en muestras complejas como el suero nativo.
Una nueva forma de anclar proteínas en electrodos
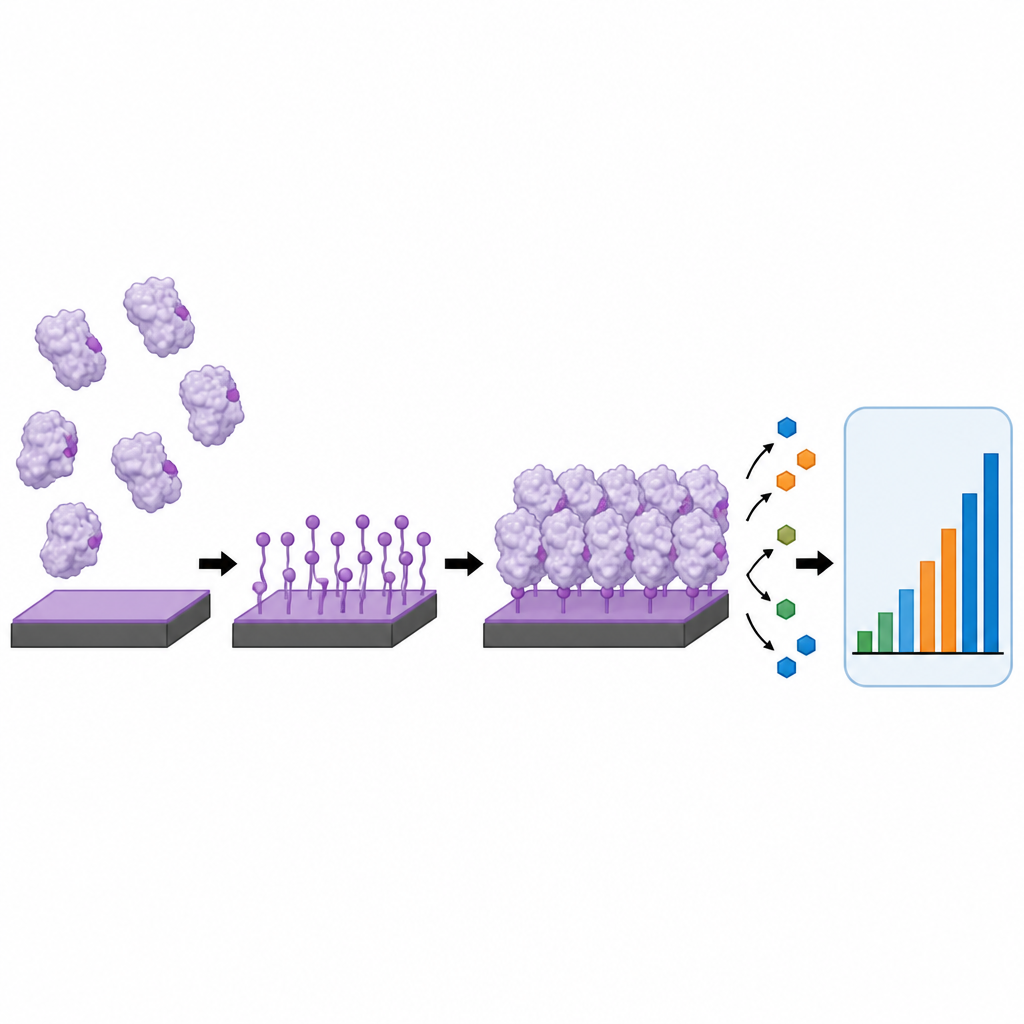
En el corazón de muchos biosensores electroquímicos hay un electrodo plano recubierto con una capa cuidadosamente ordenada de proteínas, como anticuerpos o enzimas. La forma en que estas proteínas se unen afecta en gran medida al rendimiento del sensor. Los métodos comunes, como la adsorción simple o el acoplamiento químico lento, a menudo dejan a las proteínas en orientaciones aleatorias, crean agregados o se desprenden con el tiempo. Los autores desarrollaron un enfoque que llaman clic electroquímico interfacial sobre tirosina, o i-eY-Click, que usa una señal eléctrica suave para activar una película fina sobre una superficie de carbono. Esta película activada reacciona selectivamente con residuos de tirosina expuestos en las proteínas, formando una capa proteica delgada, densa y estable en menos de tres minutos sin necesitar reactivos adicionales ni modificaciones genéticas.
Química rápida y suave que mantiene la actividad de las proteínas
El equipo confirmó primero que esta reacción centrada en la tirosina era realmente rápida, selectiva y robusta. Demostraron que la película especial sobre el electrodo podía activarse en su forma reactiva con un voltaje suave que no daña las proteínas. En comparación con un método estándar de acoplamiento por amida, i-eY-Click unió sondas moleculares unas veinte veces más rápido y alcanzó una mayor cobertura en solo unos minutos frente a la hora que requería la química antigua. Microscopía y mediciones de superficie revelaron que el nuevo método producía capas lisas y uniformes que permanecían en su lugar incluso después de lavados agresivos, mientras que las proteínas únicamente adsorbidas físicamente formaban parches desiguales y se eliminaban fácilmente. De manera importante, pruebas con varias enzimas mostraron que su actividad y sensibilidad a sustratos se preservaban en gran medida tras esta fijación eléctrica tipo “clic”.
Convertir mejor química en mejores sensores inmunitarios
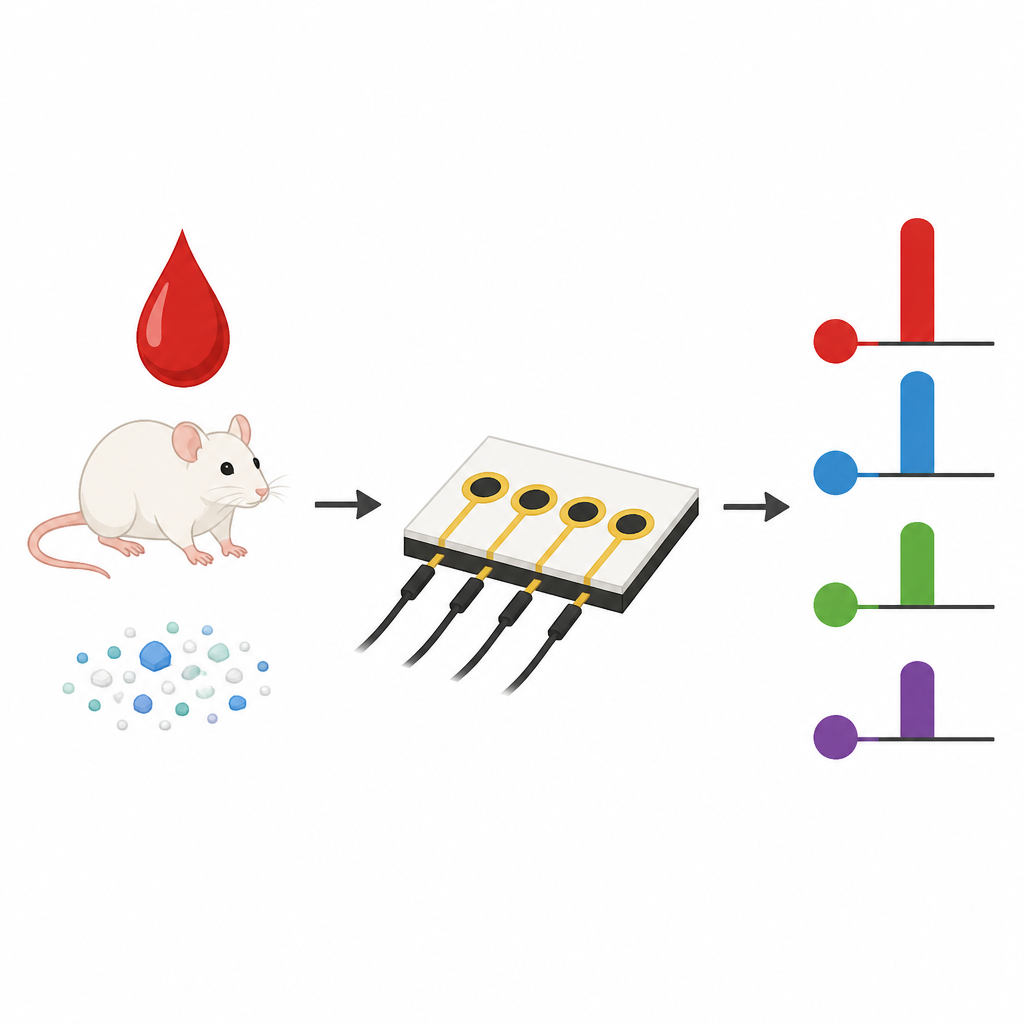
Basándose en esta química de superficie, los investigadores fabricaron pequeños chips con matrices de microelectrodos de carbono. Cada posición de la matriz fue recubierta por i-eY-Click con un anticuerpo distinto que reconoce una citocina inflamatoria específica, incluyendo IL-6, IL-1β, TNF-α e IFN-γ. Cuando se añade una pequeña muestra de sangre, las citocinas objetivo se unen a sus anticuerpos coincidentes, y un paso enzimático estándar convierte esta unión en una corriente eléctrica. En comparación con sensores hechos mediante la química de acoplamiento tradicional, los nuevos chips requirieron solo minutos para prepararse, mostraron señales más fuertes y detectaron citocinas a concentraciones más bajas. En suero de ratón no diluido, ofrecieron mayor sensibilidad, límites de detección inferiores y una reproducibilidad mucho mejor de punto a punto y de lote a lote, características cruciales para el uso diagnóstico práctico.
Vigilar la respuesta del organismo a los nanoplásticos
Para demostrar el valor en condiciones reales, los autores usaron su plataforma para monitorizar cómo respondía el sistema inmunitario de ratones a lo largo del tiempo frente a diferentes partículas nanoplásticas, incluyendo ácido poliláctico y perlas de poliestireno cargadas. Tras una única inyección, recogieron diminutas muestras de suero en varios puntos temporales y midieron las cuatro citocinas en paralelo. Los chips revelaron cursos temporales distintivos de cambios en citocinas que dependían de la carga superficial y la degradabilidad de las partículas. Algunas partículas desencadenaron picos breves y moderados en marcadores inflamatorios, mientras que partículas con carga positiva o degradables se asociaron con respuestas más intensas o prolongadas. Estos patrones fueron coherentes con pruebas de laboratorio convencionales y con imágenes de tejido que mostraron distintos niveles de daño cerebral e inflamación.
Qué significa esto para la monitorización futura de la salud y el medio ambiente
Este trabajo muestra que una química de superficie cuidadosamente diseñada puede desbloquear biosensores electroquímicos más fiables y sensibles. Al usar una reacción rápida de "clic" eléctrica dirigida a la tirosina, los autores crean capas proteicas duraderas y bien organizadas que permiten mediciones multiplexadas de citocinas en volúmenes diminutos de suero nativo. Aunque el estudio sobre nanoplásticos es exploratorio, ilustra cómo tales chips podrían emplearse para seguir respuestas inmunitarias a materiales, enfermedades o terapias a lo largo del tiempo. A largo plazo, este enfoque podría ayudar a desarrollar dispositivos compactos y asequibles que lean señales inmunitarias junto a la cama del paciente o en el campo, proporcionando instantáneas más claras de cómo el organismo reacciona a su entorno.
Cita: Song, K., Liu, Y., Ma, Q. et al. Electrochemical tyrosine-click bioconjugation enables multiplexed cytokine sensing and immunoprofiling in native serum. Nat Commun 17, 4251 (2026). https://doi.org/10.1038/s41467-026-70815-3
Palabras clave: biosensor electroquímico, detección de citocinas, inmovilización de proteínas, exposición a nanoplásticos, inmunoperfilado