Clear Sky Science · de
Elektrochemische Tyrosin-Click-Biokonjugation ermöglicht multiplexe Zytokin-Sensorik und Immunprofiling in nativen Seren
Warum winzige Signale im Blut wichtig sind
Ärztinnen, Ärzte und Forschende möchten oft die Immun-Signale des Körpers schon aus wenigen Blutstropfen ablesen, um Infektionen, Krebs oder die Auswirkungen von Umweltverschmutzung in Echtzeit zu verfolgen. Diese Signale werden von kleinen Proteinen, den Zytokinen, getragen; mehrere davon gleichzeitig in unbehandeltem Blut zu messen, ist jedoch schwierig. Heutige Sensoren verlieren häufig an Aktivität, liefern instabile Messwerte oder benötigen Stunden zur Vorbereitung. Die vorliegende Studie stellt einen schnellen Oberflächenchemie-Trick vor, der den Aufbau besserer elektrochemischer Sensoren ermöglicht und so das Immunprofiling direkt in komplexen Proben wie nativem Serum erleichtert.
Eine neue Art, Proteine auf Elektroden zu verankern
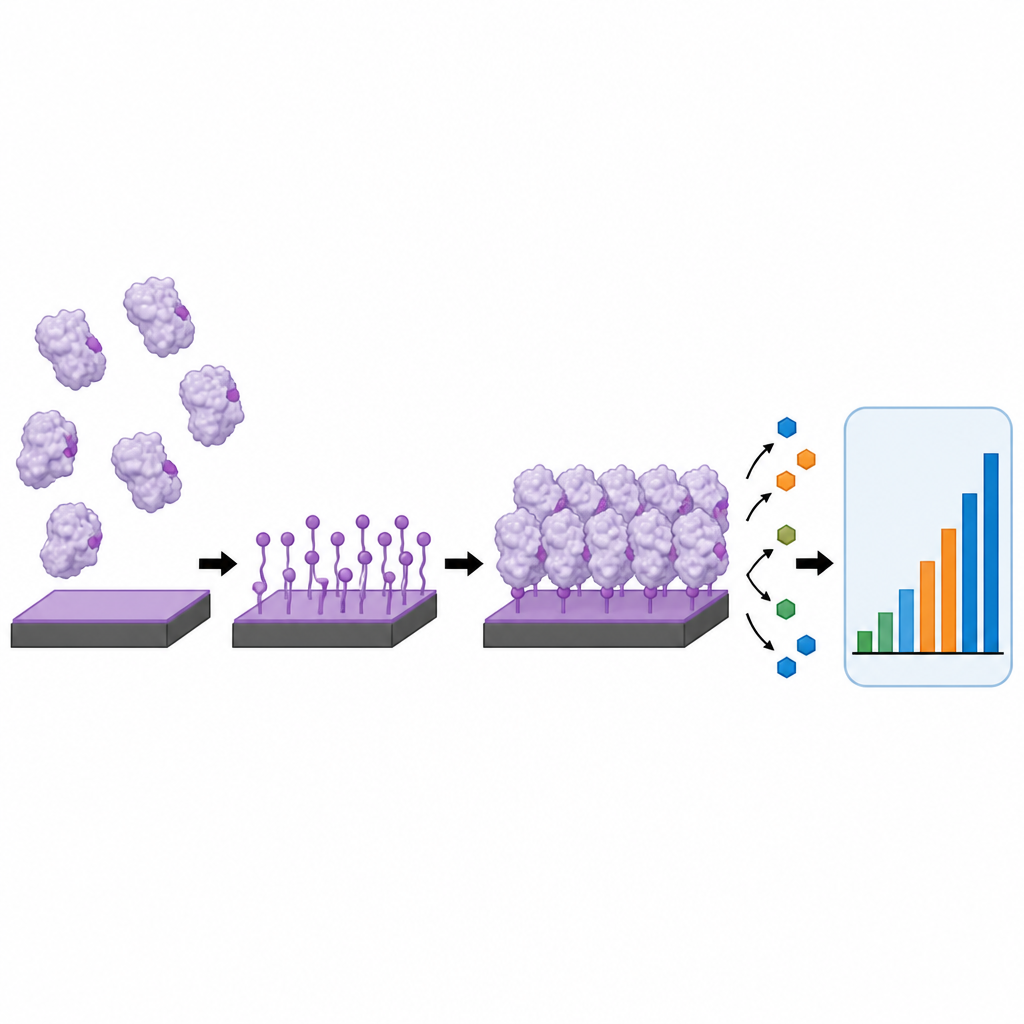
Im Kern vieler elektrochemischer Biosensoren steht eine ebene Elektrode, die mit einer sorgfältig angeordneten Proteinschicht, etwa Antikörpern oder Enzymen, beschichtet ist. Wie diese Proteine befestigt werden, beeinflusst die Sensorleistung stark. Gängige Methoden wie einfaches Adsorbieren oder langsame chemische Kupplung lassen Proteine oft in zufälligen Orientierungen, führen zu Klumpen oder werden mit der Zeit abgewaschen. Die Autorinnen und Autoren entwickelten einen Ansatz, den sie interfacial electrochemical tyrosine click oder i-eY-Click nennen. Dabei wird ein mildes elektrisches Signal genutzt, um eine dünne Schicht auf einer Kohlenstoffoberfläche zu aktivieren. Diese aktivierte Schicht reagiert dann selektiv mit Tyrosin-Bausteinen an der Außenseite von Proteinen und bildet in unter drei Minuten eine dünne, dichte und stabile Proteinschicht – ganz ohne zusätzliche Reagenzien oder genetische Modifikation.
Schnelle, schonende Chemie, die Proteine funktionsfähig hält
Das Team bestätigte zunächst, dass diese tyrosinorientierte Reaktion wirklich schnell, selektiv und robust ist. Sie zeigten, dass die Spezialschicht auf der Elektrode bei einer schonenden Spannung in ihre reaktive Form geschaltet werden kann, die Proteine nicht schädigt. Im Vergleich zu einer üblichen Amidkupplungs-Methode band i-eY-Click molekulare Sonden etwa zwanzigmal schneller an und erreichte in wenigen Minuten eine höhere Abdeckung als die ältere Chemie in einer Stunde. Mikroskopie und Oberflächenmessungen zeigten, dass die neue Methode glatte, einheitliche Schichten erzeugt, die auch nach starkem Waschen an Ort und Stelle blieben, während physikalisch adsorbierte Proteine ungleichmäßige Flecken bildeten und leicht entfernt wurden. Wichtig ist, dass Tests mit mehreren Enzymen zeigten, dass deren Aktivität und Substratempfindlichkeit durch diese elektrische „Click“-Bindung weitgehend erhalten blieben.
Aus besserer Chemie werden bessere Immunsensoren
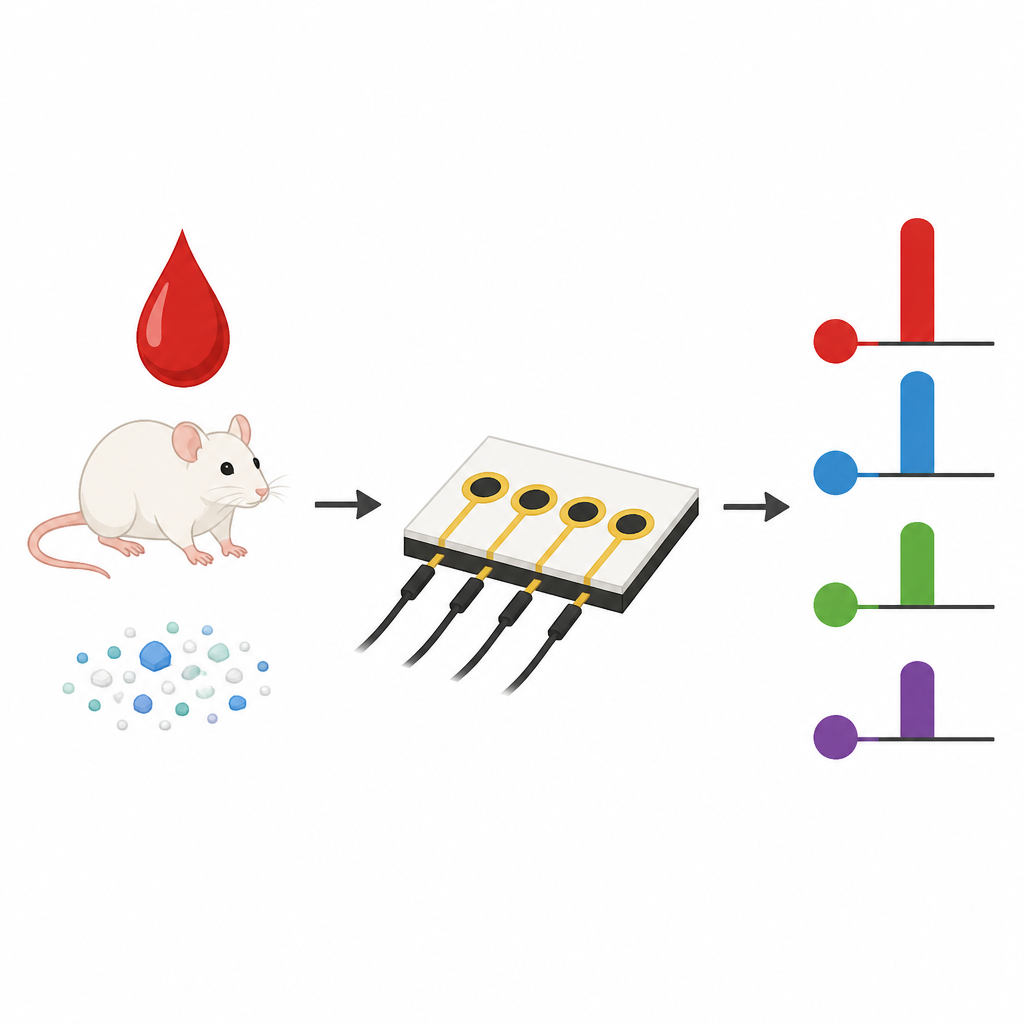
Aufbauend auf dieser Oberflächenchemie fertigten die Forschenden kleine Chips mit Arrays aus Kohlenstoff-Mikroelektroden. Jeder Punkt des Arrays wurde mittels i-eY-Click mit einem verschiedenen Antikörper beschichtet, der ein spezifisches entzündungsförderndes Zytokin erkennt, darunter IL-6, IL-1β, TNF-α und IFN-γ. Wenn eine kleine Blutprobe zugegeben wird, binden die Zielzytokine an ihre passenden Antikörper, und ein standardisierter Enzymschritt wandelt diese Bindung in einen elektrischen Strom um. Gegenüber Sensoren, die mit herkömmlicher Kupplungschemie hergestellt wurden, benötigten die neuen Chips nur Minuten zur Vorbereitung, zeigten stärkere Signale und erkannten Zytokine in niedrigeren Konzentrationen. In undilutiertem Mausserum lieferten sie höhere Empfindlichkeit, geringere Nachweisgrenzen und deutlich bessere Reproduzierbarkeit von Punkt zu Punkt und von Charge zu Charge — entscheidende Eigenschaften für den praktischen diagnostischen Einsatz.
Beobachtung der Körperantwort auf Nanoplastik
Um den realen Nutzen zu demonstrieren, nutzten die Autorinnen und Autoren ihre Plattform, um zu verfolgen, wie das Immunsystem von Mäusen über die Zeit auf verschiedene Nanoplastikpartikel reagierte, darunter Polymilchsäure und geladene Polystyrolkügelchen. Nach einer einmaligen Injektion entnahmen sie winzige Serumproben zu mehreren Zeitpunkten und maßen die vier Zytokine parallel. Die Chips zeigten unterschiedliche Zeitverläufe der Zytokinänderungen, die von der Oberflächenladung und Abbaubarkeit der Partikel abhingen. Manche Partikel lösten kurze, moderate Spitzen in Entzündungsmarkern aus, während positiv geladene oder abbaubare Partikel mit stärkeren oder länger anhaltenden Reaktionen assoziiert waren. Diese Muster stimmten mit konventionellen Labortests und mit Gewebeaufnahmen überein, die unterschiedliche Grade von Hirnschädigung und Entzündung zeigten.
Was das für künftige Gesundheits- und Umweltüberwachung bedeutet
Diese Arbeit zeigt, dass sorgfältig gestaltete Oberflächenchemie zuverlässigere und empfindlichere elektrochemische Biosensoren ermöglichen kann. Durch eine schnelle, tyrosinzielgerichtete elektrische Click-Reaktion erzeugen die Autorinnen und Autoren langlebige, gut organisierte Proteinschichten, die multiplexe Zytokinmessungen in winzigen Volumina nativem Serums unterstützen. Während die Nanplastik-Studie explorativ ist, veranschaulicht sie, wie solche Chips genutzt werden könnten, um Immunreaktionen auf Materialien, Krankheiten oder Therapien über die Zeit zu verfolgen. Langfristig könnte dieser Ansatz kompakte, bezahlbare Geräte antreiben, die Immun-Signale am Krankenbett oder im Feld auslesen und so klarere Momentaufnahmen davon liefern, wie der Körper auf seine Umwelt reagiert.
Zitation: Song, K., Liu, Y., Ma, Q. et al. Electrochemical tyrosine-click bioconjugation enables multiplexed cytokine sensing and immunoprofiling in native serum. Nat Commun 17, 4251 (2026). https://doi.org/10.1038/s41467-026-70815-3
Schlüsselwörter: elektrochemischer Biosensor, Zytokin-Sensorik, Proteinimmobilisierung, Nanoplastik-Exposition, Immunprofiling