Clear Sky Science · es
Eficacia económica de la prescripción guiada por farmacogenómica para trastornos psiquiátricos: una revisión sistemática y metaanálisis
Por qué tus genes pueden importar en la medicina de la salud mental
Muchas personas con depresión, esquizofrenia u otras enfermedades mentales tienen dificultades para encontrar un fármaco que realmente les ayude sin provocar efectos secundarios molestos. Este proceso de prueba y error resulta frustrante para los pacientes y costoso para los sistemas sanitarios. El artículo que se revisa aquí plantea una pregunta simple pero importante: si los médicos usaran información genética para ajustar los fármacos psiquiátricos a cada paciente, ¿merecerían los beneficios clínicos el coste adicional de las pruebas?
De la talla única al tratamiento a medida
La prescripción psiquiátrica estándar parte en gran medida de la suposición de que la mayoría de las personas responderán de forma similar al mismo fármaco y dosis. En la realidad, hasta un 60 % de los pacientes puede no responder bien y algunos experimentan reacciones adversas graves. La farmacogenómica —usar información genética de una persona para orientar la elección y la dosificación de fármacos— ofrece un enfoque más personalizado. Ciertos genes influyen en la rapidez con que el organismo procesa los medicamentos o en la sensibilidad de los receptores cerebrales a ellos. Al testar estos genes de antemano, los médicos pueden ajustar el tratamiento para reducir efectos secundarios, acortar el periodo de prueba y error y, potencialmente, mejorar la calidad de vida.
Cómo examinaron los investigadores los números
Los autores realizaron una revisión sistemática y un metaanálisis, lo que significa que buscaron cuidadosamente en varias bases de datos médicas y agruparon la evidencia de los mejores estudios económicos disponibles. Incluyeron 17 estudios en adultos con diagnósticos psiquiátricos como depresión mayor, esquizofrenia y trastorno por consumo de alcohol. Cada estudio comparó la atención habitual con la prescripción guiada por pruebas genéticas y presentó tanto resultados de salud como costes. La mayoría de los estudios emplearon modelos por ordenador para simular resultados a largo plazo, y muchos adoptaron una perspectiva “social” que trató de captar no solo el gasto médico sino también impactos más amplios, como la pérdida de productividad.
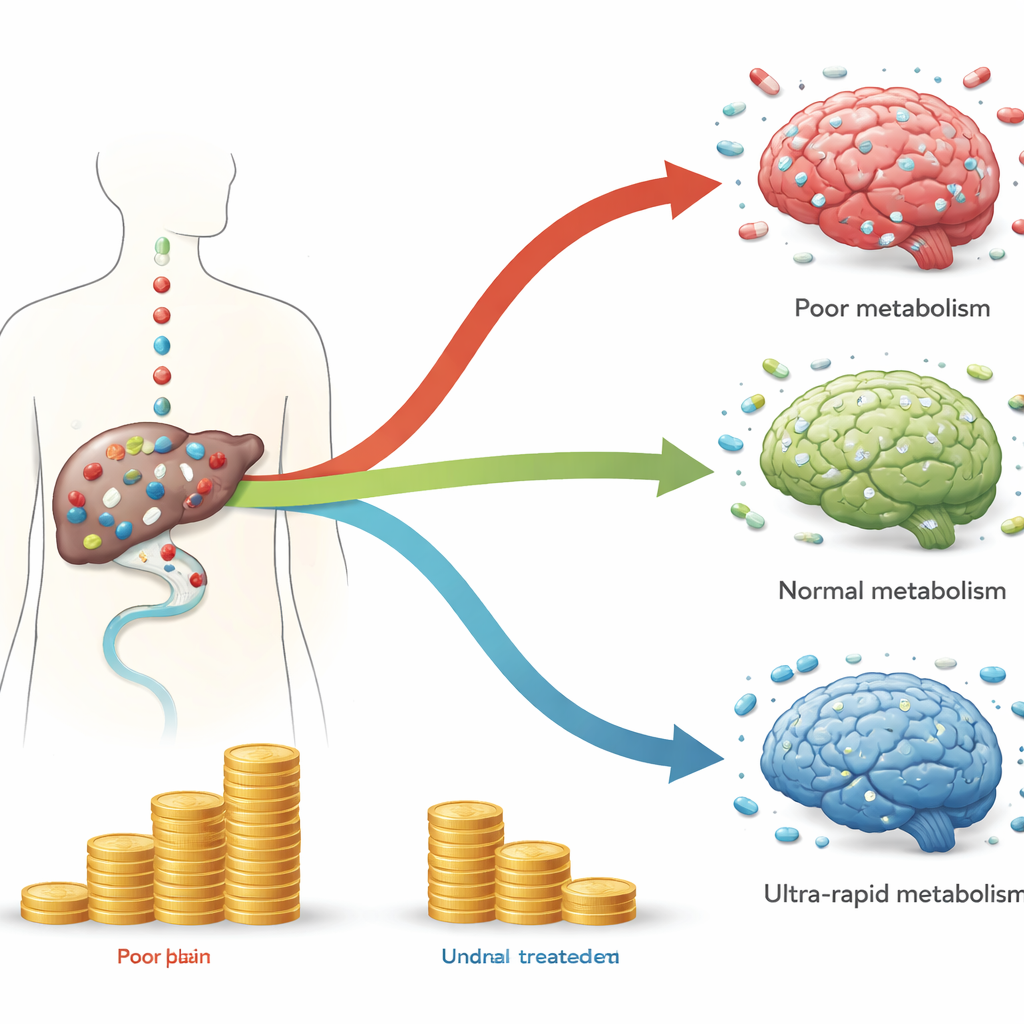
Qué muestra la evidencia sobre costes y beneficios
De los 17 estudios, aproximadamente el 88 % concluyó que la prescripción guiada por farmacogenómica era claramente rentable o incluso ahorraba costes en comparación con la atención estándar. Esto fue especialmente evidente en las pruebas multigénicas utilizadas en la depresión, donde varios análisis sugirieron que el test podría reducir los costes totales mientras mejoraba la salud. En la esquizofrenia, los estudios se centraron en usar pruebas genéticas para identificar quién tiene mayor o menor riesgo de una complicación sanguínea rara pero peligrosa por clozapina, un antipsicótico potente. Los modelos sugirieron que ajustar la intensidad del seguimiento de los pacientes según su riesgo genético también podría ser un uso eficiente de los recursos.
Por qué la respuesta aún no es concluyente
Para ir más allá de los estudios individuales, los autores combinaron datos de ocho estudios basados en modelos en un metaanálisis estadístico. Convirtieron los resultados de cada estudio en un “beneficio neto incremental”, una medida que expresa ganancias en salud y costes en términos monetarios. El resultado combinado fue positivo —lo que sugiere que la prescripción guiada por genética puede ser coste‑efectiva— pero los intervalos de confianza atravesaron el cero, lo que significa que el hallazgo no fue estadísticamente concluyente. Además, hubo una variación sustancial entre los estudios en métodos, horizontes temporales, tipos de prueba, fuentes de financiación y poblaciones de pacientes, lo que dificulta sacar conclusiones firmes. Algunos de los resultados más optimistas provenían de estudios vinculados a la industria que utilizaban paneles genéticos amplios y horizontes temporales largos, lo que plantea dudas sobre la aplicabilidad universal de esos hallazgos.
Qué podría significar esto para pacientes y sistemas sanitarios
Para las personas con depresión o esquizofrenia, el mensaje general es de esperanza cautelosa. La evidencia existente sugiere que emplear pruebas genéticas para ayudar a elegir medicamentos psiquiátricos puede, en muchos entornos, conducir a mejores resultados sin aumentar los costes globales —y puede incluso ahorrar dinero al prevenir efectos adversos graves y reducir tratamientos ineficaces. Sin embargo, dado que los estudios son muy heterogéneos y los ensayos del mundo real con seguimiento prolongado siguen siendo escasos, los responsables de políticas y los clínicos deberían ver la farmacogenómica como una herramienta prometedora y no como una solución garantizada. Se necesitarán métodos más consistentes, pruebas más amplias entre distintos fármacos y estudios que sigan a los pacientes durante años —no solo semanas— para demostrar con claridad cuándo y dónde la prescripción guiada por genes aporta buen valor tanto para los pacientes como para los presupuestos sanitarios.
Cita: Mason, E.R., Ali, M.Y., Gibson, D.S. et al. Economic effectiveness of pharmacogenomics-guided prescribing for psychiatric disorders: a systematic review and meta-analysis. Pharmacogenomics J 26, 12 (2026). https://doi.org/10.1038/s41397-026-00408-2
Palabras clave: farmacogenómica, medicamentos psiquiátricos, medicina personalizada, coste‑efectividad, tratamiento de la depresión