Clear Sky Science · de
Wirtschaftliche Wirksamkeit genetisch gesteuerter Pharmakogenomik-Verschreibung bei psychiatrischen Störungen: eine systematische Übersichtsarbeit und Meta-Analyse
Warum Ihre Gene für die Psychopharmakotherapie wichtig sein könnten
Viele Menschen mit Depression, Schizophrenie oder anderen psychischen Erkrankungen haben Schwierigkeiten, ein Medikament zu finden, das wirklich hilft, ohne lästige Nebenwirkungen zu verursachen. Dieser Trial‑and‑Error‑Prozess ist für Patientinnen und Patienten frustrierend und für Gesundheitssysteme kostspielig. Der hier besprochene Artikel stellt eine einfache, aber wichtige Frage: Wenn Ärzte genetische Informationen nutzten, um Patientinnen und Patienten den passenden psychiatrischen Wirkstoff zuzuordnen, wären der gesundheitliche Nutzen die zusätzlichen Testkosten wert?
Vom Einheitsansatz zur maßgeschneiderten Behandlung
Standardmäßige psychiatrische Verschreibungen gehen weitgehend davon aus, dass die meisten Menschen auf dasselbe Medikament und dieselbe Dosis ähnlich reagieren. Tatsächlich sprechen bis zu 60 % der Patientinnen und Patienten möglicherweise nicht gut an, und einige entwickeln schwere Nebenwirkungen. Pharmakogenomik – die Nutzung genetischer Informationen einer Person zur Steuerung von Arzneimittelwahl und Dosierung – bietet einen stärker maßgeschneiderten Ansatz. Bestimmte Gene beeinflussen, wie schnell der Körper Medikamente abbaut oder wie empfindlich Rezeptoren im Gehirn darauf reagieren. Durch vorab durchgeführte Gentests können Ärztinnen und Ärzte die Behandlung anpassen, Nebenwirkungen verringern, die Trial‑and‑Error‑Phase verkürzen und potenziell die Lebensqualität verbessern.
Wie die Forschenden die Zahlen analysierten
Die Autoren führten eine systematische Übersichtsarbeit und Meta‑Analyse durch, das heißt, sie durchsuchten sorgfältig mehrere medizinische Datenbanken und bündelten die Evidenz aus den besten verfügbaren ökonomischen Studien. Eingeschlossen wurden 17 Studien an Erwachsenen mit psychiatrischen Diagnosen wie Major Depression, Schizophrenie und Alkoholgebrauchsstörung. Jede Studie verglich die übliche Versorgung mit einer auf genetischen Tests basierenden Verschreibung und berichtete sowohl Gesundheitsauskommen als auch Kosten. Die meisten Studien nutzten Computermodelle, um langfristige Ergebnisse zu simulieren, und viele nahmen eine „gesellschaftliche“ Perspektive ein, die nicht nur medizinische Ausgaben, sondern auch breitere Auswirkungen wie Produktivitätsverluste erfassen wollte.
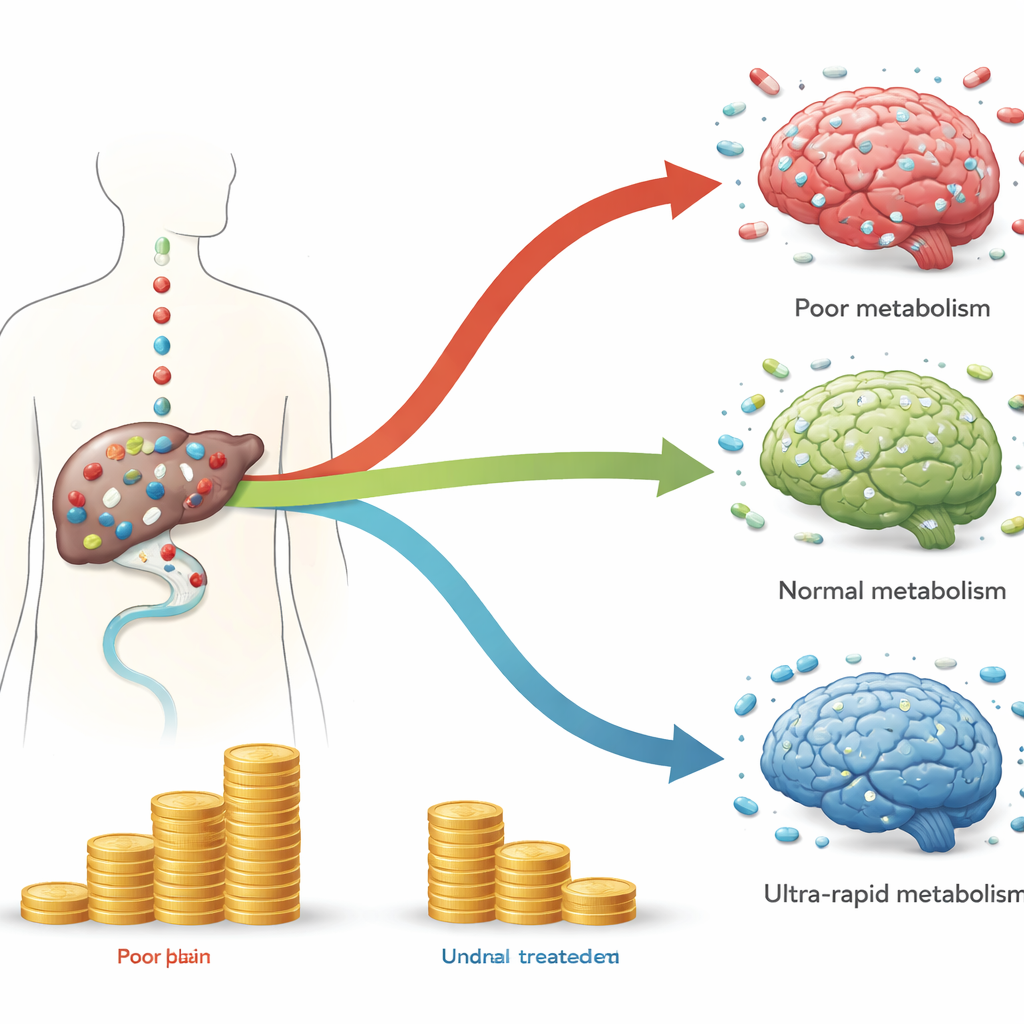
Was die Evidenz zu Kosten und Nutzen zeigt
In den 17 Studien kamen etwa 88 % zu dem Schluss, dass pharmakogenomisch gesteuerte Verschreibung entweder eindeutig kosteneffektiv war oder im Vergleich zur Standardversorgung sogar Geld sparte. Dies galt besonders für Multigen-Tests bei Depressionen, wo mehrere Analysen nahelegten, dass Tests die Gesamtkosten senken und gleichzeitig die Gesundheit verbessern könnten. Bei Schizophrenie konzentrierten sich Studien darauf, genetische Tests zu nutzen, um zu identifizieren, wer ein hohes oder niedriges Risiko für eine seltene, aber gefährliche Blutkomplikation durch Clozapin – ein starkes Antipsychotikum – hat. Die Modelle deuteten an, dass eine auf das genetische Risiko abgestimmte Anpassung der Überwachungsintensität verschiedener Patientengruppen ebenfalls eine sinnvolle Ressourcennutzung sein könnte.
Warum die Antwort noch nicht endgültig ist
Um über einzelne Studien hinauszugehen, kombinierten die Autoren Daten aus acht modellbasierten Studien in einer statistischen Meta‑Analyse. Sie wandelten die Ergebnisse jeder Studie in einen „inkrementellen Nettovorteil“ um, eine Kennzahl, die Gesundheitsgewinne und Kosten in Geldwerten ausdrückt. Das kombinierte Ergebnis war positiv – was dafür spricht, dass genetisch gesteuerte Verschreibung kosteneffektiv sein könnte – aber die Konfidenzintervalle kreuzten die Null, sodass das Ergebnis statistisch nicht sicher war. Zudem gab es erhebliche Unterschiede zwischen den Studien hinsichtlich Methoden, Zeithorizonten, Testtypen, Finanzierungsquellen und Patientengruppen, was feste Schlussfolgerungen erschwert. Einige der optimistischsten Ergebnisse stammten aus industrienahen Studien mit breiten Genpanels und langen Zeithorizonten, was Fragen zur Allgemeingültigkeit dieser Befunde aufwirft.
Was das für Patientinnen, Patienten und Gesundheitssysteme bedeuten könnte
Für Menschen mit Depression oder Schizophrenie ist die Gesamtbotschaft vorsichtig optimistisch. Die vorhandene Evidenz deutet darauf hin, dass der Einsatz genetischer Tests zur Auswahl psychiatrischer Medikamente in vielen Kontexten zu besseren Ergebnissen führen kann, ohne die Gesamtkosten zu erhöhen – und möglicherweise sogar Kosten spart, indem schwere Nebenwirkungen verhindert und verschwendete Behandlungen reduziert werden. Da die Studien jedoch stark variieren und realweltliche Langzeitstudien noch selten sind, sollten politische Entscheider und Kliniker Pharmakogenomik als ein vielversprechendes Instrument und nicht als garantierte Lösung betrachten. Einheitlichere Methoden, breitere Tests über verschiedene Wirkstoffe hinweg und Studien, die Patientinnen und Patienten über Jahre – nicht nur Wochen – verfolgen, werden nötig sein, um klar aufzuzeigen, wann und wo genbasierte Verschreibung für Patientinnen, Patienten und Gesundheitsbudgets echten Nutzen bringt.
Zitation: Mason, E.R., Ali, M.Y., Gibson, D.S. et al. Economic effectiveness of pharmacogenomics-guided prescribing for psychiatric disorders: a systematic review and meta-analysis. Pharmacogenomics J 26, 12 (2026). https://doi.org/10.1038/s41397-026-00408-2
Schlüsselwörter: Pharmakogenomik, psychiatrische Medikamente, personalisierte Medizin, Kosteneffizienz, Behandlung von Depressionen