Clear Sky Science · de
Das pulmonale Surfactantprotein D hemmt das Fortschreiten von Lungenkrebs durch Abschwächung der IL-4/STAT6-Signalübertragung
Warum der eigene Schutz der Lunge für Krebs wichtig ist
Lungenkrebs gehört weiterhin zu den tödlichsten Krebserkrankungen, unter anderem weil er häufig erst entdeckt wird, nachdem er bereits gestreut hat. Diese Studie untersucht einen wenig bekannten körpereigenen Verteidiger in der Lunge, ein Protein namens Surfactantprotein D (SP-D), und stellt eine einfache, aber wichtige Frage: Trägt dieser lokal produzierte Schutz zum Eindämmen von Lungenkrebs bei, und kann seine Verstärkung das Fortschreiten der Krankheit verlangsamen? Die Antwort der Forschenden lautet ja – zumindest in experimentellen Modellen und in Patientendaten – indem ein wachstumsförderndes Signal innerhalb der Krebszellen gedämpft wird.
Ein eingebauter Wächter in den Atemwegen
SP-D kommt normalerweise in der dünnen Flüssigkeitsschicht vor, die die Lungenbläschen auskleidet, wo es dem Immunsystem hilft, eindringende Erreger zu erkennen und zu bewältigen. Als die Autorinnen und Autoren die Genaktivität in 21 verschiedenen Krebsarten verglichen, fiel SP-D im Lungengewebe besonders auf: Sein Gen SFTPD ist in gesundem Lungengewebe deutlich aktiver als in Lungentumoren und sinkt in metastatischen (streuenden) Lungentumorabsiedelungen nahezu auf null. Die Mikroskopie humaner Tumorproben zeigte, dass die Krebszellen selbst SP-D vermissen, während nahegelegene normale Zellen am Tumorrand noch etwas produzieren. Dieses Muster legt nahe, dass Lungenzellen, wenn sie entarten und aggressiver werden, größtenteils die Produktion dieses Schutzproteins abschalten.
Verlangsamtes Tumorwachstum und verminderte Ausbreitung bei Mäusen
Um zu prüfen, ob dieses Verschwinden tatsächlich das Krankheitsverhalten beeinflusst, brachten die Forschenden menschliche Adenokarzinomzellen der Lunge (Zelllinie A549) dazu, vermehrt SP-D zu produzieren, und setzten sie in Mäuse ein. Im Vergleich zu Kontrolltumoren wuchsen die SP-D-aufgepeppten Tumoren langsamer und enthielten weniger teilende Zellen. Nachdem die Primärtumoren chirurgisch entfernt wurden, beobachteten die Forschenden, ob sich in entfernten Organen neue Tumorknoten bildeten. In Mäusen mit SP-D-überproduzierenden Tumoren waren Anzahl und Gesamtfläche sekundärer Tumoren in der Lunge deutlich reduziert. In einem separaten Experiment, das eher einer möglichen therapeutischen Anwendung entspricht, etablierten die Forschenden Lungentumoren und verabreichten dann SP-D-Protein per intranasaler Inhalation. Dadurch stieg SP-D direkt in der Lungenoberflächenflüssigkeit an; obwohl sich die Zahl neu gebildeter Tumorfoci nicht veränderte, wurden Anzahl und Größe größerer Tumorfoci signifikant verringert, was auf einen spezifischen Effekt auf Tumorprogression statt auf die initiale Aussaat hinweist.
Ein Schlüsselsignal wird abgeschwächt
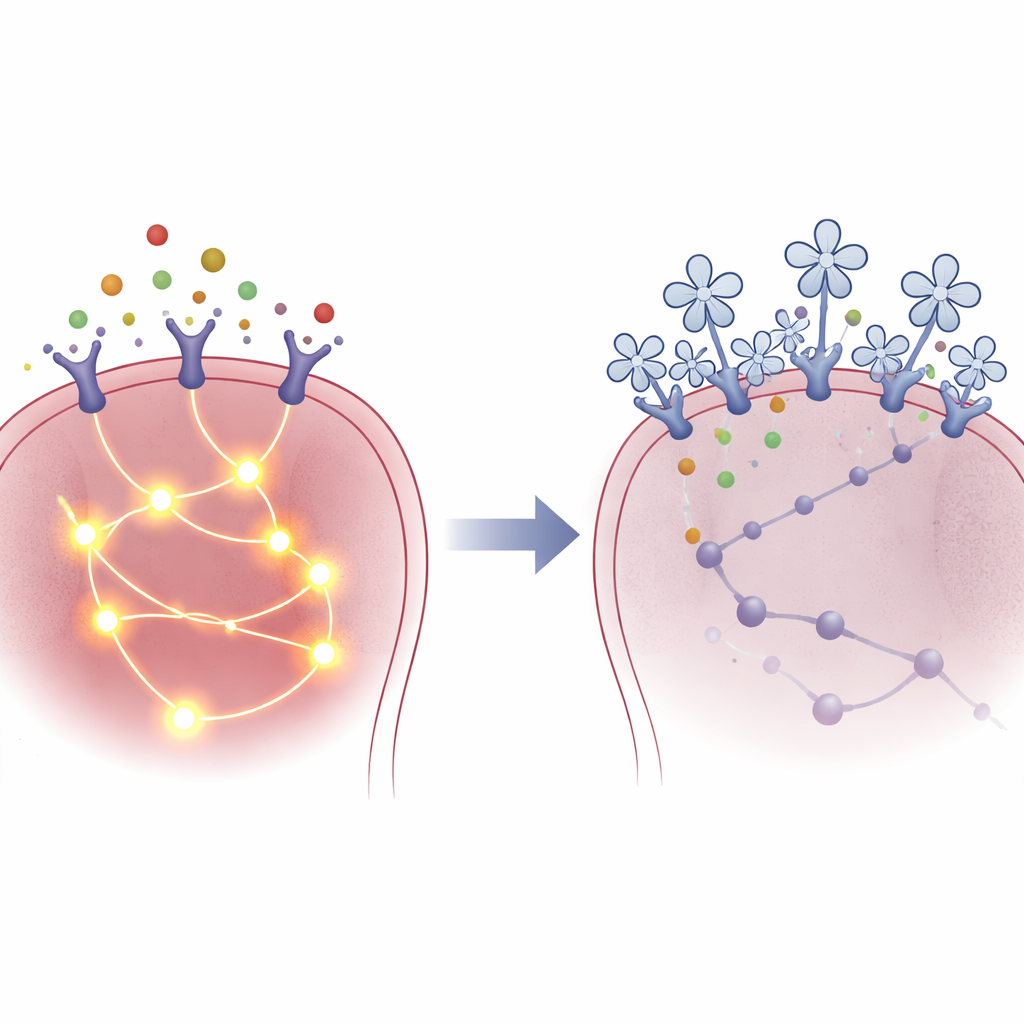
Die Autorinnen und Autoren fragten dann, wie SP-D diese Bremse innerhalb von Krebszellen bewirkt. Mithilfe von RNA-Sequenzierung verglichen sie die Genaktivität in Lungenkrebszellen, die SP-D ausgesetzt waren, mit unbehandelten Zellen. Mehrere wachstumsbezogene Signalwege wurden abgeschwächt, doch ein Signal hob sich besonders hervor: eine Kommunikationskaskade, die vom Immunboten Interleukin-4 (IL-4) und seinem Partnerprotein STAT6 angetrieben wird und für Überleben, Wachstum und Mobilität von Zellen bekannt ist. Wenn die Forschenden Lungenkrebszellen mit IL-4 oder einem verwandten Boten behandelten und anschließend SP-D zusetzten, sank die Aktivierung mehrerer Schlüssel-Signalproteine, darunter STAT6. Detaillierte Bindungsexperimente zeigten, dass SP-D in calciumabhängiger Weise direkt an den IL-4-Rezeptor auf der Zelloberfläche andocken kann. Diese Bindung störte die nachgeschaltete Aktivierung innerhalb der Zelle, obwohl IL-4 weiterhin teilweise mit seinem Rezeptor in Kontakt treten konnte, was darauf hindeutet, dass SP-D wie ein physikalischer Dämpfer auf diesen pro‑tumoralen Kanal wirkt.
Hinweise aus Patiententumoren
Um zu prüfen, ob dieser im Labor beobachtete Mechanismus auch beim Menschen relevant ist, analysierte das Team RNA-Daten von mehr als 1.100 Lungenadenokarzinomproben aus zwei unabhängigen Patientenkohorten. Tumoren mit hoher SFTPD-Expression zeigten konsistent geringere Aktivität von IL-4- und STAT6-Zielgenen sowie reduzierte inflammatorische und zellzyklusbezogene Checkpoint-Signalübertragung im Vergleich zu Tumoren mit niedriger SFTPD-Expression. Wenn Patientengruppen nach SP-D- und IL-4-ähnlicher Aktivität eingeteilt wurden, wiesen diejenigen mit hoher SFTPD- und niedriger IL-4-Signalaktivität die längste krankheitsfreie Zeit auf. Im Gegensatz dazu hatten Patienten mit niedriger SFTPD, aber starker IL-4‑ähnlicher Signalgebung das höchste Rückfallrisiko, was verdeutlicht, dass das Gleichgewicht zwischen diesem Schutzprotein und diesem Wachstumsweg klinische Ergebnisse mitprägen kann.
Was das für die zukünftige Versorgung bedeutet
Die Kernaussage für Nicht-Spezialisten lautet: Die Lunge ist kein passives Opfer bei Krebs – sie ist mit einem molekularen Schutz ausgestattet, SP-D, das direkt mit Lungenkrebszellen kommunizieren und ein wachstums- sowie ausbreitungsförderndes Signal dämpfen kann. Mit der Tumorprogression verlieren Tumoren diesen Schutz tendenziell, besonders bei Metastasierung. Durch Wiederherstellung von SP-D – entweder indem Krebszellen wieder zur Produktion angeregt werden oder indem das Protein in die Atemwege geliefert wird – gelang es den Forschenden, Tumorwachstum zu bremsen und größere metastatische Knoten bei Mäusen zu begrenzen, zum Teil durch Abschwächung der IL-4/STAT6-Signalübertragung. Obwohl noch viel Arbeit nötig ist, bevor dies zu einer Therapie werden könnte, erscheinen SP-D und die von ihm regulierten Signalwege jetzt als vielversprechende Ziele, um das Fortschreiten und Wiederauftreten von Lungentumoren zu verhindern.
Zitation: Mohammadi, A., Inayatullah, M., Schlosser, A. et al. Pulmonary surfactant protein D reduces lung cancer progression associated with decreased IL-4/STAT6 signaling. npj Precis. Onc. 10, 164 (2026). https://doi.org/10.1038/s41698-025-01163-6
Schlüsselwörter: Lungenkrebs, Surfactantprotein D, IL-4 STAT6 Signalübertragung, Tumormikroumgebung, Metastasierung