Clear Sky Science · ar
بروتين السطح الرئوي D يقلل تقدم سرطان الرئة مرتبطًا بتناقص إشارة IL-4/STAT6
لماذا يهم درع الرئة الذاتي في السرطان
يبقى سرطان الرئة أحد أكثر أنواع السرطان فتكًا، جزئيًا لأنه غالبًا ما يُكتشف بعد أن يكون قد انتشر بالفعل. تبحث هذه الدراسة في مدافع طبيعي غير معروف كثيرًا في رئتنا، وهو بروتين يدعى بروتين السطح الرئوي D (SP-D)، وتطرح سؤالًا بسيطًا لكنه قويًا: هل يساعد هذا الدرع المحلي في التحكم بسرطان الرئة، وهل يمكن أن يبطئ تعزيز وجوده المرض؟ يجد الباحثون الإجابة بنعم — على الأقل في النماذج التجريبية وبيانات المرضى — عن طريق خفض إشارة داخل الخلايا تعزز النمو.
حارس مدمج في المجاري الهوائية
يوجد SP-D عادة في الطبقة السائلة الرقيقة التي تغطي الحويصلات الهوائية في الرئة، حيث يساعد الجهاز المناعي على رصد ومعالجة الميكروبات الغازية. عندما فحص المؤلفون نشاط الجينات عبر 21 نوعًا مختلفًا من السرطان، وجدوا أن SP-D تميّز نسيج الرئة: جينها، SFTPD، نشط بدرجة أكبر في الرئة السليمة مقارنةً بأورام الرئة، وينخفض إلى ما يقرب من الصفر في رواسب سرطان الرئة النقيلية (المتصاعدة). أظهرت الميكروسكوبيات لعينات بشرية من الأورام أن الخلايا السرطانية نفسها تفتقر إلى SP-D، بينما لا تزال الخلايا الطبيعية القريبة عند حافة الورم تنتج بعضه. يشير هذا النمط إلى أنه مع تحول خلايا الرئة إلى خبيثة ثم إلى أكثر عدوانية، فإنها تقطع إلى حد كبير إنتاج هذا البروتين الوقائي.
إبطاء نمو الورم وانتشاره في الفئران
للبحث عما إذا كان هذا الفقدان مهمًا بالفعل لسلوك المرض، أجبرت الفريق خلايا سرطان الغدة الرئوية البشرية (سلالة A549) على إنتاج كمية زائدة من SP-D وزرعوها في فئران. بالمقارنة مع الأورام الضابطة، نمت الأورام المعززة بـ SP-D ببطء أكبر واحتوت على خلايا أقل منقسمة. بعد أن استأصل الجراحون الكتل الأولية، انتظر الباحثون لمعرفة ما إذا كانت عقيدات ورمية جديدة ستظهر في الأعضاء البعيدة. في الفئران التي كانت أورامها تفرط في إنتاج SP-D، انخفض عدد ومساحة الأورام الثانوية في الرئتين بشكل حاد. في تجربة منفصلة تحاكي بشكل أوثق كيفية توصيل المعالجة، نشأ الباحثون أورامًا رئوية ثم أعطوا بروتين SP-D عن طريق الاستنشاق داخل الأنف. رفع هذا مستويات SP-D مباشرة في سائل بطانة الرئة، وبينما لم يغير عدد البقع الورمية المتكونة، فقد خفّض بشكل كبير عدد وحجم البؤر الورمية الأكبر، مما يشير إلى تأثير محدد على تقدم الورم بدلاً من البذر الابتدائي.
إخماد إشارة نمو رئيسية
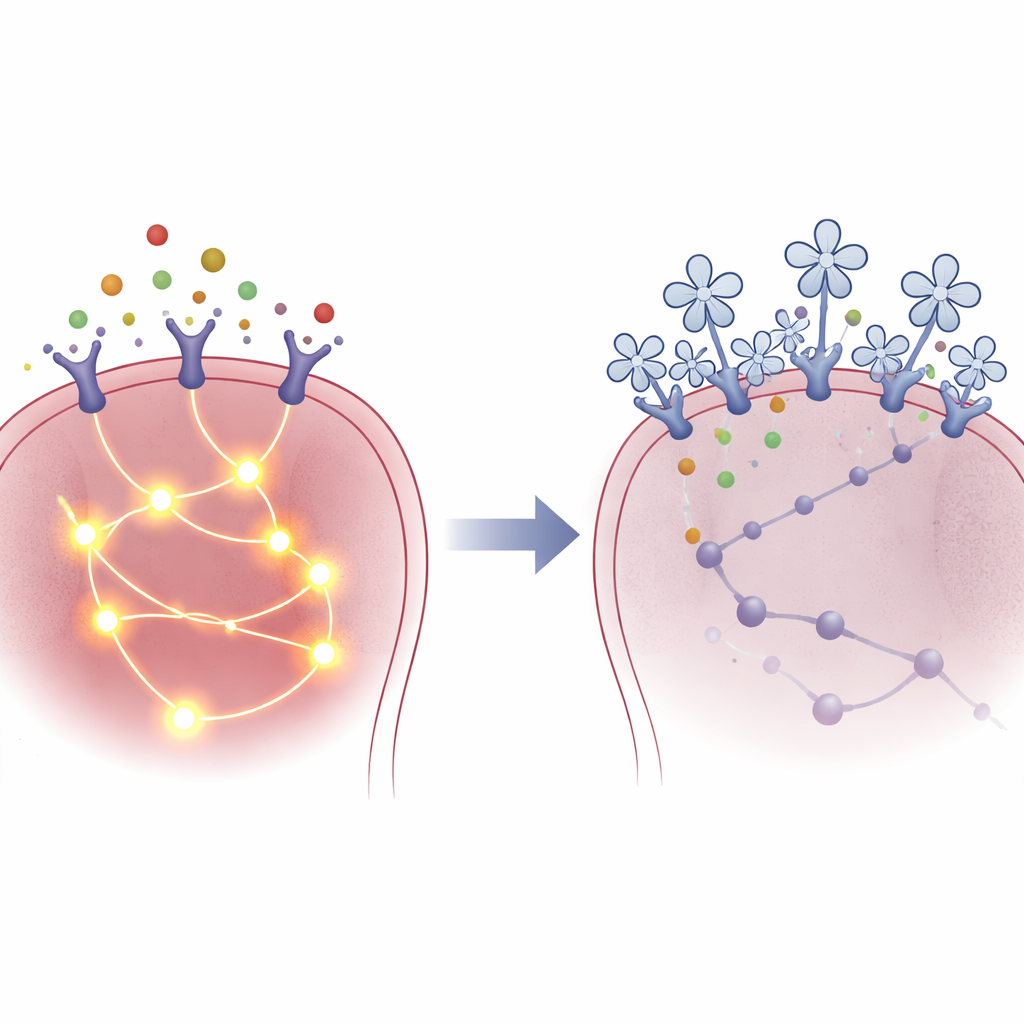
سأل المؤلفون بعد ذلك كيف يمارس SP-D هذا الكبح داخل الخلايا السرطانية. باستخدام تسلسل RNA، قارنوا نشاط الجينات في خلايا سرطان الرئة المعرضة لـ SP-D مع الخلايا غير المعالجة. تراجعت عدة مسارات مرتبطة بالنمو، لكن إشارة واحدة برزت: مسار تواصل تحركه المرسل المناعي إنترلوكين-4 (IL-4) وبروتينه الشريك STAT6، المعروف بأنه يعزز بقاء الخلايا ونموها وحركتها. عندما حمّض الباحثون خلايا سرطان الرئة في محلول يحتوي على IL-4 أو مرسل ذو صلة ثم أضافوا SP-D، لاحظوا أن تنشيط عدة بروتينات إشارية رئيسية، بما في ذلك STAT6، انخفض. أوضحت تجارب الربط التفصيلية أن SP-D يمكن أن يرتبط مباشرة بمستقبل IL-4 على غشاء الخلية بطريقة معتمدة على الكالسيوم. أعاق هذا الارتباط التفعيل المتدفق داخل الخلية، رغم أن IL-4 كان لا يزال قادرًا على إجراء تلامس جزئي مع مستقبلاته، ما يوحي بأن SP-D يعمل كمعطّل مادي لهذه القناة المشجعة للسرطان.
دلائل من أورام المرضى
لاختبار ما إذا كانت هذه الآلية المعملية تنطبق على البشر، حلل الفريق بيانات RNA لأكثر من 1100 عينة من سرطان الغدة الرئوية مأخوذة من مجموعتين مستقلتين من المرضى. أظهرت الأورام ذات التعبير العالي عن SFTPD نشاطًا أقل باستمرار لجينات الهدف المرتبطة بـ IL-4 وSTAT6، إلى جانب تناقص في الإشارات الالتهابية وإشارات نقاط التفتيش في دورة الخلية، مقارنةً بالأورام ذات التعبير المنخفض عن SFTPD. عندما جُمّع المرضى بحسب كل من مستويات SP-D ونشاطات المرتبطة بـ IL-4، استمتع من كانت أورامهم ذات SFTPD عالية وإشارة IL-4 منخفضة بأطول فترة خلو من عودة المرض. في المقابل، كان لدى المرضى ذوي SFTPD المنخفض لكن النشاط القوي من نوع IL-4 أعلى خطر للانتكاس، ما يؤكد أن التوازن بين هذا البروتين الوقائي وهذا المسار النمائي قد يساهم في تشكيل النتائج السريرية.
ماذا يعني هذا لرعاية المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن الرئة ليست ضحية سلبية في السرطان: فهي مزودة بدرع جزيئي خاص بها، SP-D، يمكنه التفاعل مباشرة مع خلايا سرطان الرئة وتخفيف إشارة تعزز النمو والانتشار. مع تطور الأورام، تميل إلى فقدان هذا الدرع، خاصة عندما تصبح نقيلية. عن طريق استعادة SP-D — إما بإجبار الخلايا السرطانية على إنتاجه مجددًا أو بتوصيل البروتين إلى المجاري الهوائية — استطاع الباحثون إبطاء نمو الورم والحد من العقيدات النقيلية الأكبر في الفئران، جزئيًا عن طريق إخماد إشارات IL-4/STAT6. وبينما لا يزال العمل كثيرًا قبل أن يتحول هذا إلى علاج، يبرز الآن SP-D والمسارات التي يتحكم بها كأهداف واعدة لمنع أورام الرئة من التقدم والعودة.
الاستشهاد: Mohammadi, A., Inayatullah, M., Schlosser, A. et al. Pulmonary surfactant protein D reduces lung cancer progression associated with decreased IL-4/STAT6 signaling. npj Precis. Onc. 10, 164 (2026). https://doi.org/10.1038/s41698-025-01163-6
الكلمات المفتاحية: سرطان الرئة, بروتين السطح الرئوي D, إشارة IL-4 STAT6, البيئة المجهرية للورم, النقائل